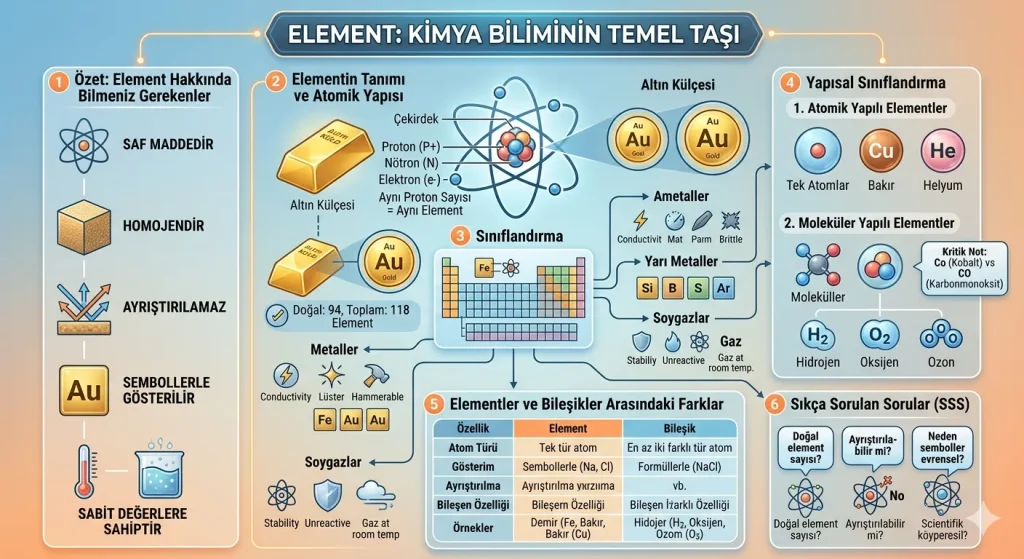
Elementler, kimyanın en temel yapı taşlarıdır. Çevremizdeki maddelerin büyük bölümü elementlerin tek başına veya farklı şekillerde birleşmesiyle oluşur. Bir elementin kimliğini belirleyen temel özellik, atom çekirdeğindeki proton sayısıdır.
Örneğin bir altın parçasındaki tüm atomlar altın atomudur. Bu nedenle altın bir elementtir. Aynı şekilde demir, bakır, oksijen ve hidrojen de elementlere örnektir.
Önemli bilgi: Elementler saf maddedir ve tek tür atomdan oluşur. Bu nedenle fiziksel ya da kimyasal yöntemlerle daha basit maddelere ayrılamaz.
Element Nedir?
Element, aynı cins atomlardan oluşan saf maddeye denir. Bir maddenin element sayılabilmesi için yapısındaki atomların proton sayılarının aynı olması gerekir.
Elementler, periyodik tabloda belirli sembollerle gösterilir. Örneğin hidrojen H, oksijen O, karbon C, demir Fe, altın ise Au sembolüyle gösterilir.
Elementleri daha iyi anlamak için önce Atom Nedir? konusunu öğrenmek faydalı olur.
Element Saf Madde midir?
Evet, elementler saf maddedir. Çünkü elementlerin yapısında tek tür atom bulunur. Yapısında farklı tür atomlar bulunan saf maddelere ise bileşik denir.
Saf maddeler genel olarak iki gruba ayrılır:
- Elementler: Tek tür atomdan oluşur.
- Bileşikler: Farklı tür atomların belirli oranlarda birleşmesiyle oluşur.
| Saf Madde Türü | Yapısı | Örnek |
|---|---|---|
| Element | Tek tür atom içerir. | Demir, oksijen, altın |
| Bileşik | Farklı tür atomlar belirli oranlarda birleşir. | Su, tuz, karbondioksit |
Elementlerin Genel Özellikleri
- Tek tür atomdan oluşurlar.
- Saf maddedirler.
- Sembollerle gösterilirler.
- Fiziksel ve kimyasal yollarla daha basit maddelere ayrılamazlar.
- Belirli erime noktası, kaynama noktası ve yoğunluk gibi ayırt edici özelliklere sahiptirler.
- Periyodik tabloda belirli bir atom numarasıyla yer alırlar.
Elementler Nasıl Gösterilir?
Elementler evrensel sembollerle gösterilir. Bu semboller genellikle elementin Latince veya İngilizce adından gelir. Element sembollerinin ilk harfi her zaman büyük yazılır. Eğer sembol iki harfliyse ikinci harf küçük yazılır.
| Element | Sembol | Örnek Kullanım |
|---|---|---|
| Hidrojen | H | H2 |
| Oksijen | O | O2 |
| Karbon | C | C |
| Demir | Fe | Fe |
| Altın | Au | Au |
Dikkat: Element sembollerinde büyük-küçük harf önemlidir. Co kobalt elementidir; CO ise karbonmonoksit bileşiğidir.
Elementlerin Yapısı
Elementler atomlardan oluşur. Bir elementin tüm atomları aynı proton sayısına sahiptir. Proton sayısı, elementin kimliğini belirler.
Örneğin tüm karbon atomlarının proton sayısı 6’dır. Bir atomun proton sayısı değişirse artık o atom başka bir elemente ait olur.
Atomik ve Moleküler Yapılı Elementler
Elementler doğada atomik veya moleküler yapıda bulunabilir.
Atomik Yapılı Elementler
Bazı elementler doğada tek tek atomlar halinde bulunur. Metaller ve soygazlar genellikle atomik yapılıdır.
Moleküler Yapılı Elementler
Bazı elementler ise doğada aynı tür atomların bir araya gelmesiyle oluşan moleküller halinde bulunur.
Elementlerin Sınıflandırılması
Elementler periyodik tabloda benzer özelliklerine göre sınıflandırılır. En temel sınıflandırma metaller, ametaller, yarı metaller ve soygazlar şeklindedir.
| Element Grubu | Temel Özellikleri | Örnekler |
|---|---|---|
| Metaller | Isı ve elektriği iyi iletir, parlaktır, tel ve levha haline getirilebilir. | Demir, bakır, altın |
| Ametaller | Genellikle ısı ve elektriği iyi iletmez, kırılgan yapıdadır. | Karbon, oksijen, azot |
| Yarı Metaller | Metal ve ametal özelliklerini birlikte gösterebilir. | Bor, silisyum |
| Soygazlar | Kararlı yapıdadır, tepkimeye girme isteği düşüktür. | Helyum, neon, argon |
Elementlerin sınıflandırılması hakkında daha fazla bilgi için Periyodik Tablo Nedir? yazısını inceleyebilirsin.
Element ve Bileşik Arasındaki Fark
Elementler ve bileşikler saf madde olmaları bakımından benzerdir. Ancak yapıları farklıdır. Elementler tek tür atomdan oluşurken, bileşikler farklı tür atomların belirli oranlarda birleşmesiyle oluşur.
| Özellik | Element | Bileşik |
|---|---|---|
| Atom türü | Tek tür atom içerir. | En az iki farklı tür atom içerir. |
| Gösterim | Sembollerle gösterilir. | Formüllerle gösterilir. |
| Ayrıştırılma | Fiziksel veya kimyasal yollarla ayrıştırılamaz. | Kimyasal yollarla ayrıştırılabilir. |
| Örnek | Fe, O2, Au | H2O, NaCl, CO2 |
Bu konunun devamı için Bileşik Nedir? yazısına geçebilirsin.
Sık Yapılan Hatalar
1. Her saf maddeyi element sanmak
Her element saf maddedir; ancak her saf madde element değildir. Bileşikler de saf maddedir.
2. Element sembollerinde büyük-küçük harfi önemsememek
Element sembollerinde ilk harf büyük, ikinci harf küçük yazılır. Co kobalt elementidir; CO ise karbonmonoksit bileşiğidir.
3. Oksijen gazını bileşik sanmak
Oksijen gazı O2 şeklinde iki oksijen atomundan oluşur. Farklı tür atom içermediği için bileşik değil, moleküler yapılı elementtir.
4. Elementlerin kimyasal yollarla ayrışabileceğini düşünmek
Elementler kimyasal yollarla daha basit maddelere ayrıştırılamaz. Ancak nükleer süreçlerde başka elementlere dönüşebilirler.
Element Konusu Özeti
- Element, aynı tür atomlardan oluşan saf maddedir.
- Elementlerin yapısında tek tür atom bulunur.
- Elementler fiziksel veya kimyasal yollarla daha basit maddelere ayrılamaz.
- Elementler sembollerle gösterilir.
- Element sembollerinde büyük-küçük harf önemlidir.
- Elementler atomik veya moleküler yapılı olabilir.
- Metaller, ametaller, yarı metaller ve soygazlar element sınıflarına örnektir.
- Elementler tek tür atom içerirken, bileşikler farklı tür atomlar içerir.
Element Nedir? Mini Test
1. Element nedir?
- A) Farklı tür atomlardan oluşan karışım
- B) Aynı tür atomlardan oluşan saf madde
- C) Sadece sıvı halde bulunan madde
- D) Fiziksel yollarla ayrılabilen karışım
Doğru cevap: B
Açıklama: Element, aynı tür atomlardan oluşan saf maddedir.
2. Aşağıdakilerden hangisi elementtir?
- A) Su
- B) Tuz
- C) Demir
- D) Karbondioksit
Doğru cevap: C
Açıklama: Demir, Fe sembolüyle gösterilen bir elementtir.
3. Elementler nasıl gösterilir?
- A) Sembollerle
- B) Cümlelerle
- C) Sadece sayılarla
- D) Karışım adlarıyla
Doğru cevap: A
Açıklama: Elementler H, O, C, Fe gibi sembollerle gösterilir.
4. O2 neden bileşik değildir?
- A) Çünkü gaz halindedir.
- B) Çünkü sadece oksijen atomlarından oluşur.
- C) Çünkü sıvıdır.
- D) Çünkü farklı atom türleri içerir.
Doğru cevap: B
Açıklama: O2 yalnızca oksijen atomlarından oluştuğu için moleküler yapılı elementtir.
5. Aşağıdakilerden hangisi element sembollerinin yazımı için doğrudur?
- A) Tüm harfler küçük yazılır.
- B) Tüm harfler büyük yazılır.
- C) İlk harf büyük, varsa ikinci harf küçük yazılır.
- D) Sembol yazımında büyük-küçük harf önemli değildir.
Doğru cevap: C
Açıklama: Element sembollerinde ilk harf büyük, ikinci harf küçük yazılır. Örneğin Co kobalttır, CO bileşiktir.
Sıkça Sorulan Sorular
Element nedir?
Element, aynı tür atomlardan oluşan ve daha basit maddelere ayrıştırılamayan saf maddedir.
Elementler saf madde midir?
Evet. Elementler tek tür atomdan oluştuğu için saf maddedir.
Elementler fiziksel yöntemlerle ayrılır mı?
Hayır. Elementler fiziksel yöntemlerle daha basit maddelere ayrılamaz.
Elementler kimyasal yöntemlerle ayrılır mı?
Hayır. Elementler kimyasal yöntemlerle daha basit maddelere ayrılamaz.
Oksijen gazı element midir?
Evet. Oksijen gazı O2 şeklinde bulunabilir ve yalnızca oksijen atomlarından oluştuğu için elementtir.
Element ile bileşik arasındaki fark nedir?
Element tek tür atom içerir. Bileşik ise farklı tür atomların belirli oranlarda birleşmesiyle oluşur.
Bu Konudan Sonra Ne Öğrenmeliyim?
Element konusunu öğrendikten sonra şu konulara geçebilirsin:
- Bileşik Nedir?
- Element ve Bileşik Arasındaki Farklar
- Periyodik Tablo Nedir?
- Atom Nedir?
- Homojen ve Heterojen Karışımlar Nedir?
Bu yazı Elementler, Bileşikler ve Karışımlar Konu Rehberi‘nin bir parçasıdır.
