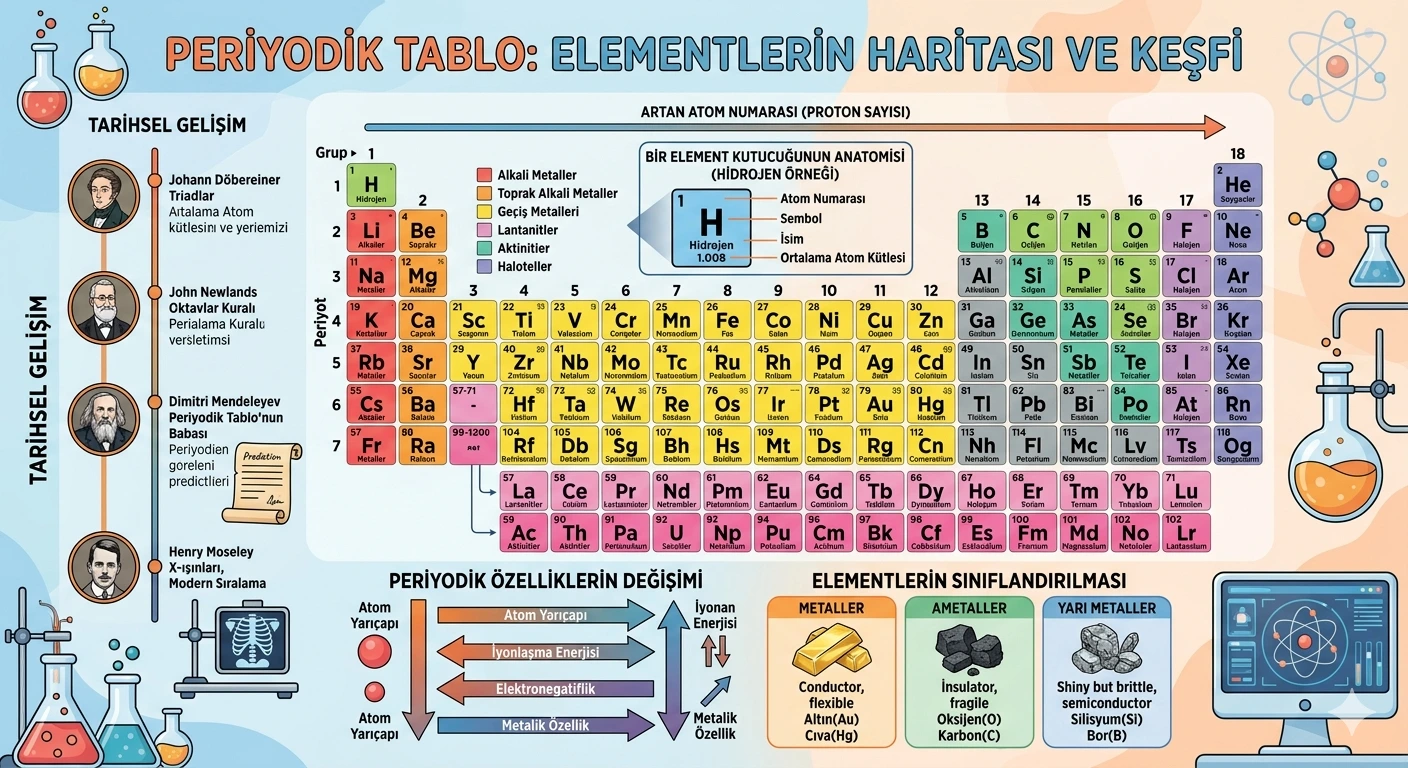
Periyodik tablo, evrendeki tüm elementlerin kimlik kartlarını içeren sistematik bir haritadır. Doğada bulunan veya laboratuvarda sentezlenen 118 elementin atom numaralarına ve kimyasal özelliklerine göre sıralandığı bu çizelge, modern kimyanın temelini oluşturur. Bu sistem sayesinde elementlerin birbirleriyle nasıl etkileşime gireceğini ve hangi fiziksel özelliklere sahip olduğunu öngörmek mümkün hale gelir.
Periyodik Tabloya Kısa Bir Bakış (Özet)
| Özellik | Açıklama |
|---|---|
| Sıralama Ölçütü | Artan atom numaralarına (proton sayısı) göre düzenlenmiştir. |
| Satır ve Sütunlar | 7 Periyot (satır) ve 18 Grup (sütun) bulunur. |
| Element Sayısı | Güncel olarak 118 element yer alır. |
| Temel Gruplar | Metaller, Ametaller, Yarı Metaller ve Soygazlar. |
Periyodik Tablo Nedir? Element Kutucuğunun Anatomisi
Periyodik sistem, elementlerin sadece bir listesi değil, aralarındaki ilişkileri gösteren dinamik bir yapıdır. Tablodaki her bir kutucuk, o elementin “kimlik bilgilerini” taşır. Atomun yapısı ve tanecikleri hakkında bilgi sahibi olmak, bu kutucuklardaki verileri okumayı kolaylaştırır.
Bir element kutucuğunda genellikle şu bilgiler yer alır:
- Atom Numarası: Elementin proton sayısını belirtir ve tablodaki yerini belirleyen temel değerdir.
- Element Sembolü: Elementin Latince isminden türetilen bir veya iki harfli simgedir (Örn: Altın için Au).
- Element Adı: Elementin yaygın olarak kullanılan ismidir.
- Ortalama Atom Kütlesi: Elementin izotoplarının ağırlıklı ortalamasını gösterir.
Periyodik Sistemin Tarihsel Gelişimi
Elementlerin sınıflandırılması süreci, bilim insanlarının benzer özellik gösteren maddeleri bir araya getirme çabasıyla başlamıştır. İlk başlarda atom kütleleri baz alınırken, modern sistemde atom numaraları esas alınmıştır.
İlk Sınıflandırma Denemeleri
- Johann Döbereiner: Benzer özellik gösteren elementleri “Triadlar” adı verilen üçlü gruplara ayırmıştır.
- John Newlands: Elementleri atom kütlelerine göre sıralamış ve “Oktavlar Kuralı” ile her sekizinci elementin benzer özellik gösterdiğini savunmuştur.
- Lothar Meyer ve Dimitri Mendeleyev: Birbirinden habersiz olarak elementleri benzer özelliklerine göre sıralamışlardır.
Biliyor muydunuz? Dimitri Mendeleyev, periyodik tablonun babası kabul edilir. O dönemde henüz keşfedilmemiş olan Galyum ve Germanyum gibi elementlerin yerini boş bırakmış ve bu elementlerin özelliklerini hayranlık uyandırıcı bir doğrulukla tahmin etmiştir.
Modern Tablo: Henry Moseley
Mendeleyev’in atom kütlesine dayalı sistemindeki hatalar, Henry Moseley’in çalışmalarıyla giderilmiştir. Moseley, X-ışınları deneyi ile elementlerin fiziksel ve kimyasal özelliklerinin atom kütlesine değil, atom numarasına (proton sayısına) bağlı olduğunu kanıtlamıştır. Günümüzde kullandığımız modern periyodik sistem bu ilkeye dayanır.
Periyodik Tablonun Yapısı: Gruplar ve Periyotlar
Tablo, elementlerin özelliklerini tahmin etmeyi sağlayan dikey ve yatay sütunlardan oluşur.
Gruplar (Dikey Sütunlar)
Aynı gruptaki elementlerin genellikle son katmanlarındaki elektron sayıları aynıdır, bu da benzer kimyasal tepkimeler vermelerini sağlar. Toplam 18 grup vardır:
- 1A Grubu (Alkali Metaller): Çok aktif metallerdir. Kritik Not: Hidrojen bu gruptadır ancak bir metal değil, ametaldir.
- 2A Grubu (Toprak Alkali Metaller): Aktif metallerdir.
- 7A Grubu (Halojenler): Tuz yapıcılar olarak bilinirler, çok aktiftirler.
- 8A Grubu (Soygazlar): Kararlı yapıdadırlar, tepkimeye girme eğilimleri çok düşüktür.
- B Grupları: Tablonun orta kısmında yer alan “Geçiş Metalleri”dir.
Periyotlar (Yatay Satırlar)
Periyodik sistemde 7 tane periyot bulunur. Bir elementin periyot numarası, o elementin elektronlarının bulunduğu katman sayısını verir. Örneğin, 3. periyottaki bir elementin elektronları 3 katmana dağılmıştır.
Elementlerin Sınıflandırılması
Elementler; görünüm, iletkenlik ve kimyasal bağ kurma eğilimlerine göre üç ana gruba ayrılırlar:
| Özellik | Metaller | Ametaller | Yarı Metaller |
|---|---|---|---|
| Görünüm | Parlaktır. | Mattır. | Genellikle parlaktır. |
| İletkenlik | Isı ve elektriği çok iyi iletirler. | İletken değildirler (Grafit hariç). | Metallerden az, ametallerden çok iletirler. |
| İşlenebilirlik | Tel ve levha haline gelebilirler. | Kırılgandırlar, işlenemezler. | Kırılgan olmalarına rağmen işlenebilirler. |
| Oda Koşulları | Cıva hariç katıdırlar. | Katı, sıvı veya gaz olabilirler. | Tamamı katıdır. |
Daha detaylı bir liste için elementler saf madde sayfamızı ziyaret edebilirsiniz.
Periyodik Özelliklerin Değişimi (Trendler)
Periyodik tabloda bir yöne doğru hareket edildiğinde elementlerin özellikleri belirli bir düzen içinde değişir. Bu değişimleri bilmek, kimya sorularını çözmede en büyük yardımcınızdır.
| Özellik | Soldan Sağa (Aynı Periyotta) | Yukarıdan Aşağıya (Aynı Grupta) |
|---|---|---|
| Atom Numarası | Artar | Artar |
| Atom Yarıçapı | Azalır (Çekirdek çekimi artar) | Artar (Katman sayısı artar) |
| İyonlaşma Enerjisi | Genellikle Artar | Azalır |
| Elektronegatiflik | Artar (8A hariç) | Azalır |
| Metalik Özellik | Azalır | Artar |
Sıkça Sorulan Sorular
1. Periyodik tabloda neden bazı elementler tablonun en altında ayrı durur?
Tablonun en altında yer alan iki satır (Lantanitler ve Aktinitler), tablonun çok genişlemesini önlemek ve estetik yapıyı korumak için aşağıya alınmıştır. Aslında 6. ve 7. periyodun parçalarıdır.
2. Yarı metallerin önemi nedir?
Yarı metaller (Bor, Silisyum vb.), özellikle elektronik sanayisinde yarı iletken özellikleri nedeniyle kritik öneme sahiptir. Bilgisayar çiplerinden güneş panellerine kadar pek çok teknolojide kullanılırlar.
3. Soygazlar neden tepkimeye girmez?
Soygazların en dış katmanları tamamen elektronla doludur. Bu “kararlı” yapı, onların başka elementlerle elektron alışverişi yapma veya ortaklaşma ihtiyacını ortadan kaldırır.
4. Hidrojen neden bir istisnadır?
Hidrojen 1A grubunda (metallerin arasında) yer almasına rağmen bir ametaldir. Bunun sebebi, atom numarasının 1 olması ve metalik özellik göstermemesidir.
Sonuç
Periyodik tablo, karmaşık görünen doğayı basit ve anlaşılır bir düzene oturtur. Elementlerin yerini ve özelliklerini kavramak, sadece kimya derslerinde değil; biyoloji, fizik ve mühendislik gibi pek çok alanda temel oluşturur. Tablodaki trendleri ve grup özelliklerini öğrendikten sonra, bu elementlerin nasıl bağlar kurduğunu anlamak için kimyasal türler arası etkileşimler konusuna geçiş yapabilirsiniz.
