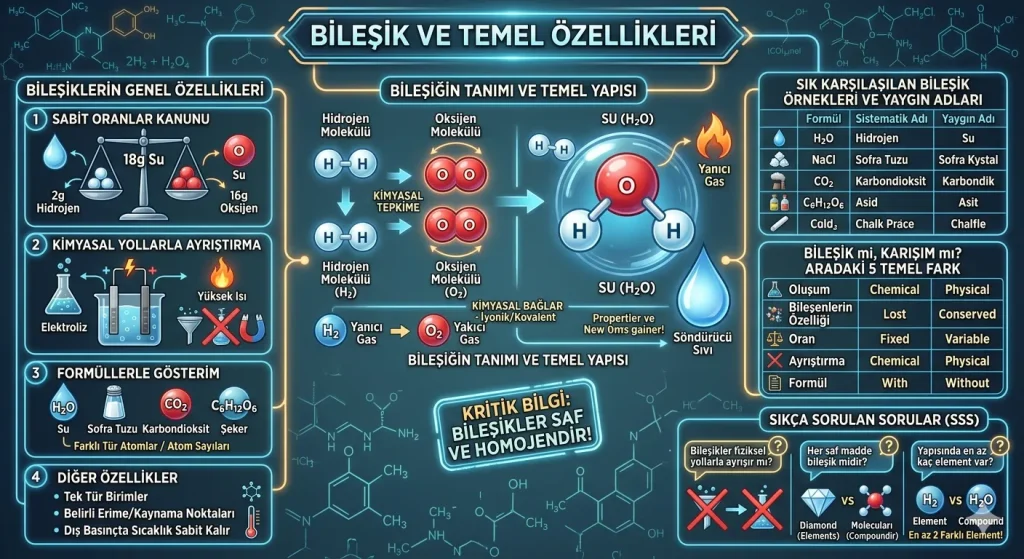
Bileşikler, kimyada maddelerin sınıflandırılmasında önemli bir yere sahiptir. Elementler tek tür atomdan oluşurken, bileşikler farklı tür atomların belirli oranlarda birleşmesiyle oluşur.
Örneğin su, hidrojen ve oksijen elementlerinin belirli oranda birleşmesiyle oluşan bir bileşiktir. Suyun formülü H2O şeklindedir. Bu formül, su molekülünde iki hidrojen atomu ve bir oksijen atomu bulunduğunu gösterir.
Önemli bilgi: Bileşikler saf maddedir; ancak element değildir. Çünkü bileşiklerin yapısında en az iki farklı element bulunur.
Bileşik Nedir?
Bileşik, farklı tür element atomlarının belirli oranlarda kimyasal bağlarla birleşmesi sonucu oluşan saf maddedir. Bileşik oluşurken elementler kimyasal değişime uğrar ve ortaya yeni özelliklere sahip bir madde çıkar.
Örneğin hidrojen yanıcı, oksijen ise yanmayı destekleyici bir gazdır. Bu iki element belirli oranda birleştiğinde su bileşiği oluşur. Su ise yangın söndürmede kullanılabilen, hidrojen ve oksijenden farklı özelliklere sahip bir maddedir.
Bileşikler Saf Madde midir?
Evet, bileşikler saf maddedir. Çünkü belirli bir kimyasal formülleri ve sabit bileşimleri vardır. Bir bileşiğin her saf örneği aynı tür taneciklerden oluşur.
Saf maddeler iki gruba ayrılır:
- Elementler: Tek tür atomdan oluşur.
- Bileşikler: Farklı tür atomların belirli oranlarda birleşmesiyle oluşur.
| Saf Madde Türü | Yapısı | Örnek |
|---|---|---|
| Element | Tek tür atom içerir. | Demir, oksijen, altın |
| Bileşik | En az iki farklı element içerir. | Su, tuz, karbondioksit |
Bileşiklerin Genel Özellikleri
- En az iki farklı elementten oluşurlar.
- Saf maddedirler.
- Belirli bir kimyasal formülleri vardır.
- Elementler belirli oranlarda birleşir.
- Kendisini oluşturan elementlerin özelliklerini göstermezler.
- Fiziksel yöntemlerle bileşenlerine ayrılamazlar.
- Kimyasal yollarla bileşenlerine ayrılabilirler.
- Belirli erime ve kaynama noktalarına sahip olabilirler.
Bileşikler Nasıl Oluşur?
Bileşikler, element atomlarının kimyasal bağlarla birleşmesi sonucunda oluşur. Bu bağlar iyonik bağ, kovalent bağ veya farklı kimyasal bağ türleri olabilir.
Bileşik oluşumu bir kimyasal değişimdir. Çünkü bu süreçte atomlar arasındaki bağlar değişir ve yeni özelliklere sahip bir madde meydana gelir.
Kimyasal bağlar hakkında daha fazla bilgi için Kimyasal Bağ Nedir? yazısını inceleyebilirsin.
Bileşikler Nasıl Gösterilir?
Bileşikler kimyasal formüllerle gösterilir. Kimyasal formül, bileşiğin hangi elementlerden oluştuğunu ve bu elementlerin hangi oranlarda birleştiğini gösterir.
| Bileşik | Formül | İçerdiği Elementler |
|---|---|---|
| Su | H2O | Hidrojen ve oksijen |
| Sofra tuzu | NaCl | Sodyum ve klor |
| Karbondioksit | CO2 | Karbon ve oksijen |
| Amonyak | NH3 | Azot ve hidrojen |
| Kalsiyum karbonat | CaCO3 | Kalsiyum, karbon ve oksijen |
Sık Karşılaşılan Bileşik Örnekleri
| Formül | Sistematik / Kimyasal Adı | Yaygın Adı |
|---|---|---|
| H2O | Su | Su |
| NaCl | Sodyum klorür | Sofra tuzu |
| HCl | Hidrojen klorür | Tuz ruhu |
| H2SO4 | Sülfürik asit | Zaç yağı |
| HNO3 | Nitrik asit | Kezzap |
| CaCO3 | Kalsiyum karbonat | Kireç taşı |
Bileşikler Nasıl Ayrıştırılır?
Bileşikler fiziksel yöntemlerle bileşenlerine ayrılamaz. Süzme, eleme, damıtma veya mıknatısla ayırma gibi yöntemler karışımlar için kullanılır.
Bir bileşiği oluşturan elementlere ayırmak için kimyasal yöntemler gerekir. Örneğin su, elektroliz yöntemiyle hidrojen ve oksijen gazlarına ayrılabilir.
Örnek: Su bileşiği fiziksel yöntemlerle hidrojen ve oksijene ayrılamaz. Bunun için elektroliz gibi kimyasal bir yöntem gerekir.
Bileşik ve Karışım Arasındaki Fark
Bileşikler ve karışımlar sıkça karıştırılır. Bileşiklerde elementler kimyasal bağlarla ve belirli oranlarda birleşir. Karışımlarda ise maddeler kimyasal bağ oluşturmadan fiziksel olarak bir araya gelir.
| Özellik | Bileşik | Karışım |
|---|---|---|
| Oluşum şekli | Kimyasal tepkime ile oluşur. | Fiziksel yollarla oluşur. |
| Bileşenlerin özelliği | Bileşenler kendi özelliklerini kaybeder. | Bileşenler kendi özelliklerini korur. |
| Oran | Belirli ve sabit oran vardır. | İstenilen oranda hazırlanabilir. |
| Ayrıştırma | Kimyasal yollarla ayrıştırılır. | Fiziksel yollarla ayrıştırılır. |
| Gösterim | Formülle gösterilir. | Formülü yoktur. |
| Örnek | Su, tuz, karbondioksit | Tuzlu su, hava, toprak |
Karışımlar hakkında daha fazla bilgi için Homojen ve Heterojen Karışımlar Nedir? yazısını inceleyebilirsin.
Element ve Bileşik Arasındaki Fark
Elementler ve bileşikler saf madde olmaları bakımından benzerlik gösterir; ancak yapıları farklıdır. Elementler tek tür atom içerirken, bileşikler en az iki farklı element içerir.
| Özellik | Element | Bileşik |
|---|---|---|
| Yapısı | Tek tür atom içerir. | En az iki farklı element içerir. |
| Gösterim | Sembollerle gösterilir. | Formüllerle gösterilir. |
| Ayrıştırılma | Daha basit maddelere ayrıştırılamaz. | Kimyasal yollarla ayrıştırılabilir. |
| Örnek | Fe, O2, Au | H2O, NaCl, CO2 |
Element konusunu tekrar etmek için Element Nedir? yazısına geçebilirsin.
Sık Yapılan Hatalar
1. Her saf maddeyi bileşik sanmak
Saf maddeler element ve bileşik olarak ikiye ayrılır. Elementler de saf maddedir; ancak bileşik değildir.
2. O2 gibi moleküler elementleri bileşik sanmak
O2 iki atom içerir; fakat bu atomlar aynı tür oksijen atomlarıdır. Farklı element içermediği için bileşik değildir.
3. Bileşiklerin fiziksel yollarla ayrılabileceğini düşünmek
Bileşikler fiziksel yöntemlerle elementlerine ayrılmaz. Bunun için kimyasal yöntemler gerekir.
4. Bileşik ile karışımı aynı sanmak
Bileşikler belirli oranlarda kimyasal bağlarla oluşur. Karışımlar ise fiziksel yollarla oluşur ve istenilen oranlarda hazırlanabilir.
Bileşik Konusu Özeti
- Bileşik, en az iki farklı elementin belirli oranlarda birleşmesiyle oluşan saf maddedir.
- Bileşikler formüllerle gösterilir.
- Bileşikler fiziksel yollarla bileşenlerine ayrılamaz.
- Bileşikler kimyasal yollarla ayrıştırılabilir.
- Bileşikleri oluşturan elementler kendi özelliklerini kaybeder.
- Su, sofra tuzu, karbondioksit ve kalsiyum karbonat bileşiklere örnektir.
- Bileşikler sabit oranlarda oluşur.
- Bileşikler karışımlardan farklıdır; çünkü karışımlar fiziksel yollarla oluşur.
Bileşik Nedir? Mini Test
1. Bileşik nedir?
- A) Tek tür atomdan oluşan saf madde
- B) En az iki farklı elementin belirli oranlarda birleşmesiyle oluşan saf madde
- C) İstenilen oranda karıştırılmış maddeler topluluğu
- D) Fiziksel yollarla ayrılan karışım
Doğru cevap: B
Açıklama: Bileşik, farklı elementlerin belirli oranlarda kimyasal bağlarla birleşmesiyle oluşur.
2. Aşağıdakilerden hangisi bileşiktir?
- A) Demir
- B) Oksijen gazı
- C) Su
- D) Altın
Doğru cevap: C
Açıklama: Su, hidrojen ve oksijen elementlerinden oluşan H2O formüllü bir bileşiktir.
3. Bileşikler nasıl gösterilir?
- A) Formüllerle
- B) Sadece sembollerle
- C) Haritalarla
- D) Renklerle
Doğru cevap: A
Açıklama: Bileşikler H2O, NaCl, CO2 gibi formüllerle gösterilir.
4. Bileşikler hangi yöntemlerle bileşenlerine ayrılabilir?
- A) Fiziksel yöntemlerle
- B) Kimyasal yöntemlerle
- C) Eleme yöntemiyle
- D) Mıknatısla
Doğru cevap: B
Açıklama: Bileşikler ancak kimyasal yöntemlerle bileşenlerine ayrılabilir.
5. Aşağıdakilerden hangisi bileşikler için yanlıştır?
- A) Saf maddedirler.
- B) Formüllerle gösterilirler.
- C) Fiziksel yollarla bileşenlerine ayrılırlar.
- D) En az iki farklı element içerirler.
Doğru cevap: C
Açıklama: Bileşikler fiziksel yollarla değil, kimyasal yollarla bileşenlerine ayrılır.
Sıkça Sorulan Sorular
Bileşik nedir?
Bileşik, en az iki farklı elementin belirli oranlarda kimyasal bağlarla birleşmesiyle oluşan saf maddedir.
Bileşikler saf madde midir?
Evet. Bileşikler belirli formüllere ve sabit bileşime sahip oldukları için saf maddedir.
Bileşikler fiziksel yöntemlerle ayrıştırılır mı?
Hayır. Bileşikler fiziksel yöntemlerle bileşenlerine ayrıştırılamaz. Kimyasal yöntemler gerekir.
Oksijen gazı bileşik midir?
Hayır. Oksijen gazı O2 şeklinde bulunur; ancak yalnızca oksijen atomlarından oluştuğu için moleküler yapılı elementtir.
Su bileşik midir?
Evet. Su, hidrojen ve oksijen elementlerinden oluşan H2O formüllü bir bileşiktir.
Bileşik ile karışım arasındaki fark nedir?
Bileşikler belirli oranlarda kimyasal bağlarla oluşur ve kimyasal yollarla ayrılır. Karışımlar ise fiziksel yollarla oluşur ve fiziksel yöntemlerle ayrılabilir.
Bu Konudan Sonra Ne Öğrenmeliyim?
Bileşik konusunu öğrendikten sonra şu konulara geçebilirsin:
- Element ve Bileşik Arasındaki Farklar
- Karışım Nedir?
- Homojen ve Heterojen Karışımlar Nedir?
- Kimyasal Bağ Nedir?
- Kimyasal Tepkime Nedir?
Bu yazı Elementler, Bileşikler ve Karışımlar Konu Rehberi‘nin bir parçasıdır.
