Allotrop atom, aynı elementin farklı yapısal formlarını ifade eder. Bu formlar, atomların farklı bağlanma şekilleri ve düzenleriyle ortaya çıkar, böylece elementin fiziksel ve kimyasal özelliklerinde değişiklikler olur.
Aynı elementin atomlarının farklı sayı ve dizilişlerle bir araya gelerek oluşturduğu farklı formlara allotrop denir. Kimyasal bağların bağlanma şekli ve atomların uzaydaki geometrik düzeni değiştikçe, maddenin fiziksel ve kimyasal davranışları da kökten değişir. Bu içerikte, allotropların neden farklı özelliklere sahip olduğunu, kovalent ağ örgüsü gibi teknik detayları ve sınavlar için kritik olan karşılaştırmaları inceleyeceğiz.
Hızlı Özet: Allotrop Kavramına Bakış
- Tanım: Aynı tür atomların farklı geometrik dizilişlere sahip olmasıdır.
- En Bilinen Örnekler: Elmas-grafit (Karbon), Oksijen-Ozon (Oksijen).
- Aynı Olanlar: Proton sayıları, çekirdek yapıları, aynı maddeyle tepkimeye girdiklerinde oluşturdukları ürünler.
- Farklı Olanlar: Fiziksel özellikler (sertlik, iletkenlik), kimyasal aktivite, bağ yapıları ve kristal sistemleri.
Allotrop Atom Ne Demektir?
Kimyasal anlamda allotrop nedir sorusunun cevabı; aynı hammadde kullanılmasına rağmen atomların bağ yapılarının farklı olmasıdır. Bir elementin atomları birbirine farklı açılarla ve farklı kuvvetlerle bağlandığında, ortaya çıkan maddelerin kimliği de farklılaşır.
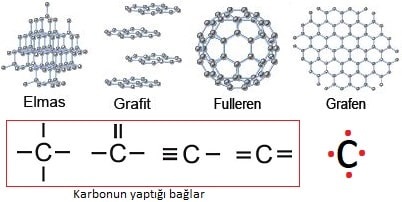
Örneğin, atomun yapısı ve özellikleri temel alındığında, bir karbon atomu her zaman 6 protona sahiptir. Ancak bu karbon atomları birbirine kovalent ağ örgüsü ile çok sıkı ve piramit şeklinde bağlanırsa “elmas”, altıgen tabakalar halinde zayıf Van der Waals kuvvetleri ile bağlanırsa “grafit” oluşur.
Allotropların Temel Özellikleri
Allotrop atomların bazı özellikleri tamamen aynıyken, bazıları onları birbirinden ayıran temel farkları oluşturur. Özellikle bağ enerjileri ve molekül geometrisi bu farkların temel sebebidir.
Hangi Özellikleri Aynıdır?
- Çekirdek Yapısı: Proton ve nötron sayıları değişmez.
- Sembolleri: Her iki allotrop da aynı element sembolü ile gösterilir (Örn: Elmas ve grafit için “C”).
- Tepkime Ürünleri: Örneğin, hem elmas hem de grafit yeterli oksijenle yakıldığında sadece Karbondioksit (CO2) gazı açığa çıkar.
Hangi Özellikleri Farklıdır?
- Fiziksel Özellikler: Özkütle, erime noktası, sertlik, renk ve elektrik iletkenliği gibi özellikler tamamen farklıdır.
- Bağ Yapıları ve Geometri: Atomlar arasındaki bağların açısı, uzunluğu ve dizilim şekli (kristal örgü) farklıdır.
- Kimyasal Aktivite: Tepkimeye girme istekleri farklıdır. Genellikle yapısı daha kararsız olan allotrop (örneğin ozon), daha aktiftir ve daha kolay tepkimeye girer.
En Yaygın Allotrop Örnekleri
Doğada pek çok elementin allotropu bulunur ancak kimya müfredatında özellikle karbon, oksijen, fosfor ve kükürt üzerinde durulur.
Karbonun Allotropları: Elmas, Grafit ve Fullerene
Karbon, kimyasal bağlar konusundaki farklılıkların en somut görüldüğü elementtir:
- Elmas: Her karbon atomu diğer 4 karbon atomuna güçlü kovalent bağlarla bağlıdır. Bu kovalent ağ örgüsü elması bilinen en sert doğal maddelerden biri yapar. Elektriği iletmez.
- Grafit: Karbon atomları altıgen tabakalar oluşturur. Bu tabakalar arasında zayıf etkileşimler bulunduğu için yumuşaktır ve elektriği iletir.
- Fullerene ve Grafen: Karbonun yapay allotroplarıdır. Nanoteknolojide ve batarya teknolojilerinde devrim yaratan süper iletken özelliklere sahiptirler.
Oksijenin Allotropları: Oksijen Gazı (O2) ve Ozon (O3)
Oksijen elementi doğada iki farklı moleküler yapıda bulunur:
- Oksijen (O2): Soluduğumuz, renksiz ve kokusuz gazdır.
- Ozon (O3): Keskin kokulu, atmosferin üst katmanlarında UV ışınlarını süzen, O2’ye göre çok daha aktif ve yükseltgen bir gazdır.
Fosfor ve Kükürt Allotropları
Fosforun en bilinen formları beyaz fosfor ve kırmızı fosfordur. Beyaz fosfor çok aktif ve zehirliyken, kırmızı fosfor daha kararlı bir yapıdadır. Kükürt ise rombik ve monoklinik kükürt olarak kristal şekillerine göre ayrılır.
Karşılaştırma Tablosu: Allotroplar Arasındaki Farklar
| Özellik | Durum |
|---|---|
| Atom Numarası ve Çekirdek Yapısı | Aynı |
| Fiziksel Özellikler (Sertlik, Erime Noktası vb.) | Farklı |
| Kristal / Geometrik Yapı (Bağ Dizilimi) | Farklı |
| Kimyasal Aktiflik (Tepkimeye Girme Hızı) | Farklı |
| Aynı Maddeyle Tepkime Sonucu Oluşan Ürün | Aynı |
Sıkça Sorulan Sorular (SSS)
1. Allotropların kimyasal özellikleri tamamen aynı mıdır?
Hayır. Aynı elementle tepkimeye girdiklerinde aynı ürünü oluştururlar ancak bağ enerjileri farklı olduğu için tepkimeye girme hızları ve aktiflikleri farklıdır.2. Elmas ve grafit neden bu kadar farklıdır?
Temel sebep atomik dizilimdir. Elmasta atomlar 3 boyutlu kovalent ağ örgüsüyle birbirine kenetlenmişken, grafitte tabakalar arası bağlar zayıftır.3. İzotop ve Allotrop arasındaki fark nedir?
İzotop, çekirdekteki nötron sayısının farklı olmasıdır (atom düzeyinde fark). Allotrop ise atomların dış yapıdaki dizilişlerinin farklı olmasıdır (molekül/madde düzeyinde fark).
Sonuç
Allotropi, doğanın aynı malzemeyi kullanarak nasıl farklı işlevler yaratabileceğinin en net kanıtıdır. Karbon atomu aynı kalsa da, dizilişindeki değişim onu dünyanın en sert maddesine (elmas) ya da en yumuşak yazı gerecine (grafit) dönüştürebilir. Bu kavramı anlamak, periyodik sistem ve elementler arasındaki ilişkileri kavramak için kritiktir.
Kimya konularında daha derinlemesine bilgi edinmek için maddenin fiziksel ve kimyasal değişimleri rehberimizi inceleyebilirsiniz.
Kaynak: MEB Kimya Müfredatı ve IUPAC Gold Book standartları esas alınmıştır.
