Atomlar doğada çoğu zaman tek başlarına kararlı halde bulunmaz. Daha düşük enerjili ve kararlı bir yapıya ulaşmak için başka atomlarla etkileşime girerler. Bu etkileşimler sonucunda atomlar arasında kimyasal bağlar oluşur.
Kimyasal bağlar, maddelerin özelliklerini belirleyen en önemli etkenlerden biridir. Örneğin sofra tuzunun kristal yapısı, suyun moleküler yapısı ve metallerin elektrik iletkenliği kimyasal bağlarla ilişkilidir.
Önemli bilgi: Kimyasal bağ oluşurken atomlar daha kararlı ve daha düşük enerjili hale gelir. Bağ koparmak için ise enerji gerekir.
Kimyasal Bağ Nedir?
Kimyasal bağ, atomları veya iyonları bir arada tutan güçlü etkileşimdir. Atomlar, kararlı elektron düzenine ulaşmak için elektron alışverişi yapabilir veya elektronlarını ortaklaşa kullanabilir.
Kimyasal bağlar genellikle atomların en dış katmanındaki elektronlarla ilgilidir. Bu elektronlara değerlik elektronları denir.
Bu konuyu daha iyi anlamak için önce Atom Nedir?, Atom Numarası ve Kütle Numarası Nedir? ve Periyodik Tablo Nedir? konularını bilmek faydalı olur.
Atomlar Neden Kimyasal Bağ Yapar?
Atomlar genellikle daha kararlı hale gelmek için kimyasal bağ yapar. Kararlı hale gelme eğilimi çoğu zaman atomların son katmanlarını doldurma isteğiyle açıklanır.
Birçok atom, elektron dizilimini soygazlara benzetmeye çalışır. Bu durum bazı kaynaklarda oktet kuralı veya dublet kuralı ile açıklanır.
- Oktet kuralı: Atomların son katmanlarında 8 elektron bulundurma eğilimidir.
- Dublet kuralı: Bazı küçük atomların son katmanlarında 2 elektronla kararlı hale gelmesidir.
Kimyasal Bağ Oluşurken Enerji Ne Olur?
Kimyasal bağ oluşurken sistem genellikle daha düşük enerjili ve daha kararlı hale gelir. Bu nedenle bağ oluşumu çoğu zaman enerji açığa çıkaran bir olaydır.
Bir kimyasal bağı koparmak için ise dışarıdan enerji verilmesi gerekir. Bu enerjiye bağ enerjisi denir.
| Olay | Enerji Durumu | Açıklama |
|---|---|---|
| Bağ oluşumu | Enerji açığa çıkarabilir. | Atomlar daha kararlı hale gelir. |
| Bağ kopması | Enerji gerekir. | Atomları ayırmak için dışarıdan enerji verilmelidir. |
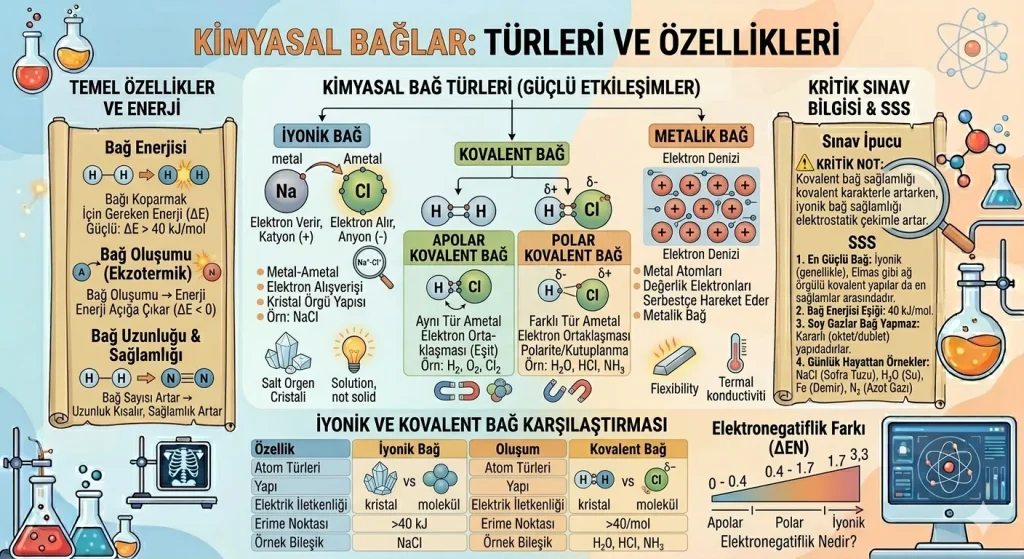
Kimyasal Bağ Türleri Nelerdir?
Kimyasal bağlar atomların türüne ve elektronların kullanım biçimine göre üç ana gruba ayrılır:
- İyonik bağ
- Kovalent bağ
- Metalik bağ
1. İyonik Bağ
İyonik bağ, genellikle bir metal atomu ile bir ametal atomu arasında elektron alışverişi sonucunda oluşan bağdır.
Metal atomu elektron vererek pozitif yüklü iyon yani katyon olur. Ametal atomu ise elektron alarak negatif yüklü iyon yani anyon olur. Zıt yüklü iyonlar arasındaki güçlü çekim kuvveti iyonik bağı oluşturur.
Örnek: Sodyum klorür yani sofra tuzu (NaCl), sodyum iyonu Na+ ve klor iyonu Cl– arasındaki iyonik bağla oluşur.
İyonik Bağların Özellikleri
- Genellikle metal ve ametal atomları arasında oluşur.
- Elektron alışverişi vardır.
- Zıt yüklü iyonlar arasında elektrostatik çekim bulunur.
- İyonik bileşikler kristal örgü yapısına sahiptir.
- Erime ve kaynama noktaları genellikle yüksektir.
- Katı halde elektriği iletmezler.
- Sıvı halde veya sulu çözeltilerinde elektriği iletebilirler.
2. Kovalent Bağ
Kovalent bağ, ametal atomları arasında elektronların ortaklaşa kullanılmasıyla oluşan bağ türüdür.
Kovalent bağlarda atomlar elektron alıp vermek yerine elektronlarını paylaşır. Bu sayede daha kararlı hale gelirler.
Örnek: Su molekülünde hidrojen ve oksijen atomları arasında kovalent bağ bulunur.
Apolar Kovalent Bağ
Aynı tür ametal atomları arasında elektronların eşit paylaşılmasıyla oluşan bağa apolar kovalent bağ denir.
- H2
- O2
- N2
- Cl2
Polar Kovalent Bağ
Farklı tür ametal atomları arasında elektronların eşit olmayan şekilde paylaşılmasıyla oluşan bağa polar kovalent bağ denir.
- H2O
- HCl
- NH3
- CO2 içindeki C-O bağları
Elektronların daha elektronegatif olan atoma daha yakın bulunması, bağda kutuplaşmaya neden olur.
3. Metalik Bağ
Metalik bağ, metal atomlarını bir arada tutan bağ türüdür. Metallerde değerlik elektronları atomlar arasında serbestçe hareket edebilir. Bu durum genellikle elektron denizi modeli ile açıklanır.
Pozitif yüklü metal iyonları ile serbest hareket eden elektronlar arasındaki çekim, metalik bağı oluşturur.
Metalik Bağın Metallere Kazandırdığı Özellikler
- Isı ve elektriği iyi iletme
- Tel ve levha haline getirilebilme
- Parlak yüzey görünümü
- Dayanıklılık
İyonik, Kovalent ve Metalik Bağ Karşılaştırması
| Özellik | İyonik Bağ | Kovalent Bağ | Metalik Bağ |
|---|---|---|---|
| Oluşum | Elektron alışverişi | Elektron ortaklaşması | Elektron denizi modeli |
| Atom türü | Genellikle metal + ametal | Ametal + ametal | Metal atomları |
| Yapı | İyonik kristal örgü | Molekül veya ağ örgü yapı | Metal kristali |
| Elektrik iletkenliği | Katı halde iletmez; sıvı ve sulu çözeltide iletebilir. | Genellikle iletmez. | Katı ve sıvı halde iletebilir. |
| Örnek | NaCl, MgO | H2O, HCl, O2 | Fe, Cu, Al |
İyonik ve Kovalent Bağ Arasındaki Fark
| Özellik | İyonik Bağ | Kovalent Bağ |
|---|---|---|
| Elektron kullanımı | Elektron alışverişi vardır. | Elektron ortaklaşması vardır. |
| Atom türleri | Genellikle metal ve ametal arasında oluşur. | Ametaller arasında oluşur. |
| Yapı birimi | İyonik kristal yapı | Molekül veya ağ yapılı olabilir. |
| Örnek | NaCl | H2O |
Kimyasal Bağ ve Zayıf Etkileşim Farkı
Kimyasal bağlar atomları veya iyonları bir arada tutan güçlü etkileşimlerdir. Zayıf etkileşimler ise moleküller arasında görülen daha zayıf çekim kuvvetleridir.
| Özellik | Kimyasal Bağ | Zayıf Etkileşim |
|---|---|---|
| Etkileşim türü | Atomlar veya iyonlar arasında | Moleküller arasında |
| Güç | Genellikle güçlüdür. | Genellikle daha zayıftır. |
| Örnek | İyonik, kovalent, metalik bağ | Hidrojen bağı, dipol-dipol, London kuvvetleri |
| Etkilediği özellikler | Maddenin kimyasal yapısını belirler. | Kaynama noktası, erime noktası gibi fiziksel özellikleri etkiler. |
Günlük Hayattan Kimyasal Bağ Örnekleri
| Madde | Bağ Türü | Açıklama |
|---|---|---|
| Sofra tuzu (NaCl) | İyonik bağ | Sodyum ve klor iyonları arasındaki çekimle oluşur. |
| Su (H2O) | Polar kovalent bağ | Hidrojen ve oksijen elektronlarını ortaklaşa kullanır. |
| Demir (Fe) | Metalik bağ | Metal atomları elektron deniziyle bir arada tutulur. |
| Azot gazı (N2) | Apolar kovalent bağ | İki azot atomu elektronlarını ortaklaşa kullanır. |
Sık Yapılan Hatalar
1. İyonik bağı molekül sanmak
İyonik bileşikler genellikle molekül yapılı değil, kristal örgü yapılıdır. NaCl bir molekül değil, iyonik kristal yapı olarak düşünülmelidir.
2. Kovalent bağı sadece aynı atomlar arasında sanmak
Kovalent bağ hem aynı tür ametaller arasında hem de farklı tür ametaller arasında oluşabilir.
3. Metalik bağı iyonik bağla karıştırmak
Metalik bağ, metal atomları ve serbest elektronlar arasındaki çekimle açıklanır. İyonik bağ ise zıt yüklü iyonlar arasındaki çekimdir.
4. Zayıf etkileşimleri kimyasal bağlarla aynı sanmak
Kimyasal bağlar atomlar veya iyonlar arasındaki güçlü etkileşimlerdir. Zayıf etkileşimler ise moleküller arasında görülür.
Kimyasal Bağ Konusu Özeti
- Kimyasal bağ, atomları veya iyonları bir arada tutan güçlü çekim kuvvetidir.
- Atomlar daha kararlı hale gelmek için bağ yapar.
- İyonik bağ elektron alışverişiyle oluşur.
- Kovalent bağ elektron ortaklaşmasıyla oluşur.
- Metalik bağ metal atomları arasında görülür.
- İyonik bağ genellikle metal-ametal arasında oluşur.
- Kovalent bağ genellikle ametal-ametal arasında oluşur.
- Kimyasal bağlar güçlü etkileşimlerdir.
Kimyasal Bağ Nedir? Mini Test
1. Kimyasal bağ nedir?
- A) Atomları veya iyonları bir arada tutan güçlü etkileşim
- B) Sadece karışımları ayırma yöntemi
- C) Maddenin sıcaklığı
- D) Sadece fiziksel görünüm değişimi
Doğru cevap: A
Açıklama: Kimyasal bağ, atomları veya iyonları bir arada tutan güçlü çekim kuvvetidir.
2. İyonik bağ genellikle hangi atomlar arasında oluşur?
- A) Metal – ametal
- B) Ametal – ametal
- C) Metal – metal
- D) Soygaz – soygaz
Doğru cevap: A
Açıklama: İyonik bağ genellikle metal ve ametal atomları arasında oluşur.
3. Kovalent bağ nasıl oluşur?
- A) Elektron alışverişiyle
- B) Elektron ortaklaşmasıyla
- C) Süzme yöntemiyle
- D) Tanecik boyutu farkıyla
Doğru cevap: B
Açıklama: Kovalent bağ, atomların elektronlarını ortaklaşa kullanmasıyla oluşur.
4. Metalik bağ hangi maddelerde görülür?
- A) Metallerde
- B) Sadece gazlarda
- C) Sadece tuzlu suda
- D) Sadece şekerli suda
Doğru cevap: A
Açıklama: Metalik bağ metal atomları arasında görülür.
5. NaCl bileşiğinde hangi bağ türü baskındır?
- A) Metalik bağ
- B) İyonik bağ
- C) Apolar kovalent bağ
- D) Zayıf etkileşim
Doğru cevap: B
Açıklama: NaCl, sodyum ve klor iyonları arasındaki iyonik çekimle oluşur.
Sıkça Sorulan Sorular
Kimyasal bağ nedir?
Kimyasal bağ, atomları veya iyonları bir arada tutan güçlü çekim kuvvetidir.
Kimyasal bağ türleri nelerdir?
Başlıca kimyasal bağ türleri iyonik bağ, kovalent bağ ve metalik bağdır.
İyonik bağ nasıl oluşur?
İyonik bağ, genellikle metal ve ametal atomları arasında elektron alışverişiyle oluşur.
Kovalent bağ nasıl oluşur?
Kovalent bağ, ametal atomlarının elektronlarını ortaklaşa kullanmasıyla oluşur.
Metalik bağ nedir?
Metalik bağ, metal atomlarını serbest elektronların oluşturduğu elektron deniziyle bir arada tutan bağdır.
Bağ oluşurken enerji açığa çıkar mı?
Genellikle evet. Bağ oluşurken sistem daha kararlı hale gelir ve enerji açığa çıkabilir. Bağ koparmak için ise enerji gerekir.
Bu Konudan Sonra Ne Öğrenmeliyim?
Kimyasal bağ konusunu öğrendikten sonra şu konulara geçebilirsin:
Bu konu şu rehberin parçasıdır: Atom ve Periyodik Sistem – Ogreniyo.com
