Maddenin katı, sıvı ve gaz halleri (ve yüksek enerjili plazma hali) arasındaki fiziksel geçişlerine hal değişimi denir. Doğadaki tüm maddeler dışarıdan ısı alarak veya dışarıya ısı vererek bir halden diğerine geçebilir. Bu süreçte maddenin kimyasal yapısı değişmez; sadece tanecikler arası boşluk, çekim kuvveti ve hareketlilik farklılaşır.
Hal Değişimi Nedir? (Özet)
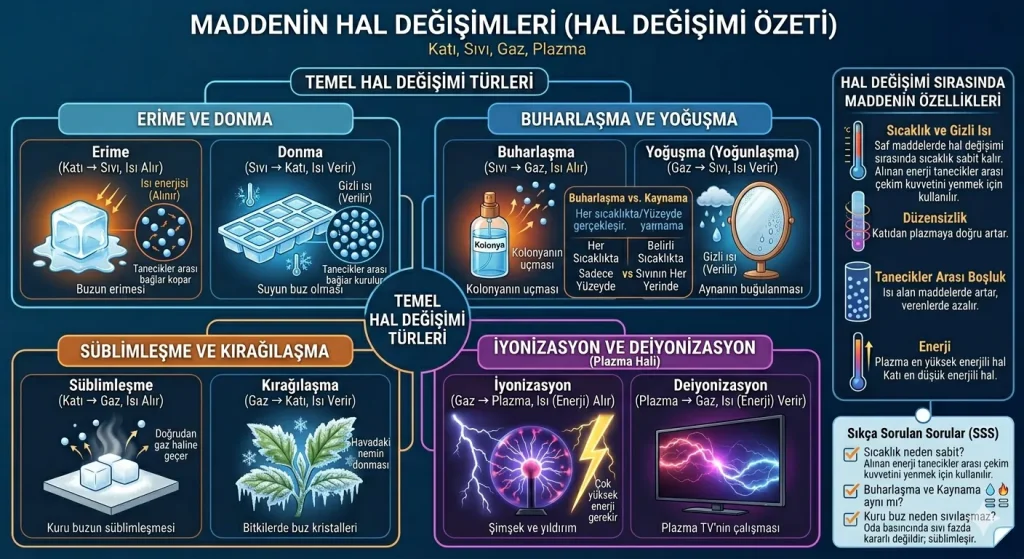
Hal değişimi, maddenin termal enerji (ısı) etkisiyle fiziksel formunun değişmesidir. Maddenin moleküler yapısı aynı kalırken, taneciklerin dizilimi ve enerjisi değişir. Temelde 8 ana hal değişimi türü bulunur:
- Isı Alan (Endotermik) Olaylar: Erime, buharlaşma, süblimleşme, iyonizasyon.
- Isı Veren (Ekzotermik) Olaylar: Donma, yoğuşma, kırağılaşma, deiyonizasyon.
Konunun temelini kavramak için öncelikle maddenin halleri nelerdir içeriğimize göz atabilirsiniz.
Temel Hal Değişimi Türleri
Maddenin hal değişimlerini, birbirinin zıttı olan süreçler şeklinde gruplandırmak öğrenmeyi kolaylaştırır.
Erime ve Donma
Erime: Katı haldeki bir maddenin ısı alarak sıvı hale geçmesidir. Buzun eriyerek suya dönüşmesi en temel örnektir. Bu süreçte madde dışarıdan enerji aldığı için tanecikler arası çekim kuvveti zayıflar.
Donma: Sıvı haldeki bir maddenin ısı vererek katı hale geçmesidir. Suyun buzluğa konulduğunda buz haline gelmesi bir donma olayıdır. Donma, erimenin tam tersidir.
Buharlaşma ve Yoğuşma
Buharlaşma: Sıvı bir maddenin ısı alarak gaz haline geçmesidir. Buharlaşma her sıcaklıkta gerçekleşir.
Kritik Not: Buharlaşma ve Kaynama Farkı
Buharlaşma sadece sıvının yüzeyinde ve her sıcaklıkta olurken; kaynama sıvının her yerinde, belirli bir sıcaklıkta ve hızlı bir şekilde gerçekleşir.
Yoğuşma (Yoğunlaşma): Gaz halindeki bir maddenin ısı vererek sıvı hale geçmesidir. Soğuk bir yüzeye çarpan su buharının su damlacıklarına dönüşmesi (örneğin banyodaki aynanın buğulanması) yoğuşmadır.
Süblimleşme ve Kırağılaşma
Süblimleşme: Katı bir maddenin sıvı aşamasını atlayarak doğrudan gaz haline geçmesidir. Naftalin ve kuru buz (katı karbondioksit) oda sıcaklığında süblimleşir.
Kırağılaşma: Gaz halindeki bir maddenin sıvılaşmadan doğrudan katı hale geçmesidir. Kışın sabah saatlerinde havadaki nemin aniden soğuyarak bitkiler üzerinde buz kristalleri oluşturmasıdır.
İyonizasyon ve Deiyonizasyon (Plazma Hali)
İyonizasyon: Gaz halindeki bir maddeye çok yüksek enerji verildiğinde, atomlardan elektron koparak maddenin plazma haline geçmesidir. Şimşek ve yıldırım oluşumu buna örnektir.
Deiyonizasyon: Plazma halindeki bir maddenin dışarıya enerji vererek tekrar gaz haline dönmesidir.
Hal Değişimi Tablosu: Isı ve Dönüşüm Özeti
Aşağıdaki tablo, maddenin geçiş süreçlerini ve enerji durumlarını özetlemektedir:
| Hal Değişimi | Dönüşüm Yönü | Isı Durumu | Örnek |
|---|---|---|---|
| Erime | Katı → Sıvı | Isı Alır | Buzun erimesi |
| Donma | Sıvı → Katı | Isı Verir | Suyun buz olması |
| Buharlaşma | Sıvı → Gaz | Isı Alır | Kolonyanın uçması |
| Yoğuşma | Gaz → Sıvı | Isı Verir | Yağmur oluşumu |
| Süblimleşme | Katı → Gaz | Isı Alır | Naftalinin koku yayması |
| Kırağılaşma | Gaz → Katı | Isı Verir | Bitkilerde beyaz buz tabakası |
| İyonizasyon | Gaz → Plazma | Isı (Enerji) Alır | Yıldırım oluşumu |
| Deiyonizasyon | Plazma → Gaz | Isı (Enerji) Verir | Plazma TV’lerin çalışma prensibi |
Hal Değişimi Sırasında Maddenin Özellikleri
Bir madde hal değiştirirken tanecik yapısında ve enerji seviyesinde önemli değişimler yaşanır:
- Sıcaklık ve Gizli Isı: Saf maddeler hal değiştirirken sıcaklıkları sabit kalır. Bu süreçte alınan veya verilen ısıya Hal Değişim Isısı (Gizli Isı) denir. Bu enerji, sıcaklığı artırmak yerine tanecikler arası bağları koparmak veya kurmak için kullanılır.
- Düzensizlik: Katıdan plazmaya doğru gidildikçe maddenin düzensizliği artar.
- Tanecikler Arası Boşluk: Isı alan maddelerde tanecikler birbirinden uzaklaşır (hacim genellikle artar), ısı verenlerde ise birbirine yaklaşır.
- Enerji: Plazma hali maddenin en yüksek enerjili hali, katı hali ise en düşük enerjili halidir.
Bu süreçlerin termodinamik temellerini anlamak için isi ve sicaklik arasindaki farklar yazımızı inceleyebilirsiniz.
Sıkça Sorulan Sorular (SSS)
Hal değişimi sırasında sıcaklık neden sabit kalır?
Saf maddelerde hal değişimi sırasında alınan enerji, maddenin sıcaklığını artırmak için değil, tanecikler arasındaki çekim kuvvetini yenerek fiziksel hali değiştirmek (Gizli Isı) için harcanır.
Buharlaşma ve kaynama aynı şey mi?
Hayır. Buharlaşma her sıcaklıkta ve sadece yüzeyde olurken; kaynama belirli bir sıcaklıkta (kaynama noktası) ve sıvının tamamında gerçekleşir.
Kuru buz neden sıvılaşmaz?
Kuru buz (katı karbondioksit), standart atmosfer basıncında sıvı halde bulunamaz. Bu nedenle ısı aldığında doğrudan gaz haline geçer, yani süblimleşir.
Plazma haline geçiş için ne gereklidir?
Gaz halindeki bir maddenin plazmaya dönüşmesi (iyonizasyon) için çok yüksek sıcaklık veya güçlü bir elektrik alanı gibi yoğun bir enerji girişi gereklidir.
Sonuç
Hal değişimleri, doğadaki enerji döngüsünün temelini oluşturur. Maddenin katı, sıvı, gaz ve plazma halleri arasındaki bu geçişler, maddenin kimliğini değiştirmeden sadece fiziksel yapısını ve enerjisini yeniden düzenler. Özellikle gizli ısı kavramını ve buharlaşma-kaynama farkını bilmek, fen bilimleri derslerinde ve günlük hayattaki fiziksel olayları anlamlandırmada size büyük avantaj sağlar.
Konuyla ilgili daha derinlemesine bilgi için fiziksel değişimler ve kimyasal degisimler arasındaki temel farkları da öğrenmenizi öneririz.
