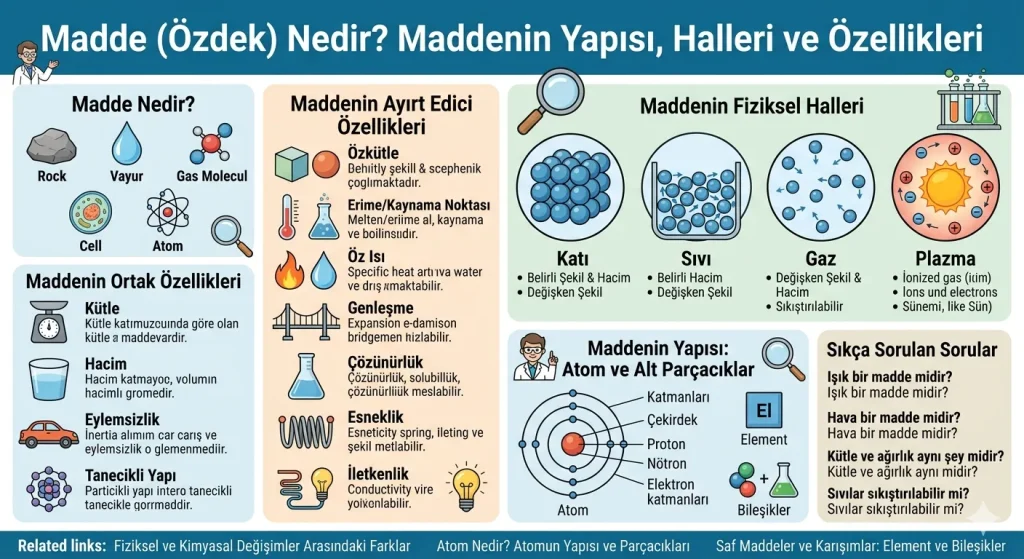
Kütlesi, hacmi, eylemsizliği olan ve tanecikli yapıdan oluşan her şeye madde veya diğer adıyla özdek denir. Çevremizde gördüğümüz taş, su ve hava gibi varlıkların yanı sıra gözle göremediğimiz hücreler ve atomlar da birer maddedir. Bir varlığın madde sayılabilmesi için mutlaka uzayda bir yer kaplaması ve bir kütleye sahip olması gerekir. Bu bağlamda ışık, ısı veya ses gibi olgular kütleleri ve hacimleri olmadığı için madde değil, birer enerji formudur.
Öne Çıkan Bilgi: Maddenin var olabilmesi için dört temel ortak özelliği (kütle, hacim, eylemsizlik, tanecikli yapı) aynı anda taşıması şarttır. Bu özelliklerden biri bile eksikse o varlık bilimsel olarak madde kabul edilmez.
Maddenin Ortak Özellikleri
Doğadaki tüm maddelerde, miktarı ne olursa olsun bulunan özelliklere “ortak özellikler” denir. Bu özellikler maddeyi tanımlamamıza yardımcı olur ancak maddeleri birbirinden ayırt etmek için yeterli değildir.
1. Kütle ve Hacim
- Kütle: Bir cismin sahip olduğu değişmeyen madde miktarıdır. “m” harfi ile gösterilir ve birimi genellikle kilogram (kg) veya gramdır (g).
- Hacim: Maddenin uzayda (boşlukta) kapladığı yerdir. “V” harfi ile gösterilir. Katı ve sıvıların hacmi belirli iken, gazların hacmi bulundukları kaba göre değişir.
2. Eylemsizlik ve Tanecikli Yapı
- Eylemsizlik: Maddenin sahip olduğu hareket durumunu koruma isteğidir. Duran bir cismin durmaya devam etmek istemesi veya hareket halindeki bir cismin dış bir kuvvet etki etmedikçe hareketini sürdürme eğilimidir.
- Tanecikli Yapı: Tüm maddeler atom veya molekül adı verilen küçük birimlerden oluşur. Maddenin bütünsel görünümünün altında aslında büyük boşluklar ve sürekli hareket eden tanecikler yer alır.
Maddenin Ayırt Edici Özellikleri
Bir maddeyi diğerinden ayırmamızı sağlayan, madde miktarına bağlı olmayan özelliklerdir. Her maddenin kendine has değerleri vardır. Önemli ayırt edici özellikler şunlardır:
- Özkütle (Yoğunluk): Birim hacimdeki kütle miktarıdır.
- Erime ve Kaynama Noktası: Saf maddelerin hal değiştirdiği sabit sıcaklık değerleridir.
- Öz Isı: Bir gram maddenin sıcaklığını 1°C artırmak için gereken ısı miktarıdır.
- Genleşme Katsayısı: Sıcaklık artışıyla maddenin boyutlarındaki değişim oranıdır (Gazlar için ayırt edici değildir).
- Çözünürlük: Bir maddenin belirli bir çözücü içindeki çözünebilme kapasitesidir.
- Esneklik: Katı maddeler için ayırt edici olan, kuvvet uygulandığında şekil değiştirme ve kuvvet kalktığında eski haline dönme özelliğidir.
- İletkenlik: Maddenin ısıyı veya elektriği iletme yeteneğidir; her maddenin iletkenlik düzeyi farklıdır.
Daha detaylı bilgi için Fiziksel ve Kimyasal Değişimler Arasındaki Farklar içeriğimize göz atabilirsiniz.
Maddenin Fiziksel Halleri
Maddeler, tanecikleri arasındaki çekim kuvvetine ve enerji seviyelerine göre doğada dört temel halde bulunur.
Katı, Sıvı ve Gaz Hali
Katı: Tanecikler birbirine çok yakındır ve sadece titreşim hareketi yaparlar. Belirli bir şekilleri ve hacimleri vardır.
Sıvı: Tanecikler katılara göre daha serbesttir; titreşim ve yer değiştirme (akma) hareketi yaparlar. Belirli bir hacimleri vardır ancak şekilleri bulundukları kaba göre değişir.
Gaz: Tanecikler arası boşluk en fazladır. Tanecikler her yöne serbestçe hareket eder (titreşim, öteleme, dönme). Belirli bir şekilleri ve hacimleri yoktur.
Plazma Hali: Maddenin Dördüncü Hali
Gaz halindeki bir maddeye çok yüksek enerji verildiğinde elektronlar atomlardan ayrılır. Ortamda serbest iyonlar ve elektronların bir arada bulunduğu bu “iyonize gaz” karışımına plazma denir. Güneş, yıldızlar, şimşek ve floresan lambalar plazma haline örnektir. Plazmalar elektriği çok iyi iletir ve manyetik alanlardan etkilenir.
Maddenin Yapısı: Atom ve Alt Parçacıklar
Maddenin en küçük yapı taşı atomdur. Atomlar; merkezdeki çekirdekte bulunan pozitif yüklü protonlar, yüksüz nötronlar ve çekirdek etrafındaki katmanlarda çok hızlı hareket eden negatif yüklü elektronlardan oluşur.
Aynı tür atomların bir araya gelmesiyle elementler, farklı tür atomların belirli oranlarda kimyasal bağlarla birleşmesiyle bileşikler oluşur. Maddenin tüm fiziksel ve kimyasal kimliğini, bu atomik dizilim ve tanecikler arası etkileşimler belirler.
Konuyla ilgili daha derinlemesine bilgi için Atom Nedir? Atomun Yapısı ve Parçacıkları yazımızı inceleyebilirsiniz.
Fiziksel Hallerin Karşılaştırma Tablosu
| Özellik | Katı | Sıvı | Gaz |
|---|---|---|---|
| Tanecik Hareketi | Sadece Titreşim | Titreşim ve Öteleme | Titreşim, Öteleme ve Dönme |
| Belirli Şekil | Var | Yok (Kabın şeklini alır) | Yok |
| Belirli Hacim | Var | Var | Yok (Kabın hacmini alır) |
| Sıkıştırılabilirlik | Yok denilecek kadar az | Çok az (İhmal edilir) | Çok yüksek |
Sıkça Sorulan Sorular
Işık bir madde midir?
Hayır, ışık bir enerji formudur. Maddenin temel şartları olan kütle ve hacme sahip değildir.
Hava bir madde midir?
Evet, hava bir gaz karışımıdır; kütlesi vardır ve boşlukta yer kaplar.
Kütle ve ağırlık aynı şey midir?
Hayır. Kütle değişmeyen madde miktarıdır (kg/g), ağırlık ise bu kütleye etki eden yerçekimi kuvvetidir (Newton). Ağırlık bulunulan gezegene veya yüksekliğe göre değişebilir.
Sıvılar sıkıştırılabilir mi?
Bilimsel olarak sıvılar çok küçük bir miktar sıkıştırılabilir ancak bu miktar ihmal edilecek kadar azdır. Bu yüzden fizik ve kimya problemlerinde “sıvılar sıkıştırılamaz” kabul edilir.
Sonuç
Madde, evrenin fiziksel dokusunu oluşturan temel unsurdur. Kütle, hacim, eylemsizlik ve tanecikli yapı gibi ortak özellikler tüm maddeleri kapsarken; özkütle, iletkenlik ve erime noktası gibi ayırt edici özellikler maddelerin kimliğini belirler. Maddenin halleri arasındaki geçişler, taneciklerin enerjisindeki değişimle açıklanır. Bu temel kavramları kavramak, modern bilimin ve teknolojinin işleyişini anlamak için atılan ilk adımdır.
Maddenin sınıflandırılması hakkında daha fazla bilgi için Saf Maddeler ve Karışımlar: Element ve Bileşikler içeriğimizi ziyaret edebilirsiniz.