Gaz, maddenin en yüksek enerjili ve en düzensiz halidir. Tanecikleri arasındaki boşlukların çok fazla olması nedeniyle belirli bir şekli ve hacmi yoktur; bulundukları kabı tamamen doldururlar. Sıkıştırılabilme ve akışkanlık en belirgin fiziksel özellikleridir.
Maddenin Gaz Hali ve Tanecik Yapısı
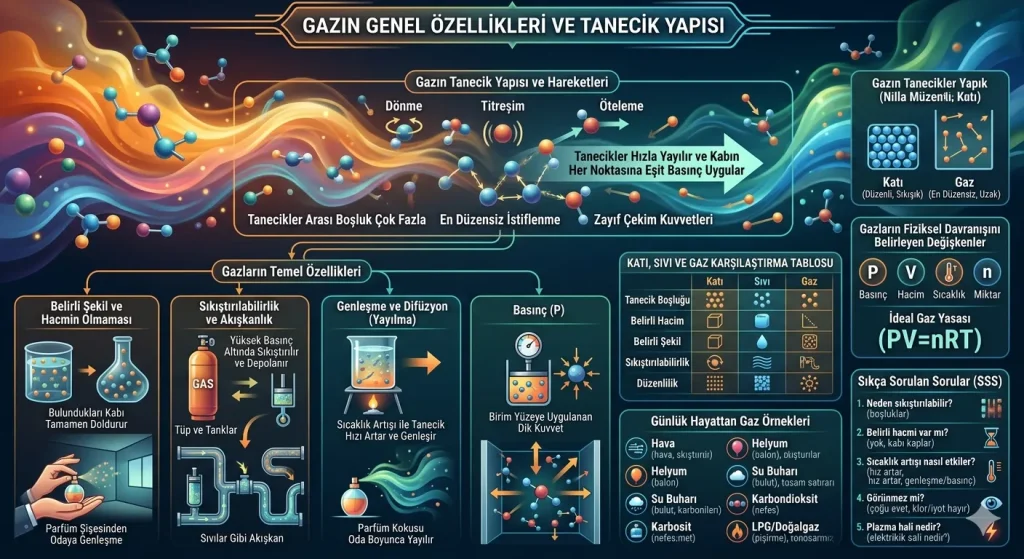
Maddenin dört temel halinden biri olan gaz hali, taneciklerin (atom veya moleküllerin) birbirinden en uzak olduğu ve en serbest hareket ettiği evredir. Katı ve sıvıların aksine, gaz tanecikleri arasındaki çekim kuvvetleri oldukça zayıftır. Bu durum, gazların bulundukları ortamda hızla yayılmasını ve kabın her noktasına eşit basınç uygulamasını sağlar. Günlük hayatta soluduğumuz hava, ocaklarda kullanılan doğalgaz ve su buharı maddenin gaz haline verilebilecek en temel örneklerdir.
Daha kapsamlı bir bakış için maddenin halleri içeriğimize göz atabilirsiniz.
Gazların Genel Özellikleri Nelerdir?
Gazların fiziksel davranışlarını anlamak için tanecik yapısını incelemek gerekir. Gazları diğer madde hallerinden ayıran temel özellikler şunlardır:
Tanecikler Arası Boşluk ve Düzensizlik
Gazlarda tanecikler arasındaki boşluklar, taneciklerin kendi hacimlerine oranla çok büyüktür. Bu nedenle gazlar, maddenin en düzensiz hali olarak tanımlanır. Tanecikler; dönme, titreşim ve öteleme hareketlerini bir arada yaparak sürekli hareket halindedir.
Sıkıştırılabilirlik ve Akışkanlık
Gaz tanecikleri arasındaki boşluklar çok fazla olduğu için, üzerlerine basınç uygulandığında bu boşluklar azalır ve gazlar kolayca sıkıştırılabilir. Bu özellik, gazların tüplerde veya tanklarda depolanmasını sağlar. Ayrıca gazlar, sıvılar gibi akışkan bir yapıya sahiptir; bir noktadan başka bir noktaya kolayca süzülebilirler.
Belirli Bir Şekil ve Hacmin Olmaması
Gazların kendilerine has sabit bir şekli veya hacmi yoktur. Konuldukları kabın şeklini alırlar ve kabın hacmi ne kadarsa o hacme yayılırlar. Küçük bir parfüm şişesindeki gaz, oda kapısı açıldığında tüm odayı kaplayacak şekilde genleşebilir.
Genleşme ve Difüzyon (Yayılma)
Sıcaklık artışı ile gaz taneciklerinin hızı artar ve gaz genleşir. Aynı zamanda gazlar, yüksek konsantrasyonlu bir bölgeden düşük konsantrasyonlu bir bölgeye kendiliğinden yayılırlar. Bu olaya difüzyon denir. Bir odanın köşesine sıkılan parfüm kokusunun kısa sürede her yere ulaşması difüzyonun en net örneğidir.
Gazların Fiziksel Davranışını Belirleyen Değişkenler
Bilimsel olarak gazların durumunu tanımlamak için dört temel değişken kullanılır:
- Basınç (P): Gaz taneciklerinin birim yüzeye uyguladığı dik kuvvettir.
- Hacim (V): Gazın içinde bulunduğu kabın toplam hacmidir.
- Sıcaklık (T): Gaz taneciklerinin ortalama kinetik enerjisinin bir ölçüsüdür (Genellikle Kelvin cinsinden hesaplanır).
- Miktar (n): Gazın mol sayısı cinsinden miktarıdır.
Kritik Bilgi: Bu dört temel değişken arasındaki ilişki, bilimsel çalışmalarda İdeal Gaz Yasası (PV=nRT) ile formüle edilir.
Katı, Sıvı ve Gaz Karşılaştırma Tablosu
Maddenin üç temel halini aşağıdaki tablo üzerinden hızlıca karşılaştırabilirsiniz:
| Özellik | Katı | Sıvı | Gaz |
|---|---|---|---|
| Tanecik Boşluğu | Yok denecek kadar az | Az | Çok fazla |
| Belirli Hacim | Var | Var | Yok |
| Belirli Şekil | Var | Yok (Kabın şekli) | Yok (Kabın şekli) |
| Sıkıştırılabilirlik | Sıkıştırılamaz | İhmal edilecek kadar az | Çok yüksek |
| Düzenlilik | En düzenli | Orta | En düzensiz |
Maddenin diğer halleri hakkında daha detaylı bilgi için katıların özellikleri ve sıvı maddelerin özellikleri yazılarımızı inceleyebilirsiniz.
Günlük Hayattan Gaz Örnekleri
Çevremizde gördüğümüz veya göremediğimiz pek çok madde gaz halindedir:
- Hava: Azot, oksijen ve diğer gazların karışımıdır.
- Helyum: Uçan balonlarda kullanılan hafif bir gazdır.
- Su Buharı: Suyun gaz fazına geçmiş halidir.
- Karbondioksit: Nefes verirken dışarı attığımız veya bitkilerin fotosentezde kullandığı gazdır.
- LPG ve Doğalgaz: Isınma ve pişirme amacıyla kullanılan enerji kaynaklarıdır.
Sıkça Sorulan Sorular (SSS)
Gazlar neden sıkıştırılabilir?
Gaz tanecikleri arasında çok büyük boşluklar bulunur. Basınç uygulandığında bu boşluklar daraldığı için gazlar kolayca sıkıştırılabilir. Katı ve sıvılarda tanecikler birbirine çok yakın olduğu için bu mümkün değildir.
Gazların belirli bir hacmi var mıdır?
Hayır, gazların belirli bir hacmi yoktur. Gazlar bulundukları kabın hacmini tamamen kaplarlar. Kap ne kadar büyükse gaz o kadar yayılır.
Sıcaklık artışı gazları nasıl etkiler?
Sıcaklık arttığında gaz taneciklerinin kinetik enerjisi ve hızı artar. Bu durum, sabit basınçlı sistemlerde hacmin artmasına (genleşme), sabit hacimli sistemlerde ise basınç artışına neden olur.
Bütün gazlar görünmez midir?
Hayır, çoğu gaz renksiz ve şeffaf olduğu için görünmezdir. Ancak klor gazı (sarı-yeşil) veya iyot buharı (mor) gibi renkli ve gözle görülebilen gazlar da mevcuttur.
Gazlar elektrik akımını iletir mi?
Normal şartlar altında gazlar yalıtkandır. Ancak yüksek voltaj veya iyonlaşma durumunda iletkenlik kazanabilirler. Daha fazlası için plazma hali nedir içeriğimize bakabilirsiniz.
Sonuç
Gazlar, maddenin en dinamik ve düzensiz hali olarak evrenin büyük bir kısmını oluşturur. Tanecikler arası boşluğun fazla olması onlara sıkıştırılabilme, yayılma ve akışkanlık gibi kritik özellikler kazandırır. Kimya ve fizik biliminin temelini oluşturan gaz yasalarını anlamak için bu genel özellikleri kavramak oldukça önemlidir. Maddenin halleri arasındaki dönüşümleri öğrenmek isterseniz fiziksel değişimler ve kimyasal değişimler rehberimizi okuyabilirsiniz.
