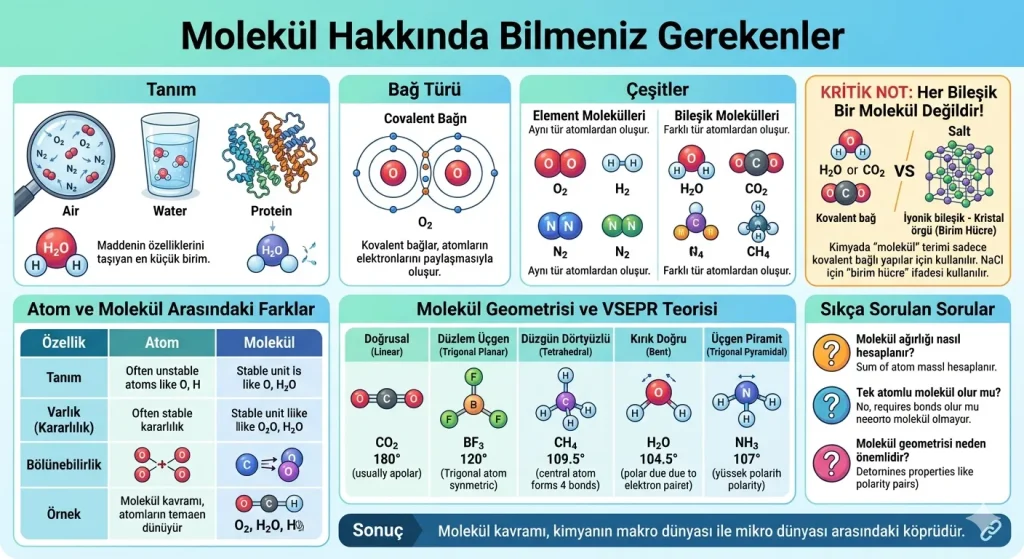
Özet: Molekül Hakkında Bilmeniz Gerekenler
- Tanım: İki veya daha fazla atomun kimyasal bağlarla bir araya gelerek oluşturduğu, maddenin özelliklerini taşıyan en küçük birime molekül denir.
- Bağ Türü: Moleküller, atomların elektronlarını paylaşmasıyla oluşan kovalent bağlar sayesinde bir arada tutulur.
- Çeşitler: Aynı tür atomlardan oluşanlara “element molekülü”, farklı tür atomlardan oluşanlara “bileşik molekülü” denir.
- Geometri: Moleküllerin uzaydaki dizilimi (VSEPR teorisi), maddenin polarlığını, kaynama noktasını ve çözünürlüğünü doğrudan etkiler.
Molekül Nedir? Temel Tanım
İçtiğimiz suyun tadından soluduğumuz havanın kalitesine, vücudumuzdaki proteinlerin işleyişinden kullandığımız ilaçların etkisine kadar her şey moleküllerin yapısıyla ilgilidir. En temel tanımıyla molekül; en az iki atomun belirli bir düzende, güçlü kimyasal kuvvetlerle birbirine bağlanması sonucu oluşan elektriksel olarak nötr gruplardır. Kimya biliminde molekül, bir saf maddenin kimyasal özelliklerini kaybetmeden bölünebileceği en küçük yapı taşıdır.
Doğadaki pek çok madde, kararsız olan atomların daha kararlı hale gelmek için birleşmesiyle oluşur. Bu süreçte atomun yapısı ve parçacıkları hakkında bildiğimiz temel kurallar devreye girer; atomlar elektronlarını paylaşarak moleküler yapıları meydana getirir. Her molekülün kendine has bir kütlesi, büyüklüğü ve üç boyutlu bir geometrik şekli vardır.
Molekül Çeşitleri Nelerdir?
Moleküller, içerdikleri atomların türüne göre iki ana grupta incelenir:
1. Element Molekülleri
Aynı tür atomların bir araya gelmesiyle oluşurlar. Doğada pek çok element tek atomlu değil, moleküler yapıda bulunur. Örneğin; Hidrojen (H2), Azot (N2) ve Oksijen (O2) gibi yapılar element moleküllerine örnektir.
2. Bileşik Molekülleri
En az iki farklı tür atomun belirli oranlarda birleşmesiyle oluşan yapılardır. Su (H2O), Karbondioksit (CO2) ve Metan (CH4) en yaygın örneklerdir. Bileşik molekülleri, kendisini oluşturan elementlerden tamamen farklı fiziksel ve kimyasal özellikler sergiler.
Moleküler Bağlar ve Kritik Bir Fark
Moleküllerin oluşabilmesi için atomların birbirine kovalent bağ ile bağlanması gerekir. Ancak burada öğrencilerin sıkça karıştırdığı çok önemli bir nokta vardır:
KRİTİK NOT: Her Bileşik Bir Molekül Değildir!
Kimyada “molekül” terimi sadece kovalent bağlı yapılar için kullanılır. Örneğin sofra tuzu (NaCl) iyonik bir bileşiktir. İyonik bileşikler bağımsız moleküllerden değil, sonsuz bir “kristal örgü” yapısından oluşur. Bu yüzden NaCl için molekül değil, “birim hücre” ifadesi kullanılır.
Atomlar arasında elektronların ortaklaşa kullanılmasıyla kurulan kimyasal bağlar, molekülün sağlamlığını belirler. Eğer elektronlar eşit paylaşılıyorsa “apolar kovalent”, farklı güçlerle çekiliyorsa “polar kovalent” bağlar oluşur.
Molekül Geometrisi ve VSEPR Teorisi
Moleküller sadece kağıt üzerindeki formüllerden ibaret değildir; uzayda belirli bir üç boyutlu şekle sahiptirler. Bu şekli açıklayan VSEPR (Değerlik Kabuğu Elektron Çifti İtme Kuramı), atomların etrafındaki elektronların birbirini iterek en uzak konuma yerleştiğini savunur.
Molekülün geometrisi, maddenin polarlığını ve dolayısıyla su gibi çözücülerde çözünüp çözünmeyeceğini belirler. İşte temel molekül geometrileri:
| Geometri | Açı | Örnek | Özellik |
|---|---|---|---|
| Doğrusal | 180° | CO2, BeH2 | Genellikle apolardır. |
| Düzlem Üçgen | 120° | BH3, BF3 | Simetrik yapılıdır. |
| Düzgün Dörtyüzlü | 109.5° | CH4 | Merkez atom 4 bağ yapar. |
| Kırık Doğru | 104.5° | H2O | Elektron çiftleri nedeniyle polardır. |
| Üçgen Piramit | 107° | NH3 | Yüksek polarlık gösterir. |
Atom ve Molekül Arasındaki Farklar
Maddeyi tanırken atom ve molekül kavramlarını birbirinden ayırmak, kimyasal tepkimeleri anlamak için şarttır:
| Özellik | Atom | Molekül |
|---|---|---|
| Tanım | Maddenin en küçük yapı taşıdır. | En az iki atomun bağ yapmış halidir. |
| Varlık | Soygazlar hariç genellikle kararsızdır. | Bağımsız ve kararlı birimlerdir. |
| Bölünebilirlik | Kimyasal yollarla daha küçüğe bölünemez. | Kimyasal yollarla atomlarına ayrılabilir. |
| Örnek | Fe, He, O, H | O2, H2O, C6H12O6 |
Sıkça Sorulan Sorular
1. Molekül ağırlığı (MA) nasıl hesaplanır?
Molekülü oluşturan her bir atomun kütlesi, formüldeki sayılarıyla çarpılır ve toplanır. Örneğin H2O için: (2 x 1) + (1 x 16) = 18 g/mol.
2. Tek atomlu molekül olur mu?
Hayır. “Molekül” tanımı gereği en az iki atomun bağ yapması gerekir. Soygazlar (He, Ne vb.) doğada tek atomlu (monatomik) halde bulunurlar ancak molekül olarak adlandırılmazlar.
3. Molekül geometrisi neden önemlidir?
Geometri, molekülün polarlığını belirler. Örneğin suyun “kırık doğru” yapısı onu polar bir çözücü yapar; eğer su doğrusal olsaydı, bugün bildiğimiz pek çok biyolojik süreç gerçekleşemezdi.
Sonuç
Molekül kavramı, kimyanın makro dünyası ile mikro dünyası arasındaki köprüdür. Maddenin fiziksel halinden kimyasal tepkimelere girme isteğine kadar her detay, moleküllerin yapısında gizlidir. Element ve bileşik molekülleri arasındaki farkı kavramak, özellikle iyonik yapılarla moleküler yapıları karıştırmamak kimya derslerindeki başarınızın anahtarıdır. Konuyu daha derinlemesine incelemek için periyodik tablo ve elementlerin özellikleri sayfamıza göz atabilirsiniz.