Orbital, bir elektronun atom içinde bulunma olasılığının yüksek olduğu alanı ifade eder. Atom yörüngeleri olarak da bilinen orbitaller, elektronların dağılımını ve enerji seviyelerini belirler. s, p, d ve f orbitalleri farklı şekil ve enerji özelliklerine sahiptir.
Orbitaller nedir?
Orbitaller, atom çekirdeği etrafında elektronların bulunma ihtimalinin yüksek olduğu üç boyutlu bölgeler olarak tanımlanır. Klasik anlamda elektronların belirli yörüngelerde döndüğü düşüncesi yerine, kuantum mekaniği yaklaşımıyla elektronların belirli bir bölgede bulunma olasılığı vardır. Bu bölgeler orbitaller olarak adlandırılır ve her orbital farklı şekil ve enerji seviyesine sahiptir.
Atomda elektronlar, enerji seviyelerine göre farklı orbitallerde yer alır. Bu orbitaller, elektronların atom içindeki dağılımını ve kimyasal bağların oluşumunu etkiler. s, p, d ve f orbitalleri, atomun farklı enerji seviyelerinde bulunur ve her biri farklı şekil ve kapasiteye sahiptir.
Orbitaller özellikleri nelerdir?
s orbitali
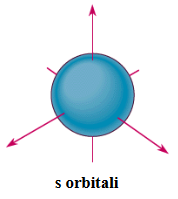
Küreseldir. En fazla iki elektron alır. Baş kuantum sayısı büyüdükçe s orbitallerinin enerjisi artar. İkincil kuantum sayısının sıfır değerine karşılık gelir.
p orbitalleri

İkinci veya daha üst enerji düzeylerinde bulunur. 3 orbitalden oluşur (px, py ve pz orbitalleri). Bu üç orbitalin enerjileri birbirine eşittir ve en çok 6 elektron alır. İkincil kuantum sayısının 1 değerine karşılık gelir.
d orbitalleri

Üçüncü veya daha üst temel enerji düzeylerinde bulunur. 5 orbitalden oluşur ve en çok 10 elektron alır. l’nin 2 değerine karşılık gelir.
f orbitalleri
Dördüncü veya daha üst enerji düzeylerinde bulunur. 7 orbitalden oluşur ve en çok 14 elektron alır. İkincil kuantum sayısının 3 değerine karşılık gelir.
Orbitallere elektron dağılımı
Atom numarası bilinen bir atomun, elektron dağılımını gösteren şemaya atomun orbital şeması denir. Orbitaller ![]() şeklinde gösterilir.
şeklinde gösterilir.
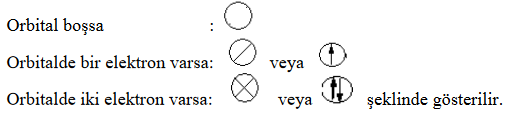
Elektronların orbitallere dağılımı yazılırken aşağıdaki kurallar uygulanır.
- Çekirdeğe en yakın olan en düşük enerjili orbitalden başlanarak sıra ile en yüksek enerjili orbitale doğru doldurulur (Aufbau kuralı).
- Her orbital en fazla iki elektron alır. Bu elektronların spinleri (dönme yönleri) zıttır (Pauli kuralı).
- Eş enerjili orbitallere, önce elektronlar birer birer yerleştirilir. Sonra her bir orbitaldeki elektron sayısı ikiye tamamlanır (Hund kuralı).
Atomların elektron dağılımlarında orbitalin sembolünün önüne hangi temel enerji düzeyinde olduğu, sağ üst kısmına ise içerdiği elektron sayısı yazılır.

Küresel simetri
Eş enerjili orbitallerin yarı dolu veya tam dolu olması atoma küresel simetri özelliği kazandırır. Eş enerjili orbitallerin yarı dolu veya tam dolu olması durumunda elektronlar çekirdek tarafından daha kuvvetli çekildiğinden çekirdeğe yaklaşır ve atom çapı küçülür. Bu durum atoma kararlılık kazandırır. Örneğin; s orbitalinde 1 veya 2, p orbitalinde 3 veya 6, d orbitalinde 5 veya 10, f orbitalinde 7 veya 14 elektron bulunması atoma küresel simetrik yapı kazandırır.
Örnekler
- Doğru: Bir atomda 1s orbitalinde en fazla 2 elektron bulunabilir.
- Doğru: p orbitalleri üç farklı yönde (x, y, z) bulunur ve toplamda 6 elektron alabilir.
- Yanlış: Elektronlar atomda belirli yörüngelerde sabit hızla döner.
- Yanlış: d orbitalleri sadece iki tane vardır ve küresel şekildedir.
En sık yapılan hatalar
- Elektronların kesin yörüngelerde dolaştığını düşünmek.
- Orbitallerin şekillerini karıştırmak (örneğin, p orbitallerini küresel sanmak).
- Her enerji seviyesinde tüm orbital tiplerinin bulunacağını varsaymak.
- Orbitallerin kapasitesini yanlış anlamak (örneğin, bir orbitalde 3 elektron olabileceğini düşünmek).
Sık sorulan sorular
Orbitaller neden farklı şekillere sahiptir?
Orbitallerin şekilleri, elektronların dalga fonksiyonlarının çözümlerinden kaynaklanır. Elektronların bulunma olasılıklarının dağılımı, kuantum sayıları tarafından belirlenir ve bu da orbitallerin farklı geometrik şekillerde olmasına neden olur.
Ayrıca bakın;


