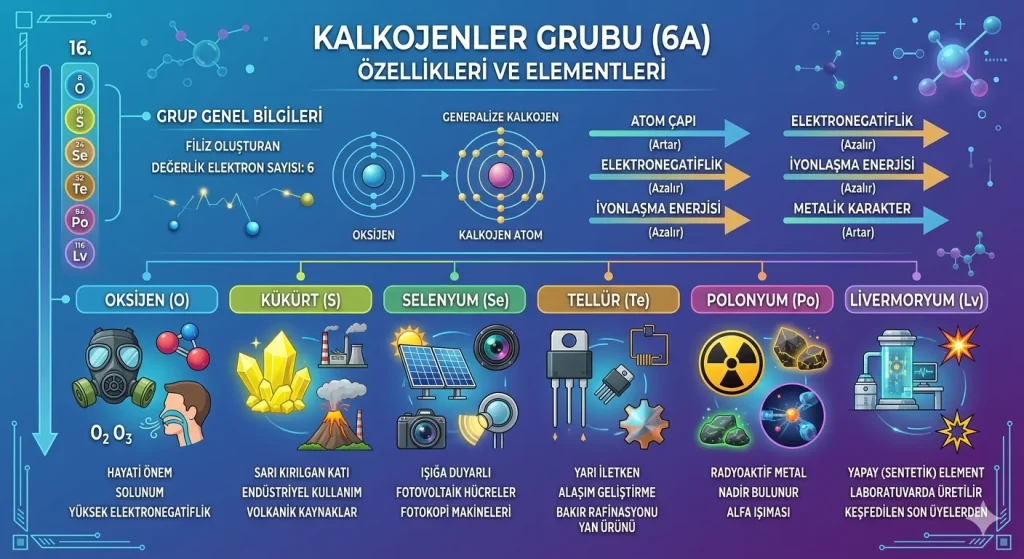
Özet: Kalkojenler, periyodik sistemin 16. grubunda (6A grubu) yer alan; oksijen, kükürt, selenyum, tellür, polonyum ve livermoryum elementlerinden oluşan gruptur. “Filiz oluşturan” anlamına gelen bu grup, doğada genellikle metallerle bileşik yapmış halde (oksitler ve sülfürler) bulunur. Tüm üyelerinin değerlik elektron sayısı 6’dır.
Kalkojenler, kimya eğitiminde periyodik sistem ve özellikleri konusunun en kritik başlıklarından biridir. Bu grup, ametal karakterden metalik karaktere geçişin en net gözlemlendiği dikey sütundur. Grubun ilk üyesi olan oksijen yaşamın temel taşıyken, alt sıralardaki elementler endüstriyel ve ileri teknolojik alanlarda stratejik öneme sahiptir.
Kalkojenler Grubu Elementleri Nelerdir?
6A grubu, atom numarası arttıkça fiziksel ve kimyasal özellikleri belirgin şekilde değişen altı elementten oluşur:
- Oksijen (O): Grubun ilk üyesi, renksiz ve hayati öneme sahip bir gazdır.
- Kükürt (S): Sarı renkli, doğada yaygın bulunan kırılgan bir ametaldir.
- Selenyum (Se): Işığa duyarlı (fotosensitif) özellikleri olan bir ametaldir.
- Tellür (Te): Metalik görünümlü, yarı iletken özellik gösteren bir yarı metaldir.
- Polonyum (Po): Nadir bulunan, oldukça radyoaktif bir metaldir.
- Livermoryum (Lv): Laboratuvar ortamında sentezlenen yapay bir elementtir.
6A Grubu (Kalkojenler) Genel Özellikleri
Kalkojenlerin kimyasal davranışlarını belirleyen temel karakteristik özellikler şunlardır:
- Değerlik Elektron Sayısı: Grubun tüm elementlerinin son katmanında 6 elektron bulunur. Elektron dizilimleri ns2 np4 ile sonlanır.
- Yükseltgenme Basamakları: Kararlı yapıya (oktet) ulaşmak için genellikle 2 elektron alarak -2 iyon yüküne sahip olurlar. Oksijen hariç diğer elementler +4 ve +6 gibi pozitif yükseltgenme basamaklarında da bulunabilirler.
- Karakter Değişimi: Grupta yukarıdan aşağıya doğru inildikçe ametal özellik azalırken, metalik özellik artar.
- Bağ Yapma Eğilimi: Ametallerle kovalent, metallerle iyonik bağ oluşturma eğilimindedirler. Kimyasal etkileşimlerin detayları için kimyasal bağlar ve türleri içeriğimizi inceleyebilirsiniz.
Elementlerin Fiziksel ve Kimyasal Karşılaştırması
| Element | Sembol | Atom No | Oda Koşulundaki Hali | Sınıfı |
|---|---|---|---|---|
| Oksijen | O | 8 | Gaz | Ametal |
| Kükürt | S | 16 | Katı | Ametal |
| Selenyum | Se | 34 | Katı | Ametal |
| Tellür | Te | 52 | Katı | Yarı Metal |
| Polonyum | Po | 84 | Katı | Metal |
| Livermoryum | Lv | 116 | Katı (Tahmin Edilen) | Metal (Sentetik) |
Oksijen (O) ve Kükürt (S)
Oksijen, yer kabuğunda en bol bulunan elementtir. Havada diatomik (O2) veya ozon (O3) molekülleri şeklinde bulunur. Grubun diğer üyelerinden farklı olarak oda sıcaklığında gaz halindedir ve elektronegatifliği gruptaki en yüksek elementtir.
Kükürt ise doğada hem elementel halde hem de sülfat/sülfür bileşikleri olarak bulunur. Barut yapımı, sülfürik asit üretimi ve kauçuğun işlenmesi (vulkanizasyon) gibi pek çok endüstriyel süreçte temel maddedir. Oksijenin aksine oda koşullarında katı formdadır.
Selenyum (Se) ve Tellür (Te)
Selenyum, ışığa maruz kaldığında elektrik iletkenliği artan özel bir elementtir. Bu fotokondüktif özelliği sayesinde fotokopi makinelerinde, güneş pillerinde ve ışık sensörlerinde yaygın olarak kullanılır.
Tellür ise genellikle bakır rafinasyonu sırasında yan ürün olarak elde edilir. Metalürjide alaşımların işlenebilirliğini artırmak için kullanılır ve yarı iletken teknolojisinde önemli bir yere sahiptir.
Grup İçindeki Periyodik Eğilimler
6A grubunda yukarıdan aşağıya (Oksijenden Livermoryuma) doğru gidildikçe gözlenen temel değişimler şunlardır:
- Atom Çapı: Katman sayısı arttığı için atom yarıçapı belirgin şekilde artar.
- Elektronegatiflik: Çekirdeğin elektronları çekme gücü azaldığı için yukarıdan aşağıya doğru düşer.
- İyonlaşma Enerjisi: En dış katmandaki elektronları koparmak kolaylaştığı için iyonlaşma enerjisi azalır.
- Erime ve Kaynama Noktası: Molekül kütlesi ve Van der Waals kuvvetlerinin artması nedeniyle genellikle aşağı doğru artış gösterir.
Bu periyodik değişimler, halojenler grubu 7A gibi komşu gruplarla benzerlik gösterse de, kalkojenlerin kendine has reaktiflik dengesi onları kimyasal tepkimelerde benzersiz kılar.
Sıkça Sorulan Sorular
1. Kalkojen ne anlama gelir?
Yunanca “chalkos” (bakır/filiz) ve “genos” (oluşturan) kelimelerinden türetilmiştir. Bu elementlerin çoğu doğada bakır filizlerinin içinde bulunduğu için bu isim verilmiştir.
2. 6A grubu elementleri metal mi ametal mi?
Grup karma bir yapıdadır. Oksijen, kükürt ve selenyum ametal; tellür yarı metal; polonyum ve livermoryum ise metal sınıfındadır.
3. Kalkojenlerin değerlik elektron sayısı kaçtır?
Kalkojenlerin değerlik elektron sayısı 6’dır. Kararlı hale geçmek için genellikle dışarıdan 2 elektron alma eğilimindedirler.
4. Grupta atom çapı en büyük olan element hangisidir?
Grupta en aşağıda yer alan Livermoryum (Lv), en fazla katman sayısına sahip olduğu için en büyük atom çapına sahiptir. Doğal elementler arasında ise Polonyum (Po) en büyüğüdür.
Sonuç
Kalkojenler grubu, periyodik tablonun hem biyolojik yaşam hem de endüstriyel üretim açısından en zengin gruplarından biridir. Oksijenin solunumdaki hayati rolünden kükürdün sanayideki gücüne, selenyumun yüksek teknolojideki yerinden polonyumun radyoaktif doğasına kadar geniş bir yelpazeye yayılırlar. Kimya sınavlarında özellikle bu elementlerin değerlik elektron sayıları, ametallerin genel özellikleri ve gruptaki metalik karakter değişimi sıkça sorgulanmaktadır.
