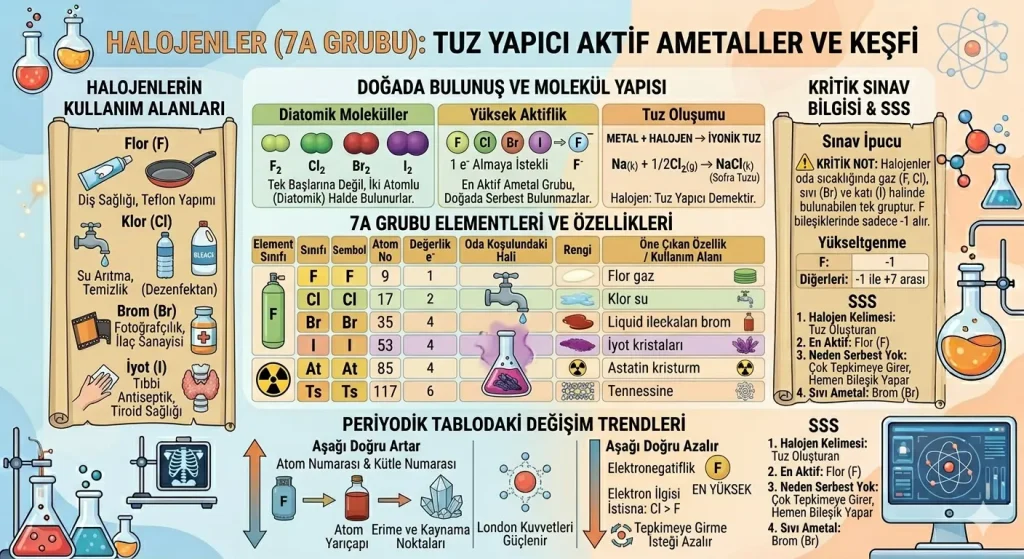
Halojenler, periyodik tablonun en önemli ametal gruplarından biridir. Bu grup elementleri özellikle elektron alma eğilimleri, yüksek elektronegatiflikleri ve metallerle tuz oluşturma özellikleriyle bilinir.
Flor, klor, brom ve iyot günlük hayatta en çok bilinen halojenlerdir. Klor su arıtımında, flor diş sağlığında, iyot antiseptiklerde ve tiroid sağlığında, brom ise bazı endüstriyel alanlarda kullanılır.
Önemli bilgi: Halojenler genellikle doğada serbest atomlar hâlinde bulunmaz. Yüksek reaktiflikleri nedeniyle çoğunlukla bileşikler hâlinde veya iki atomlu moleküller şeklinde bulunurlar.
Halojen Nedir?
Halojen, periyodik tablonun 7A grubunda yer alan elementlere verilen addır. Halojen kelimesi “tuz oluşturan” anlamına gelir. Bu isim, halojenlerin metallerle birleşerek tuzları oluşturabilmesinden gelir.
Halojenlerin son katmanlarında 7 değerlik elektronu bulunur. Kararlı elektron düzenine ulaşmak için genellikle 1 elektron alırlar ve -1 yüklü iyon yani anyon oluştururlar.
Bu konuyu daha iyi anlamak için önce Periyodik Tablo Nedir?, Ametal Nedir? ve Elektronegatiflik Nedir? yazılarını inceleyebilirsin.
Halojenler Hangileridir?
7A grubunda yer alan halojen elementler şunlardır:
| Element | Sembol | Atom Numarası | Oda Koşullarındaki Hâli | Öne Çıkan Özellik |
|---|---|---|---|---|
| Flor | F | 9 | Gaz | Elektronegatifliği en yüksek elementtir. |
| Klor | Cl | 17 | Gaz | Su arıtımı ve dezenfeksiyonda kullanılır. |
| Brom | Br | 35 | Sıvı | Oda sıcaklığında sıvı olan tek ametaldir. |
| İyot | I | 53 | Katı | Antiseptiklerde ve tiroid sağlığında önemlidir. |
| Astatin | At | 85 | Katı | Radyoaktif ve doğada çok az bulunan elementtir. |
| Tennessine | Ts | 117 | Yapay element | Laboratuvar ortamında sentezlenen çok ağır elementtir. |
Halojenlerin Genel Özellikleri
- Periyodik tablonun 7A grubunda yer alırlar.
- Ametal özellik gösterirler.
- Son katmanlarında 7 değerlik elektronu bulunur.
- Genellikle 1 elektron alarak -1 yüklü iyon oluştururlar.
- Metallerle iyonik bağlı tuzlar oluşturabilirler.
- Kendi aralarında veya başka ametallerle kovalent bağ oluşturabilirler.
- Doğada çoğunlukla iki atomlu moleküller hâlinde bulunabilirler.
- Grupta aşağı doğru inildikçe kimyasal aktiflik genellikle azalır.
Halojenler Neden Tuz Oluşturan Elementlerdir?
Halojenler, metallerle kolayca tepkimeye girerek iyonik bileşikler oluşturabilir. Bu bileşiklerin çoğu tuz olarak adlandırılır.
Örneğin sodyum metali ile klor gazı tepkimeye girerek sodyum klorür yani sofra tuzunu oluşturur.
Örnek: 2Na + Cl2 → 2NaCl
Bu nedenle halojenler “tuz oluşturan” elementler olarak bilinir.
Halojenlerin Fiziksel Özellikleri
Halojenler, oda koşullarında farklı fiziksel hallerde bulunabilen bir gruptur. Flor ve klor gaz, brom sıvı, iyot ise katıdır.
| Element | Fiziksel Hâl | Renk / Görünüm | Not |
|---|---|---|---|
| Flor | Gaz | Açık sarı | Çok aktif bir ametaldir. |
| Klor | Gaz | Sarı-yeşil | Keskin kokulu ve zehirlidir. |
| Brom | Sıvı | Kızıl-kahverengi | Oda sıcaklığında sıvı olan tek ametaldir. |
| İyot | Katı | Mor-siyah parlak katı | Isıtıldığında süblimleşebilir. |
Halojenlerin Kimyasal Özellikleri
Halojenlerin kimyasal özellikleri, son katmanlarında 7 elektron bulundurmalarıyla yakından ilişkilidir. Bu elementler bir elektron alarak kararlı elektron düzenine ulaşmaya çalışır.
| Kimyasal Özellik | Açıklama | Örnek |
|---|---|---|
| -1 iyon oluşturma | Genellikle 1 elektron alarak -1 yüklü iyon oluştururlar. | Cl + e– → Cl– |
| Yüksek elektronegatiflik | Bağ elektronlarını güçlü çekebilirler. | Flor en elektronegatif elementtir. |
| Tuz oluşturma | Metallerle iyonik bileşikler oluşturabilirler. | NaCl, KBr |
| Diatomik molekül oluşturma | Doğada iki atomlu moleküller hâlinde bulunabilirler. | F2, Cl2, Br2, I2 |
Halojenlerde Aktiflik Nasıl Değişir?
Halojenler ametal oldukları için kimyasal aktiflikleri elektron alma eğilimleriyle ilişkilidir. Grupta yukarıdan aşağıya inildikçe atom yarıçapı artar ve çekirdeğin elektron çekme gücü azalır.
Bu nedenle halojenlerde grupta aşağıya doğru inildikçe aktiflik genellikle azalır. En aktif halojen flordur.
| Yön | Atom Yarıçapı | Elektronegatiflik | Ametalik Aktiflik |
|---|---|---|---|
| 7A grubunda aşağı doğru | Artar. | Azalır. | Azalır. |
Kısa kural: Halojenlerde aktiflik genellikle F > Cl > Br > I şeklindedir.
Halojenlerde Erime ve Kaynama Noktası Nasıl Değişir?
Halojenler iki atomlu moleküller hâlinde bulunabilir. Grupta aşağı doğru inildikçe atom ve molekül büyüklüğü artar. Elektron sayısının artması London kuvvetlerini güçlendirir.
Bu nedenle halojenlerde grupta aşağı inildikçe erime ve kaynama noktaları genellikle artar.
| Yön | London Kuvvetleri | Erime / Kaynama Noktası | Fiziksel Hâl Değişimi |
|---|---|---|---|
| F’den I’ye doğru | Artar. | Artar. | Gaz → sıvı → katı eğilimi görülür. |
London kuvvetlerini detaylı öğrenmek için Zayıf Etkileşimler ve Fiziksel Bağlar yazısını inceleyebilirsin.
Florun Özellikleri
Flor, en aktif halojen ve elektronegatifliği en yüksek elementtir. Bileşiklerinde genellikle -1 yükseltgenme basamağı gösterir.
- Sembolü F’dir.
- Açık sarı renkli gazdır.
- Çok reaktiftir.
- Diş macunlarında florür bileşikleri kullanılabilir.
Klorun Özellikleri
Klor, sarı-yeşil renkli bir gazdır. Güçlü dezenfektan özelliği nedeniyle su arıtımında ve temizlik ürünlerinde yaygın olarak bilinir.
- Sembolü Cl’dir.
- Oda koşullarında gazdır.
- Keskin kokuludur.
- Sodyumla birleşerek sofra tuzunu oluşturur.
Bromun Özellikleri
Brom, oda sıcaklığında sıvı halde bulunan tek ametaldir. Kızıl-kahverengi renge sahiptir.
- Sembolü Br’dir.
- Oda koşullarında sıvıdır.
- Halojenler arasında fiziksel hâliyle dikkat çeker.
- Bazı sanayi ve kimyasal uygulamalarda kullanılır.
İyodun Özellikleri
İyot, oda koşullarında katı hâlde bulunan bir halojendir. Mor-siyah parlak görünüme sahiptir ve ısıtıldığında süblimleşebilir.
- Sembolü I’dir.
- Oda koşullarında katıdır.
- Antiseptiklerde kullanılabilir.
- Tiroid bezinin çalışması için önemlidir.
Halojenlerin Kullanım Alanları
| Halojen | Kullanım Alanı | Neden Önemli? |
|---|---|---|
| Flor | Diş sağlığı, bazı polimerler | Florür bileşikleri diş minesinin korunmasında kullanılabilir. |
| Klor | Su arıtımı, temizlik ürünleri | Mikroorganizmaları etkisiz hâle getirmede kullanılır. |
| Brom | İlaç, fotoğrafçılık, bazı endüstriyel alanlar | Kimyasal bileşikleri farklı alanlarda kullanılır. |
| İyot | Antiseptikler, tiroid sağlığı | Canlılar için eser miktarda gereklidir. |
Halojenler ve Soygazlar Arasındaki Fark
| Özellik | Halojenler | Soygazlar |
|---|---|---|
| Grup | 7A grubu | 8A grubu |
| Değerlik elektron sayısı | 7 | Genellikle 8, helyumda 2 |
| Aktiflik | Yüksektir. | Genellikle düşüktür. |
| İyon oluşturma eğilimi | Genellikle -1 iyon oluştururlar. | İyon oluşturma eğilimleri düşüktür. |
| Örnek | F, Cl, Br, I | He, Ne, Ar, Kr, Xe |
Sık Yapılan Hatalar
1. Halojenleri metal sanmak
Halojenler ametal özellik gösteren elementlerdir. Periyodik tablonun sağ tarafında yer alırlar.
2. Bromun gaz olduğunu düşünmek
Brom oda sıcaklığında sıvı olan tek ametaldir.
3. Halojenlerde aktifliğin aşağı doğru arttığını sanmak
Halojenlerde grupta aşağı inildikçe elektronegatiflik azalır ve ametalik aktiflik genellikle azalır.
4. Florun diğer halojenler gibi pozitif yükseltgenme basamakları alabileceğini düşünmek
Flor elektronegatifliği en yüksek elementtir ve bileşiklerinde genellikle -1 yükseltgenme basamağı gösterir.
Halojenler Konu Özeti
- Halojenler periyodik tablonun 7A grubunda yer alır.
- Halojen kelimesi “tuz oluşturan” anlamına gelir.
- Halojenlerin son katmanında 7 değerlik elektronu bulunur.
- Genellikle -1 yüklü iyon oluştururlar.
- Flor, klor, brom ve iyot en bilinen halojenlerdir.
- Brom oda sıcaklığında sıvı olan tek ametaldir.
- Flor elektronegatifliği en yüksek elementtir.
- Halojenlerde grupta aşağı inildikçe aktiflik genellikle azalır.
- Halojenlerde grupta aşağı inildikçe erime ve kaynama noktası genellikle artar.
Halojenler Mini Test
1. Halojenler periyodik tabloda hangi grupta yer alır?
- A) 1A
- B) 2A
- C) 7A
- D) 8A
Doğru cevap: C
Açıklama: Halojenler periyodik tablonun 7A grubunda yer alır.
2. Elektronegatifliği en yüksek element hangisidir?
- A) Flor
- B) Klor
- C) Brom
- D) İyot
Doğru cevap: A
Açıklama: Flor, elektronegatifliği en yüksek elementtir.
3. Oda sıcaklığında sıvı olan tek ametal hangisidir?
- A) Klor
- B) Brom
- C) Flor
- D) İyot
Doğru cevap: B
Açıklama: Brom, oda sıcaklığında sıvı halde bulunan tek ametaldir.
4. Halojenler genellikle hangi yüklü iyonu oluşturur?
- A) +1
- B) +2
- C) -1
- D) -2
Doğru cevap: C
Açıklama: Halojenler genellikle 1 elektron alarak -1 yüklü iyon oluşturur.
5. Halojenlerde grupta aşağı indikçe aktiflik genellikle nasıl değişir?
- A) Artar
- B) Azalır
- C) Değişmez
- D) Tamamen yok olur
Doğru cevap: B
Açıklama: Halojenlerde aşağı indikçe elektronegatiflik azalır ve ametalik aktiflik genellikle azalır.
Sıkça Sorulan Sorular
Halojen nedir?
Halojen, periyodik tablonun 7A grubunda yer alan aktif ametal elementlere verilen addır.
Halojenler hangileridir?
Flor, klor, brom, iyot, astatin ve tennessine halojenler grubunda yer alır.
Halojen kelimesi ne anlama gelir?
Halojen kelimesi “tuz oluşturan” anlamına gelir. Halojenler metallerle birleşerek tuz oluşturabilir.
En aktif halojen hangisidir?
En aktif halojen flordur. Flor aynı zamanda elektronegatifliği en yüksek elementtir.
Brom neden önemlidir?
Brom, oda sıcaklığında sıvı halde bulunan tek ametal olmasıyla dikkat çeker.
Halojenlerde erime ve kaynama noktası nasıl değişir?
Grupta aşağı doğru inildikçe molekül büyüklüğü ve London kuvvetleri arttığı için erime ve kaynama noktaları genellikle artar.
Bu Konudan Sonra Ne Öğrenmeliyim?
Halojenler konusunu öğrendikten sonra şu konulara geçebilirsin:
Bu konu şu rehberin parçasıdır: Atom ve Periyodik Sistem
