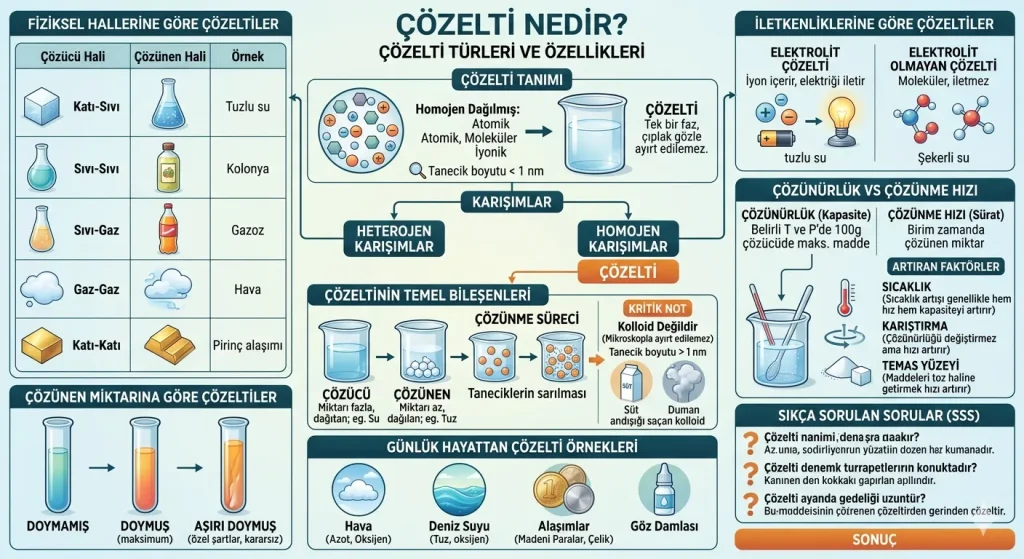
Kısa Özet: Çözelti, iki veya daha fazla maddenin birbiri içerisinde atomik, moleküler veya iyonik düzeyde homojen olarak dağılmasıyla oluşan karışımlardır. Dışarıdan bakıldığında tek bir faz (tek bir madde) gibi görünen çözeltiler, en az bir çözücü ve bir çözünen maddeden meydana gelir.
Kimya biliminde maddeler saf maddeler ve karışımlar olarak ikiye ayrılır. Karışımlar ise kendi içinde homojen ve heterojen olmak üzere iki grupta incelenir. Çözelti, aslında “homojen karışım” teriminin bilimsel karşılığıdır. Bir karışımın çözelti sayılabilmesi için bileşenlerinin her noktada aynı özelliği göstermesi ve bileşenlerin çıplak gözle ya da mikroskopla ayırt edilememesi gerekir.
Çözeltinin Temel Bileşenleri: Çözücü ve Çözünen
Her çözelti en az iki temel bileşenden oluşur. Bu bileşenlerin etkileşimi, çözeltinin fiziksel ve kimyasal özelliklerini belirler.
Çözücü Nedir?
Bir çözeltide genellikle miktarı daha fazla olan ve diğer maddeyi kendi içinde dağıtan bileşene çözücü denir. Kimyada su, en yaygın ve “evrensel” çözücü olarak kabul edilir. Ancak çözücüler sadece sıvı olmak zorunda değildir; katı (alaşımlarda olduğu gibi) veya gaz fazında da olabilirler.
Çözünen Nedir?
Çözücü içerisinde dağılan, genellikle miktarı daha az olan bileşene çözünen denir. Örneğin, tuzlu suda su çözücü, tuz ise çözünendir. Çözünme süreci, çözünen taneciklerinin çözücü molekülleri tarafından sarılmasıyla gerçekleşir.
Kritik Not: Çözelti mi, Kolloid mi?
Bazı karışımlar dışarıdan homojen görünse de aslında “kolloid” olabilir. Bir karışımın gerçek bir çözelti olması için tanecik boyutunun 1 nanometreden (nm) küçük olması gerekir. Süt veya duman gibi karışımlar, tanecikleri ışığı saçtığı için çözelti değil, kolloiddir.
Daha fazla bilgi için: Homojen ve heterojen karışım farkları
Çözelti Türleri Nelerdir?
Çözeltiler; bileşenlerinin fiziksel haline, içerdikleri çözünen miktarına ve elektrik iletkenliklerine göre üç ana başlıkta sınıflandırılır.
1. Fiziksel Hallerine Göre Çözeltiler
Çözeltinin fiziksel halini genellikle çözücünün hali belirler. Aşağıdaki tabloda farklı fiziksel hallerdeki bileşenlerin oluşturduğu çözelti örneklerini inceleyebilirsiniz:
| Çözücü Hali | Çözünen Hali | Çözelti Örneği | Bileşenlerin Durumu |
|---|---|---|---|
| Sıvı | Katı | Tuzlu su, şekerli su | Katının sıvıda dağılması |
| Sıvı | Sıvı | Kolonya, sirke | Sıvı-sıvı karışımı |
| Sıvı | Gaz | Gazoz, deniz suyu | Gazın sıvıda çözünmesi |
| Gaz | Gaz | Hava | Azot ve oksijen karışımı |
| Katı | Katı | Pirinç, çelik, lehim | Metal-metal (Alaşım) |
2. Çözünen Miktarına Göre Çözeltiler
Bir çözeltinin ne kadar madde içerdiği, onun doygunluk durumunu belirler:
- Doymamış Çözelti: Belirli sıcaklık ve basınçta, çözebileceğinden daha az madde içeren çözeltilerdir.
- Doymuş Çözelti: Belirli şartlarda çözebileceği maksimum madde miktarını çözmüş olan çözeltilerdir.
- Aşırı Doymuş Çözelti: Özel şartlar (sıcaklık artışı vb.) altında, normalde çözebileceğinden daha fazla madde içeren kararsız çözeltilerdir.
3. İletkenliklerine Göre Çözeltiler
- Elektrolit Çözelti: İçerisinde iyon barındıran ve elektriği ileten çözeltilerdir (Örn: Tuzlu su).
- Elektrolit Olmayan Çözelti: Moleküler düzeyde çözünen ve elektriği iletmeyen çözeltilerdir (Örn: Şekerli su).
Çözünürlük ve Çözünme Hızı: İki Farklı Kavram
Öğrenciler tarafından sıkça karıştırılan bu iki kavramın farkını anlamak kimya sorularında hata yapmanızı engeller:
Çözünürlük Nedir? (Kapasite)
Belirli bir sıcaklık ve basınçta, 100 gram çözücüde çözünebilen maksimum madde miktarıdır. “Benzer benzeri çözer” ilkesiyle belirlenir. Sıcaklık ve basınç (gazlar için) çözünürlüğü değiştirir.
Çözünme Hızı Nedir? (Sürat)
Birim zamanda çözünen madde miktarıdır. Bir maddenin çözünürlüğü yüksek olsa bile çözünme hızı yavaş olabilir. Çözünme hızını artırmak için:
- Sıcaklık: Genellikle hem hızı hem kapasiteyi artırır.
- Karıştırma: Çözünürlüğü değiştirmez ama çözünme hızını artırır.
- Temas Yüzeyi (Tanecik Boyutu): Maddeyi toz haline getirmek çözünme hızını artırır (Örn: Pudra şekerinin küp şekerden hızlı çözünmesi).
Hesaplamalar hakkında detaylı bilgi için: Molarite ve molalite hesaplama yöntemleri
Günlük Hayattan Çözelti Örnekleri
- Hava: %78 azot ve %21 oksijen içeren bir gaz çözeltisidir.
- Deniz Suyu: Su içerisinde çeşitli tuzların ve oksijenin çözünmesiyle oluşur.
- Madeni Paralar: Farklı metallerin homojen karışımı olan alaşımlardır.
- Göz Damlası: Steril su içerisinde belirli oranlarda ilaç içeren sıvı çözeltidir.
Sıkça Sorulan Sorular (SSS)
Her karışım bir çözelti midir?
Hayır. Sadece homojen olan karışımlar çözeltidir. Örneğin çamurlu su veya zeytinyağı-su karışımı heterojendir ve çözelti değildir.
Karıştırmak çözünürlüğü artırır mı?
Hayır. Karıştırmak sadece çözünme hızını artırır. Bir bardak suda çözünebilecek maksimum şeker miktarını karıştırarak değiştiremezsiniz; sadece şekerin daha çabuk çözünmesini sağlarsınız.
Gazların çözünürlüğü sıcaklıkla nasıl değişir?
Katıların aksine, gazların çözünürlüğü sıcaklık arttıkça azalır. Isınan denizlerde balıkların yüzeye yakın gelmesinin veya soğuk içeceklerin daha fazla asit (gaz) tutmasının nedeni budur.
Alaşım nedir?
En az biri metal olmak üzere iki veya daha fazla maddenin eritilerek karıştırılmasıyla oluşan katı-katı çözeltilerdir.
Sonuç
Çözeltiler, kimyanın ve günlük hayatın ayrılmaz bir parçasıdır. Soluduğumuz havadan içtiğimiz suya kadar pek çok yapı çözelti formundadır. Bir karışımın çözelti olup olmadığını anlamak için homojenlik ve tanecik boyutu kriterlerine bakmak gerekir. Çözünürlük (kapasite) ile çözünme hızı (sürat) arasındaki farkı kavramak, hem akademik başarı hem de endüstriyel süreçleri anlamak için temel bir adımdır.
Konuyla ilgili daha derinlemesine bilgi için Maddeler arası etkileşimler ve kimyasal bağlar içeriğimize göz atabilirsiniz.
