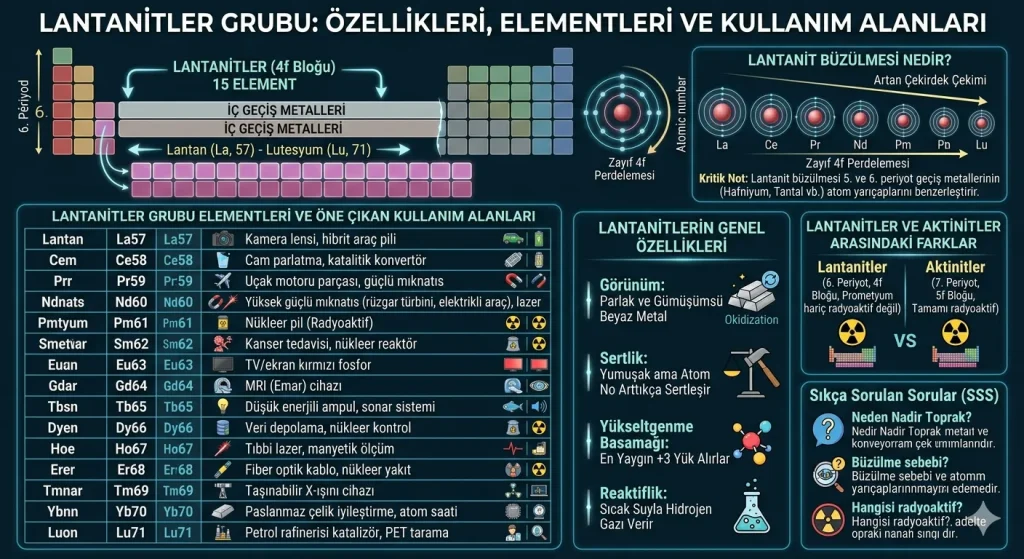
Lantanitler, periyodik tablonun 6. periyodunda yer alan, atom numarası 57 (Lantan) ile 71 (Lutesyum) arasında değişen 15 elementlik özel bir seridir. Kimya literatüründe “iç geçiş metalleri” olarak tanımlanan bu grup, elektron dizilimlerinin 4f orbitalleriyle sonlanması nedeniyle 4f bloğu elementleri olarak da adlandırılır. Günümüzde akıllı telefonlardan yenilenebilir enerji teknolojilerine kadar pek çok stratejik alanda kritik rol oynarlar.
Kısa Özet: Lantanitler; gümüşümsü beyaz renkte, yumuşak ve kimyasal olarak birbirine çok benzeyen metallerdir. Doğada genellikle bir arada bulundukları ve ayrıştırılmaları zor olduğu için “nadir toprak elementleri” olarak bilinirler.
Lantanitlerin Periyodik Tablodaki Yeri
Periyodik tabloya bakıldığında, ana gövdenin altında yer alan iki yatay sıradan üstteki lantanitlere aittir. Aslında bu elementler, 6. periyotta 3B grubunun bir parçasıdır. Ancak tablonun yatayda aşırı uzamasını engellemek ve görsel düzeni korumak amacıyla alt kısma taşınmışlardır. Tamamı metalik karakter gösteren bu elementler, periyodik tablo özellikleri açısından benzer reaktiflik seviyelerine sahiptir.
Lantanitler Grubu Elementleri Listesi
Lantanitler grubunda yer alan 15 elementin atom numaraları, sembolleri ve öne çıkan kullanım alanları aşağıdaki tabloda özetlenmiştir:
| Element Adı | Sembol | Atom No | Öne Çıkan Kullanım Alanı |
|---|---|---|---|
| Lantan | La | 57 | Kamera lensleri, hibrit araç pilleri |
| Seryum | Ce | 58 | Cam parlatma, katalitik konvertörler |
| Praseodimyum | Pr | 59 | Uçak motorları, güçlü mıknatıslar |
| Neodimyum | Nd | 60 | Yüksek güçlü mıknatıslar, lazerler |
| Prometyum | Pm | 61 | Nükleer piller (Radyoaktiftir) |
| Samaryum | Sm | 62 | Kanser tedavisi, nükleer reaktörler |
| Europiyum | Eu | 63 | TV ve ekranlardaki kırmızı fosforlar |
| Gadolinyum | Gd | 64 | MRI (Emar) görüntüleme cihazları |
| Terbiyum | Tb | 65 | Düşük enerjili ampuller, sonar sistemleri |
| Disprozyum | Dy | 66 | Veri depolama cihazları, nükleer kontrol |
| Holmiyum | Ho | 67 | Tıbbi lazerler, manyetik alan ölçümü |
| Erbiyum | Er | 68 | Fiber optik kablolar, nükleer yakıt |
| Tulyum | Tm | 69 | Taşınabilir X-ışını cihazları |
| İtterbiyum | Yb | 70 | Paslanmaz çelik iyileştirme, atom saatleri |
| Lutesyum | Lu | 71 | Petrol rafinerileri, PET taramaları |
Lantanitlerin Genel Özellikleri
Lantanitler, iç kabuklarındaki 4f orbitallerinin dolması nedeniyle birbirlerine çok yakın kimyasal davranışlar sergilerler. Bu benzerlik, onları doğada birbirinden ayırmayı en zor element gruplarından biri yapar.
Fiziksel ve Kimyasal Karakteristikler
- Görünüm: Parlak ve gümüşümsü beyaz metallerdir. Havayla temas ettiklerinde hızla oksitlenerek matlaşırlar.
- Sertlik: Genellikle yumuşaktırlar; ancak atom numarası arttıkça (Lantan’dan Lutesyum’a doğru) sertlikleri artar.
- Yükseltgenme Basamağı: Bileşiklerinde en kararlı ve yaygın olarak +3 yükseltgenme basamağını alırlar.
- Reaktiflik: Kimyasal olarak oldukça aktiftirler. Sıcak suyla tepkimeye girerek hidrojen gazı açığa çıkarırlar.
Lantanit Büzülmesi Nedir?
Lantanitler grubunda atom numarası arttıkça atom ve iyon yarıçapının beklenmedik şekilde küçülmesi olayına lantanit büzülmesi denir. Normal şartlarda periyodik tabloda atom numarası arttıkça yarıçapın artması beklenirken, lantanitlerde durum tam tersidir.
Bunun temel nedeni, 4f orbitallerindeki elektronların çekirdek yükünü yeterince perdeleyememesidir. Artan çekirdek yükü, dış elektronları daha güçlü çeker ve atom hacminin küçülmesine yol açar.
Lantanitlerin Kullanım Alanları
Lantanitler, modern endüstride “teknolojinin vitaminleri” olarak tanımlanır. Çok küçük miktarlarda eklendikleri malzemelerin özelliklerini kökten değiştirirler:
- Güçlü Mıknatıslar: Neodimyum mıknatıslar, günümüzde rüzgar türbinlerinden elektrikli araç motorlarına kadar her yerde kullanılır.
- Ekran Teknolojisi: Akıllı telefon ve televizyon ekranlarındaki canlı renkler, Europiyum ve Terbiyum gibi elementlerin fosfor özelliklerinden gelir.
- Savunma ve Havacılık: Gece görüş dürbünleri, lazer güdümlü füzeler ve uçak motoru parçalarında lantanit alaşımları tercih edilir.
- Enerji: Seryum, petrolün rafine edilmesinde katalizör olarak kullanılırken; nükleer reaktörlerde nötron emici olarak farklı lantanitlerden faydalanılır.
Lantanitler ve Aktinitler Arasındaki Farklar
Periyodik tablonun altındaki iki satır sıklıkla karıştırılsa da aralarında belirgin farklar vardır:
- Lantanitler: 6. periyottadır, 4f bloğundadır. Prometyum hariç radyoaktif değillerdir.
- Aktinitler: 7. periyottadır, 5f bloğundadır. Tamamı radyoaktiftir. Detaylı bilgi için aktinitler grubu rehberimizi inceleyebilirsiniz.
Sıkça Sorulan Sorular (SSS)
1. Lantanitler neden nadir toprak elementi olarak adlandırılır?
Bu isim tarihsel bir yanılgıdan kaynaklanır. Aslında yerkabuğunda gümüşten daha bol bulunurlar. Ancak saf halde ayrıştırılmaları teknolojik olarak zor ve maliyetli olduğu için bu isim verilmiştir.
2. Lantanit büzülmesinin temel sebebi nedir?
4f orbitallerinin zayıf perdeleme etkisi nedeniyle artan çekirdek çekim gücünün, elektron bulutunu merkeze doğru daha fazla çekmesidir.
3. Hangi lantanit elementi radyoaktiftir?
Lantanitler serisi içinde doğal olarak kararlı izotopu bulunmayan ve radyoaktif olan tek element Prometyum (Pm) elementidir.
Sonuç
Lantanitler grubu, hem akademik kimya eğitiminde hem de ileri teknoloji üretiminde vazgeçilmez bir yere sahiptir. Lantanit büzülmesi gibi kavramlar, periyodik tablodaki atomik değişimleri anlamak için temel teşkil eder. Bu elementler; enerji, tıp ve iletişim sektörlerindeki rolleriyle modern dünyanın gizli kahramanlarıdır. Kimya sınavlarında başarılı olmak için bu grubun +3 değerlikli yapısını ve geçiş metalleri ile olan farklarını iyi kavramak gerekir.
