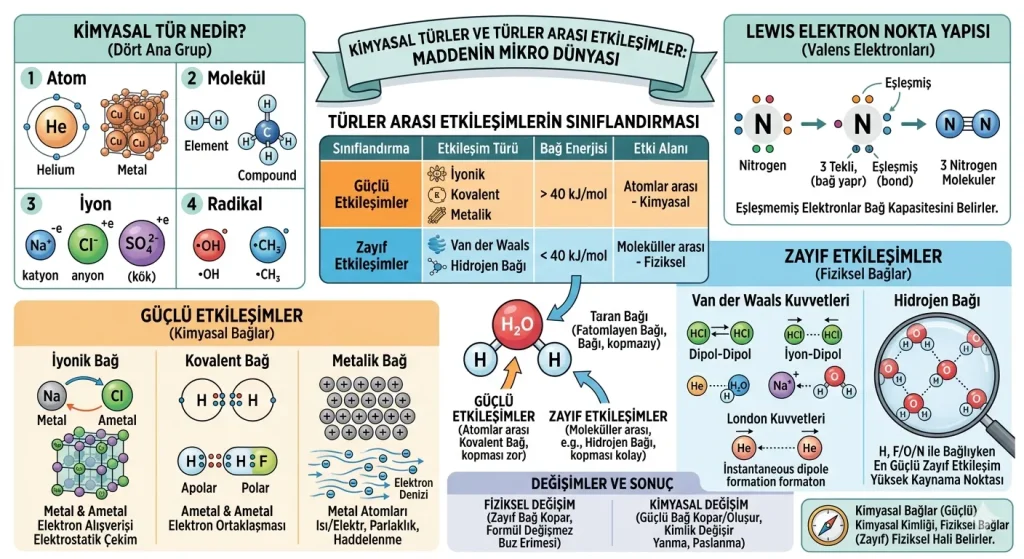
Özet: Kimyasal türler; atom, molekül, iyon ve radikal olmak üzere dört ana grupta incelenir. Bu türlerin birbirleriyle etkileşimi, bağın kopması için gereken enerjiye göre “Güçlü Etkileşimler” (Kimyasal Bağlar) ve “Zayıf Etkileşimler” (Fiziksel Bağlar) olarak ikiye ayrılır. Maddenin kimyasal kimliğini güçlü etkileşimler, fiziksel halini ise zayıf etkileşimler belirler.
Kimya biliminde maddenin yapısını ve değişimlerini anlamak için öncelikle maddeyi oluşturan temel birimleri tanımak gerekir. Kimyasal türler ve türler arası etkileşimler konusu, hem TYT Kimya müfredatının temelini oluşturur hem de maddelerin neden farklı fiziksel ve kimyasal özelliklere sahip olduğunu açıklar. Bu içeriğimizde, atomların nasıl bağ kurduğundan moleküller arası çekim kuvvetlerine kadar tüm detayları inceleyeceğiz.
Kimyasal Tür Nedir?
Maddenin bağımsız olarak var olabilen en küçük birimlerine kimyasal tür denir. Kimyasal türleri dört temel başlıkta sınıflandırırız:
- Atom: Bir elementin tüm özelliklerini taşıyan en küçük yapı taşıdır. Soy gazlar (He, Ne) ve metaller (Fe, Cu) doğada atomik yapıda bulunabilir.
- Molekül: En az iki atomun kovalent bağlarla bir arada tutulmasıyla oluşan bağımsız gruplardır. Element molekülü (H2, O2) veya bileşik molekülü (H2O, CH4) olabilirler.
- İyon: Elektron almış (anyon: Cl–) veya vermiş (katyon: Na+) atom ya da atom gruplarıdır. Çok atomlu iyonlara (SO42-) “kök” denir.
- Radikal: Üzerinde eşleşmemiş elektron bulunduran, yüksek enerjili ve çok tepkisel (reaktif) türlerdir (•OH, •CH3).
Lewis Elektron Nokta Yapısı
Atomların bağ yapma kapasitelerini ve son katmanlarındaki elektronları anlamak için Lewis sembolleri kullanılır. Bir atomun sembolü etrafına, değerlik elektron sayısı kadar nokta konulur. Noktalar önce dört köşeye birer birer yerleştirilir, elektron sayısı 4’ten fazlaysa eşleştirilmeye başlanır.
Önemli: Lewis yapısındaki eşleşmemiş (tekli) elektron sayısı, bir atomun yapabileceği bağ sayısını belirler. Örneğin, Azot (7N) 5 değerlik elektronuna sahiptir ve Lewis yapısında 3 tane tekli elektronu bulunduğu için 3 bağ yapar.
Türler Arası Etkileşimlerin Sınıflandırılması
Kimyasal türler birbirine yaklaştığında protonlar ve elektronlar arasında itme-çekme kuvvetleri oluşur. Çekme kuvvetlerinin itme kuvvetlerinden çok daha baskın olduğu durumlarda bağ oluşur. Etkileşimler, bağın gücüne göre ikiye ayrılır:
| Sınıflandırma | Etkileşim Türü | Bağ Enerjisi | Etki Alanı |
|---|---|---|---|
| Güçlü Etkileşimler | İyonik, Kovalent, Metalik | Genellikle > 40 kJ/mol | Atomlar arası (Kimyasal) |
| Zayıf Etkileşimler | Van der Waals, Hidrojen Bağı | Genellikle < 40 kJ/mol | Moleküller arası (Fiziksel) |
Not: 40 kJ/mol değeri kesin bir sınır değildir. Örneğin suyun buharlaşması için gereken enerji 43,9 kJ/mol olsa da, bu olay fiziksel bir değişimdir ve zayıf etkileşimlerle ilgilidir.
Güçlü Etkileşimler (Kimyasal Bağlar)
Atomları bir arada tutarak yeni maddelerin oluşmasını sağlayan bağlardır. Bu bağlar koptuğunda maddenin kimyasal yapısı değişir.
1. İyonik Bağ
Metal ve ametal atomları arasında elektron alışverişi ile oluşur. Zıt yüklü iyonların birbirini elektrostatik çekim kuvvetiyle çekmesi sonucunda meydana gelir. İyonik bileşikler oda koşullarında katı haldedir ve kristal örgü yapısına sahiptir.
2. Kovalent Bağ
Ametal atomları arasında elektronların ortaklaşa kullanılmasıyla oluşur. Elektronegatiflik farkına göre ikiye ayrılır:
- Apolar Kovalent Bağ: Aynı tür ametaller arasında (H-H, Cl-Cl).
- Polar Kovalent Bağ: Farklı tür ametaller arasında (H-F, H2O).
3. Metalik Bağ
Metal atomlarını bir arada tutan kuvvettir. Metal atomlarının değerlik elektronlarının oluşturduğu “elektron denizi” ile pozitif metal iyonları arasındaki çekimdir. Metalik bağ sayesinde metaller;
- Isı ve elektriği iyi iletir.
- Tel ve levha haline getirilebilir (haddelenebilir).
- Yüzeyleri parlaktır.
Zayıf Etkileşimler (Fiziksel Bağlar)
Maddenin katı, sıvı veya gaz halinde bulunmasını belirleyen etkileşimlerdir. Maddenin halleri arasındaki geçişler bu bağların gücüyle doğrudan ilişkilidir.
Van der Waals Kuvvetleri
- Dipol-Dipol: Polar moleküller arasındaki çekimdir (HCl-HCl).
- İyon-Dipol: Bir iyon ile polar bir molekül arasındaki çekimdir (Na+ – H2O).
- London Kuvvetleri: Apolar moleküller ve soy gazlarda görülen anlık polarlanmadır. Kritik Not: Toplam elektron sayısı arttıkça polarlanabilirlik artar, bu da London kuvvetlerini ve dolayısıyla kaynama noktasını yükseltir.
Hidrojen Bağı
Hidrojenin, elektronegatifliği çok yüksek olan F, O, N atomlarına bağlı olduğu moleküller arasında görülür. Zayıf etkileşimlerin en güçlüsüdür. Suyun (H2O) yüksek kaynama noktası bu bağ sayesindedir.
Fiziksel ve Kimyasal Değişimler
Türler arası etkileşimleri anlamak, değişimleri sınıflandırmayı kolaylaştırır:
- Fiziksel Değişim: Sadece zayıf etkileşimler kopar veya oluşur. Maddenin formülü değişmez (Buzun erimesi, şekerin suda çözünmesi).
- Kimyasal Değişim: Güçlü etkileşimler kopar ve yeni bağlar oluşur. Maddenin kimliği değişir (Yanma, paslanma, elektroliz).
Sıkça Sorulan Sorular
1. Kimyasal türler kaça ayrılır?
Temel olarak atom, molekül, iyon ve radikal olmak üzere dört gruba ayrılır.
2. En güçlü zayıf etkileşim hangisidir?
Genellikle hidrojen bağı, Van der Waals kuvvetlerinden daha güçlüdür.
3. London kuvvetleri her molekülde bulunur mu?
Evet, London kuvvetleri tüm atom ve moleküllerde bulunur; ancak apolar moleküllerde ve soy gazlarda etkin olan tek kuvvettir.
4. Lewis yapısında noktalar neyi temsil eder?
Atomun en dış katmanında bulunan değerlik elektronlarını temsil eder.
Sonuç
Kimyasal türler ve türler arası etkileşimler, maddenin mikro dünyasını anlamamızı sağlayan bir haritadır. Atomları bir arada tutan güçlü bağlar kimyasal özellikleri belirlerken; molekülleri bir arada tutan zayıf bağlar maddenin fiziksel halini belirler.
