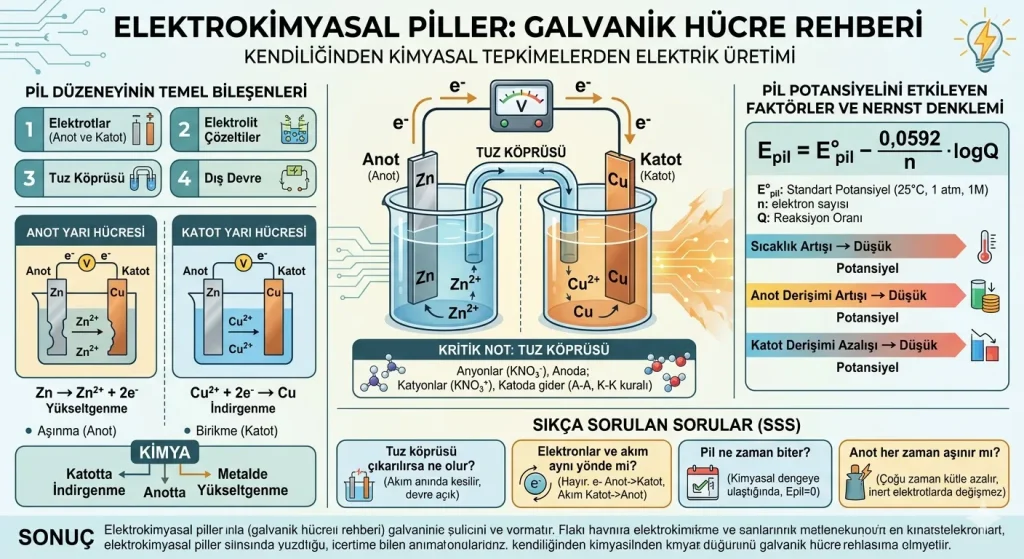
Özet: Elektrokimyasal piller (galvanik hücreler), kendiliğinden gerçekleşen kimyasal tepkimelerden elektrik enerjisi üreten sistemlerdir. Bu düzenekler; yükseltgenmenin olduğu anot, indirgenmenin olduğu katot, iyon iletimini sağlayan elektrolitler ve yük dengesini koruyan tuz köprüsü olmak üzere dört temel bileşenden oluşur.
Elektrokimyasal piller, modern teknolojideki batarya sistemlerinin temelini oluşturur. Bu sistemlerin çalışma prensibi, elektronların bir maddeden diğerine aktarıldığı redoks (yükseltgenme-indirgenme) tepkimelerine dayanır. Kimyasal bağlardaki enerji, kontrollü bir şekilde dış devreye aktarılarak elektrik akımı elde edilir. Bir pilin sürekliliği, iki yarı hücre arasındaki potansiyel farkın korunmasına bağlıdır.
Elektrokimyasal Pil (Galvanik Hücre) Nedir?
Elektrokimyasal piller, diğer adıyla galvanik veya voltaik hücreler, kimyasal enerjiyi elektrik enerjisine dönüştürür. Bu süreçte aktifliği farklı iki metal (elektrot) kullanılır. Metaller arasındaki aktiflik farkı, elektronların aktif olan metalden pasif olana doğru akmasını sağlayan bir “itici güç” yani potansiyel farkı yaratır.
Sistemin sağlıklı çalışabilmesi için Metalik Aktiflik ve Yükseltgenme Basamakları prensiplerinin doğru analiz edilmesi gerekir. Bu prensipler, hangi elektrodun aşınacağını, hangisinin kütle kazanacağını belirler.
Pil Düzeneğinin Temel Bileşenleri
Standart bir pil düzeneği, devrenin tamamlanması ve enerji üretimi için şu bileşenlere ihtiyaç duyar:
1. Elektrotlar (Anot ve Katot)
Tepkimenin gerçekleştiği metal çubuklardır:
- Anot: Elektronların verildiği (yükseltgenme) bölgedir.
- Katot: Elektronların alındığı (indirgenme) bölgedir.
2. Elektrolit Çözeltiler
İçerisinde serbest iyonlar bulunduran ve elektrik iletimini sağlayan sıvılardır. Genellikle elektrot olarak kullanılan metalin kendi tuz çözeltisi tercih edilir.
3. Tuz Köprüsü
İki yarı hücreyi birbirine bağlayan ve iyon dengesini sağlayan kritik bir parçadır. İçinde genellikle potasyum nitrat (KNO3) gibi doygun tuz çözeltileri bulunur.
Kritik Not: Tuz köprüsündeki Anyonlar Anoda, Katyonlar Katoda gider (A-A, K-K kuralı). Bu hareket olmazsa yük birikmesi nedeniyle pil saniyeler içinde durur.
4. Dış Devre (İletken Tel ve Voltmetre)
Elektronların anottan katoda akmasını sağlayan yoldur. Voltmetre, bu akış sırasında oluşan gerilimi (pil potansiyelini) ölçer.
Anot ve Katot Arasındaki Farklar
Anot ve katodu ayırt etmek için “KİMYA” (Katotta İndirgenme, Metalde Yükseltgenme Anotta) kodlaması kullanılır. Aşağıdaki tablo temel farkları özetlemektedir:
| Özellik | Anot Yarı Hücresi | Katot Yarı Hücresi |
|---|---|---|
| Reaksiyon Türü | Yükseltgenme (Ox) | İndirgenme (Red) |
| Elektrot Kütlesi | Genellikle azalır (Aşınma) | Genellikle artar (Birikme) |
| Çözelti Derişimi | Artar (İyon oluşumu) | Azalır (İyonların metale dönüşümü) |
| Elektron Yönü | Elektronların çıkış noktası | Elektronların varış noktası |
| İşaret | Negatif (-) uç | Pozitif (+) uç |
Hesaplamalarda hata yapmamak için Standart Elektrot Potansiyelleri tablosundaki değerler baz alınmalıdır.
Pil Potansiyelini Etkileyen Faktörler ve Nernst Denklemi
Bir pilin ürettiği gerilim her zaman sabit değildir. Standart şartlar (25°C sıcaklık, 1 atm basınç ve 1M derişim) değiştiğinde pil potansiyeli de değişir. Bu durumu açıklayan en temel yapı Nernst Denklemi‘dir:
Epil = E°pil – (0,0592 / n) * logQ
- Sıcaklık: Pil tepkimeleri genellikle ekzotermiktir. Sıcaklık artışı pil potansiyelini düşürür.
- Derişim: Anot çözeltisinin derişimi artarsa veya katot çözeltisinin derişimi azalırsa pil potansiyeli düşer.
- Basınç: Eğer tepkimede gaz fazında bir madde varsa basınç değişimi potansiyeli etkiler.
Elektrokimyasal Pil Nasıl Çalışır?
Sistem devreye alındığında olaylar şu sırayla gerçekleşir:
- Aktif metal (anot) atomları elektron vererek iyonlaşır ve çözeltiye geçer.
- Açığa çıkan elektronlar dış devre (tel) üzerinden katoda ulaşır.
- Katot çözeltisindeki katyonlar, gelen elektronları alarak indirgenir ve elektrot üzerinde toplanır.
- Tuz köprüsü, bozulan yük dengesini iyon transferiyle yeniden kurar.
- Bu süreç, elektrot bitene veya sistem dengeye ulaşana kadar sürer.
Sıkça Sorulan Sorular
Tuz köprüsü çıkarılırsa ne olur?
Tuz köprüsü devreyi tamamlar. Çıkarıldığı anda iyon dengesi sağlanamaz, devre açık hale gelir ve elektrik akımı anında kesilir.
Elektronlar ve akım aynı yönde mi hareket eder?
Hayır. Fiziksel olarak elektronlar anottan katoda akar. Ancak geleneksel elektrik akım yönü, elektronların tersi yönünde yani katottan anoda kabul edilir.
Pil ne zaman biter?
Pil tepkimesi kimyasal dengeye ulaştığında (Epil = 0) potansiyel farkı sıfırlanır ve pil akım üretmeyi durdurur.
Anot her zaman aşınır mı?
Çoğu standart pilde anot kütlesi azalır. Ancak inert (tepkimeye girmeyen) elektrotların kullanıldığı bazı özel düzeneklerde elektrot kütlesi değişmeyebilir.
Sonuç
Elektrokimyasal piller, kimyasal enerjinin kontrollü bir redoks tepkimesiyle elektrik enerjisine dönüştürülmesidir. Başarılı bir analiz için anotta yükseltgenme, katotta indirgenme olduğunu bilmek ve tuz köprüsünün iyon dengesi görevini kavramak esastır. Nernst denklemi gibi faktörler ise pilin gerçek dünya koşullarındaki performansını anlamamızı sağlar. Sınav hazırlığında “KİMYA” kodlamasını unutmamak, soru çözüm hızınızı önemli ölçüde artıracaktır.
