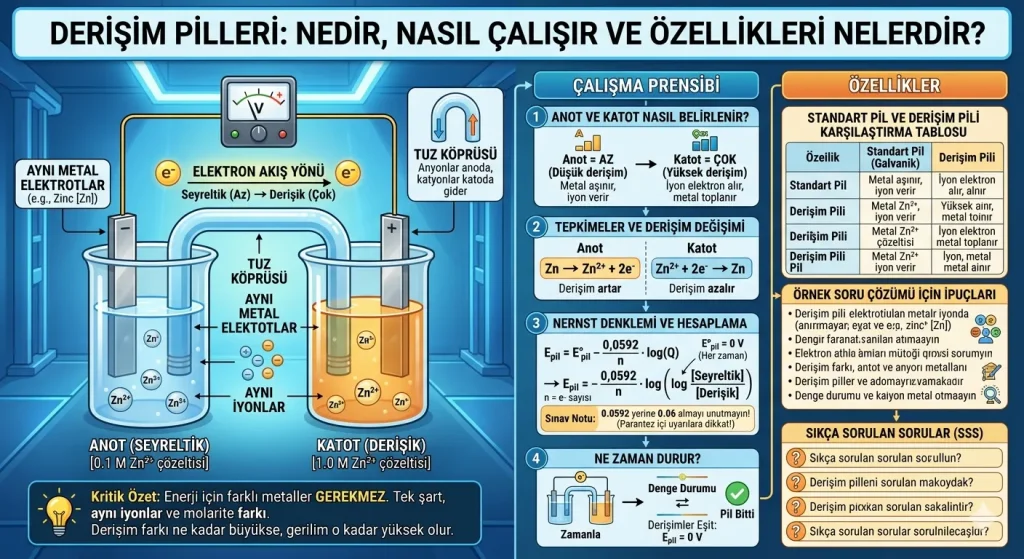
Derişim pili; aynı metalden yapılmış elektrotların, aynı metal iyonlarını içeren ancak derişimleri farklı olan iki ayrı çözeltiye daldırılmasıyla oluşan elektrokimyasal bir sistemdir. Bu pillerde elektrik akımı, iki çözelti arasındaki derişim farkından kaynaklanır. Derişimler birbirine eşitlendiğinde sistem dengeye ulaşır ve pil çalışmayı durdurur.
Kritik Özet: Derişim pillerinde enerji üretimi için farklı metallere (aktiflik farkına) ihtiyaç duyulmaz. Tek şart, aynı iyonların bulunduğu iki bölme arasında molarite farkı olmasıdır. Derişim farkı ne kadar büyükse, pilin üreteceği gerilim o kadar yüksek olur.
Derişim Pillerinin Çalışma Prensibi
Derişim pillerinin temel çalışma mantığı, doğadaki denge kurma eğilimidir. Sistem, iki bölme arasındaki derişim farkını ortadan kaldırmak için hareket eder. Bu süreçte gerçekleşen yükseltgenme ve indirgenme tepkimeleri sonucunda dış devreden elektron akışı başlar.
Anot ve Katot Nasıl Belirlenir?
Derişim pillerinde anot ve katodu belirlemek için sadece çözeltilerin derişim miktarına bakılır. Elektrokimyasal pil düzenekleri içindeki temel kurallar burada da geçerlidir ancak şu pratik kodlama işinizi kolaylaştıracaktır:
- Anot = AZ: İyon derişimi düşük (az) olan bölmedir. Bu bölmede metal aşınarak çözeltiye iyon verir ve derişim artmaya başlar.
- Katot = ÇOK: İyon derişimi yüksek (fazla) olan bölmedir. Bu bölmede çözeltideki iyonlar elektron alarak metal üzerinde toplanır ve derişim azalmaya başlar.
Elektron Akış Yönü
Tüm pillerde olduğu gibi elektronlar her zaman anottan katoda doğru hareket eder. Derişim pilleri özelinde bu durum, elektronların derişimi az olan (seyreltik) kaptan, derişimi fazla olan (derişik) kaba doğru akması anlamına gelir.
Nernst Denklemi ve Derişim Pilleri
Derişim pillerinde her iki elektrot da aynı maddeden yapıldığı için standart pil potansiyeli (E°pil) her zaman 0 (sıfır) kabul edilir. Çünkü her iki yarı hücrenin standart indirgenme potansiyelleri birbirinin aynısıdır.
Pilin anlık gerilimini hesaplamak için Nernst denklemi formülü kullanılır:
Epil = E°pil – (0,0592 / n) * log(Q)
Derişim pilleri için bu formül şu şekilde sadeleşir:
Epil = – (0,0592 / n) * log([Seyreltik] / [Derişik])
Sınav Notu: Sorularda genellikle işlem kolaylığı sağlaması açısından 0,0592 sabiti yerine 0,06 alınması istenir. Sorunun altındaki parantez içi uyarılara mutlaka dikkat edin.
Derişim Pili Ne Zaman Durur?
Pil çalıştığı sürece anottaki derişim artar, katottaki derişim ise azalır. Zamanla bu iki değer birbirine yaklaşır. Her iki kaptaki iyon derişimleri eşitlendiğinde potansiyel fark (Epil) sıfır olur ve pil akım üretmeyi durdurur. Bu durum sistemin kimyasal dengeye ulaştığını ve pilin “bittiğini” gösterir.
Standart Pil ve Derişim Pili Arasındaki Farklar
Aşağıdaki tablo, galvanik hücreler ile derişim pilleri arasındaki temel farkları özetlemektedir:
| Özellik | Standart Pil (Galvanik) | Derişim Pili |
|---|---|---|
| Elektrotlar | Genellikle farklı metaller | Aynı metaller |
| Çözeltiler | Farklı iyonlar içerebilir | Aynı iyonlar |
| Gerilim Kaynağı | Metallerin aktiflik farkı | Çözeltilerin derişim farkı |
| E°pil Değeri | Sıfırdan farklıdır | Her zaman sıfırdır |
Örnek Soru Çözümü İçin İpuçları
AYT Kimya ve genel kimya sınavlarında derişim pilleri ile ilgili soruları çözerken şu adımları takip edebilirsiniz:
- Önce kaplardaki molarite değerlerini karşılaştırın. Derişimi küçük olan kaba “Anot”, büyük olan kaba “Katot” yazın.
- Tuz köprüsü görevleri gereği; anyonların anoda, katyonların katoda gideceğini unutmayın.
- Nernst denkleminde E°pil yerine mutlaka 0 yazın.
- Derişim farkı ne kadar fazlaysa, pil potansiyelinin o kadar yüksek olacağını aklınızda bulundurun. Dışarıdan su ekleyerek veya buharlaştırarak derişimi değiştirmek pil gerilimini doğrudan etkiler.
Sıkça Sorulan Sorular (SSS)
Derişim pillerinde elektrotlar farklı olabilir mi?
Hayır, eğer elektrotlar farklı olursa bu bir derişim pili değil, standart bir galvanik pil olur. Derişim pilinin temel özelliği, elektrotların ve çözeltideki iyon türlerinin aynı olmasıdır.
Derişimler eşitlenince ne olur?
Derişimler eşitlendiğinde sistem kimyasal dengeye ulaşır. Potansiyel fark (voltaj) sıfırlandığı için pil durur ve elektrik üretimi kesilir.
E°pil değeri neden her zaman sıfırdır?
Çünkü E°pil, standart şartlarda (her iki çözeltinin de 1 molar olduğu durum) ölçülen değerdir. Derişim pilinde her iki bölme de 1 molar olsaydı, aralarında hiçbir fark kalmayacağı için potansiyel üretilemezdi.
Derişim pili neden enerji üretir?
Sistem, yüksek derişimli bölgedeki iyonları azaltıp düşük derişimli bölgedeki iyonları artırarak dengeye gelmek ister. Bu istemli (spontan) süreç sırasında açığa çıkan enerji elektrik akımına dönüşür.
Sonuç
Derişim pilleri, elektrokimyanın temel prensiplerini ve metalik aktiflik konusunu anlamak için kritik bir örnektir. Aktiflik farkı olmasa bile sadece derişim farkı kullanılarak elektrik üretilebileceğini kanıtlar. Sınavlarda başarılı olmak için “Anot = Az Derişim” kuralını unutmamak ve Nernst denklemindeki logaritmik oranları doğru yerleştirmek yeterlidir. Kimya derslerinde bu konu, sistemlerin dengeye ulaşma isteğinin en somut göstergelerinden biri olarak karşımıza çıkar.
