Elektrokimyasal pillerde standart pil potansiyeli (E°), çözelti derişimlerinin 1 molar (1M) ve sıcaklığın 25°C olduğu ideal durumlar için hesaplanır. Ancak gerçek dünya uygulamalarında ve laboratuvar deneylerinde derişimler genellikle 1M’den farklıdır. Nernst denklemi, derişimlerin standart değerlerden saptığı durumlarda pil potansiyelinin (voltajın) ne olacağını hesaplamamızı sağlayan en temel kimya formülüdür.
Nernst Denklemi Nedir? (Kısa Özet)
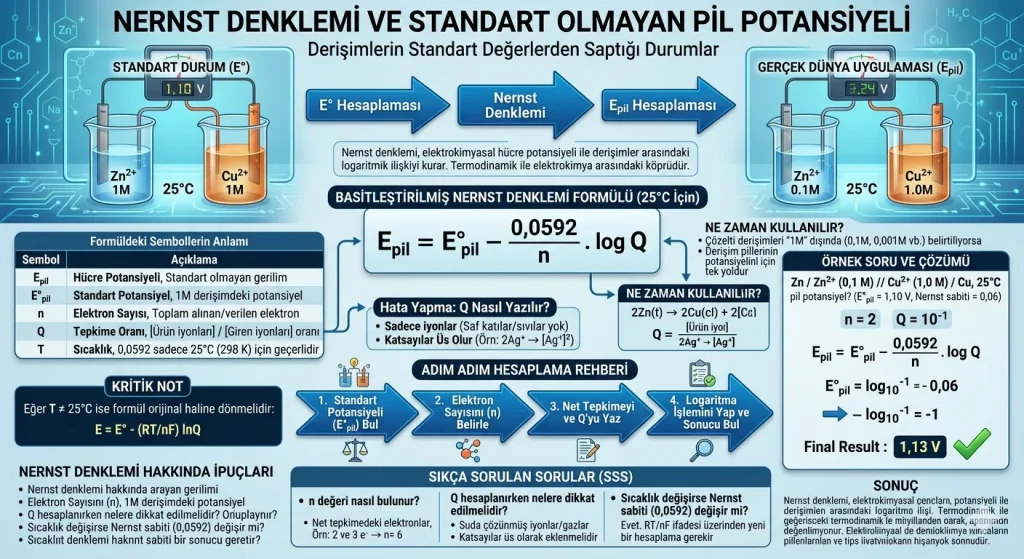
Nernst denklemi, bir elektrokimyasal hücrenin potansiyeli ile tepkimeye giren maddelerin derişimleri arasındaki logaritmik ilişkiyi kurar. Özetle; anot veya katot bölmesindeki iyon derişimi değiştiğinde, pilin ürettiği gerilimin ne kadar artacağını veya azalacağını bu denklemle buluruz. Bu denklem, termodinamik ile elektrokimya arasındaki köprüdür.
Nernst Denklemi Formülü ve Bileşenleri
Çoğu kimya probleminde ve sınav sorusunda, 25°C (298 K) sıcaklık için basitleştirilmiş Nernst denklemi kullanılır:
Epil = E°pil – (0,0592 / n) . log Q
Formüldeki Sembollerin Anlamı
Denklemi hatasız uygulamak için değişkenlerin temsil ettiği değerleri doğru tanımlamak gerekir:
| Sembol | Anlamı | Açıklama |
|---|---|---|
| Epil | Hücre Potansiyeli | Mevcut (standart olmayan) koşullardaki pil gerilimi. |
| E°pil | Standart Potansiyel | Çözeltilerin 1M olduğu durumdaki potansiyel. |
| n | Elektron Sayısı | Denkleştirilmiş redoks tepkimesinde alınan/verilen toplam elektron. |
| Q | Tepkime Oranı | [Ürün iyonları] / [Giren iyonları] oranı. |
| T | Sıcaklık | Formüldeki 0,0592 sabiti yalnızca 25°C (298 K) için geçerlidir. |
KRİTİK NOT: Eğer sıcaklık 25°C’den farklıysa, 0,0592 sabiti kullanılamaz. Bu durumda formülün orijinal hali olan E = E° – (RT/nF) lnQ yapısına dönülmelidir. Burada R ideal gaz sabiti, T mutlak sıcaklık (Kelvin) ve F Faraday sabitidir.
Hata Yapma: Q (Tepkime Oranı) Nasıl Yazılır?
Öğrencilerin Nernst denkleminde en çok hata yaptığı nokta Q değerini hesaplamaktır. Q hesaplanırken şu iki kural asla unutulmamalıdır:
- Sadece iyonlar: Saf katılar ve sıvılar denkleme dahil edilmez.
- Katsayılar Üs Olur: Tepkime denklemindeki iyonların başındaki katsayılar, derişimlerin üzerine üs olarak yazılmalıdır. Örneğin; 2Ag+ iyonu varsa, payda kısmına [Ag+]2 yazılır.
Nernst Denklemi Ne Zaman Kullanılır?
Eğer bir soruda pil düzeneği veriliyor ve çözelti derişimleri “1M” dışında (örneğin 0,1M veya 0,001M) belirtiliyorsa, orada mutlaka Nernst denklemi uygulanmalıdır. Ayrıca elektrotları aynı ancak derişimleri farklı olan derişim pilleri potansiyelini hesaplamak için de bu formül tek yoldur.
Adım Adım Hesaplama Rehberi
- Standart Potansiyeli (E°pil) Bulun: Derişimler 1M imiş gibi standart indirgenme potansiyellerini kullanarak E° değerini hesaplayın.
- Elektron Sayısını (n) Belirleyin: Alınan ve verilen elektronları eşitleyerek net tepkimeyi yazın. “n” bu eşitlenen sayıdır.
- Net Tepkimeyi ve Q’yu Yazın: Q = [Anot iyonu]katsayı / [Katot iyonu]katsayı formülünü kurun.
- Logaritma İşlemini Yapın: Q değerinin logaritmasını alarak formülde yerine koyun ve sonucu bulun.
Örnek Soru ve Çözümü
Soru: Zn / Zn2+ (0,1 M) // Cu2+ (1,0 M) / Cu pilinin 25°C’deki potansiyelini hesaplayınız. (E°pil = 1,10 V, Nernst sabitini 0,06 alınız.)
Çözüm:
- n değeri: Zn → Zn2+ + 2e⁻ ve Cu2+ + 2e⁻ → Cu tepkimelerinden n = 2 bulunur.
- Q değeri: Net tepkime: Zn(k) + Cu2+(suda) → Zn2+(suda) + Cu(k).
Q = [Zn2+] / [Cu2+] = 0,1 / 1,0 = 10-1 - Denklem Kurulumu:
Epil = 1,10 – (0,06 / 2) . log(10-1) - Matematiksel İşlem:
log(10-1) = -1
Epil = 1,10 – (0,03 . -1)
Epil = 1,10 + 0,03 - Sonuç: 1,13 V
Nernst Denklemi Hakkında İpuçları
- Anot derişimi azalırsa veya katot derişimi artarsa pil potansiyeli artar.
- Pil dengeye ulaştığında (pil bittiğinde) Epil = 0 olur.
- Denge anında Q değeri, denge sabiti olan Kc‘ye eşit olur.
- Derişim pillerinde E°pil her zaman sıfırdır; voltajı sadece Nernst denklemindeki derişim farkı oluşturur.
Sıkça Sorulan Sorular (SSS)
Nernst denkleminde n değeri nasıl bulunur?
n değeri, anot ve katot yarı tepkimeleri denkleştirildiğinde alınan-verilen toplam elektron sayısıdır. Örneğin, bir tarafta 2, diğer tarafta 3 elektron varsa, en küçük ortak kat olan 6 değeri “n” olarak alınır.
Q (tepkime oranı) hesaplanırken nelere dikkat edilmelidir?
Sadece suda çözünmüş iyonlar ve gazlar Q’ya dahil edilir. Saf metaller (elektrotlar) yazılmaz. İyonların önündeki katsayılar mutlaka derişim değerine üs olarak eklenmelidir.
Sıcaklık değişirse Nernst sabiti (0,0592) değişir mi?
Evet, değişir. 0,0592 değeri oda sıcaklığı (25°C) için hesaplanmış bir sabittir. Farklı sıcaklıklarda (RT/nF) ifadesi üzerinden yeni bir hesaplama yapılması gerekir.
Sonuç
Nernst denklemi, elektrokimyanın en pratik ve sınavda en çok karşımıza çıkan konularından biridir. Standart olmayan koşullarda pilin voltajını belirlemek için kullanılır. Hesaplama yaparken özellikle logaritma işlemine, katsayıların üs olarak yazılmasına ve elektron sayısının (n) doğru belirlenmesine dikkat etmek hata payını minimize eder. Konuyu tam olarak kavramak için elektrokimyasal piller başlığını tekrar incelemeniz önerilir.