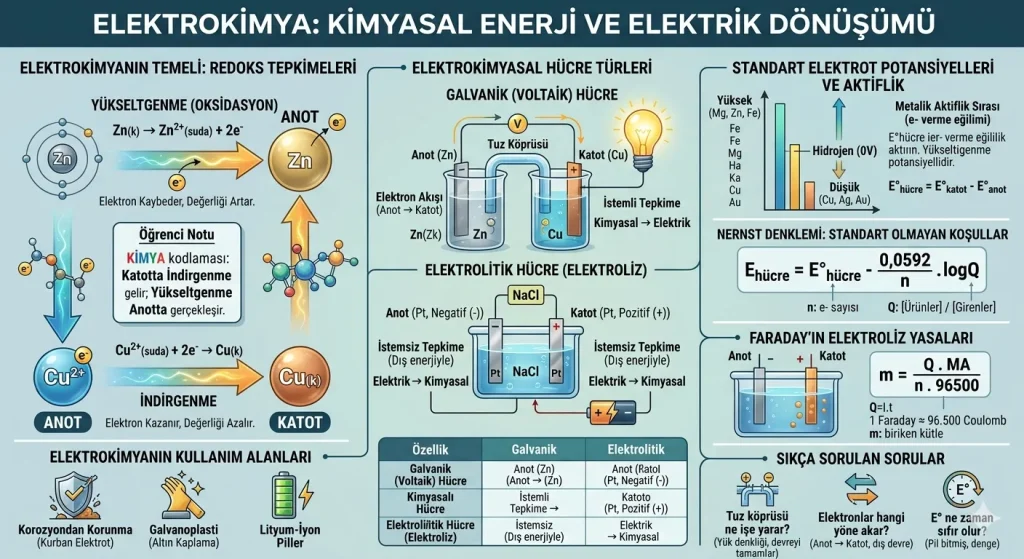
Özet: Elektrokimya; kimyasal enerjinin elektrik enerjisine dönüşümünü ve elektrik enerjisi yardımıyla kimyasal değişimlerin nasıl gerçekleştiğini inceleyen kimya alt dalıdır. Temelinde elektron alışverişine dayanan redoks tepkimeleri yer alır.
Elektrokimya, modern teknolojinin kalbinde yer alan bir disiplindir. Akıllı telefon bataryalarından otomobillerdeki akülere, metallerin korozyondan korunmasından endüstriyel kaplamacılığa kadar geniş bir yelpazeyi kapsar. Bu rehberde, lise ve AYT müfredatına uygun olarak elektrokimyanın temel taşlarını, pil düzeneklerini ve sayısal hesaplamaların mantığını öğreneceksiniz.
Elektrokimyanın Temeli: Redoks Tepkimeleri
Elektrokimyasal olayların tamamı redoks (indirgenme-yükseltgenme) süreçlerine dayanır. Bir sistemde elektrik akımından bahsedebilmemiz için elektronların bir maddeden diğerine hareket etmesi gerekir.
Yükseltgenme (Oksidasyon)
Bir atomun veya iyonun elektron kaybetmesi olayıdır. Elektron veren taneciğin yükseltgenme basamağı (değerliği) artar. Elektrokimyasal hücrelerde bu işlem her zaman anot elektrotunda gerçekleşir. Örneğin; Zn(k) → Zn2+(suda) + 2e– tepkimesi bir yükseltgenmedir.
İndirgenme (Redüksiyon)
Bir atomun veya iyonun elektron kazanması sürecidir. Elektron alan taneciğin yükseltgenme basamağı azalır. Bu olay hücrenin katot bölgesinde meydana gelir. Örneğin; Cu2+(suda) + 2e– → Cu(k) tepkimesi bir indirgenmedir.
Öğrenci Notu: Kavramları karıştırmamak için “KİMYA” kodlamasını unutmayın: Katotta İndirgenme, Meydana gelir; Yükseltgenme Anotta gerçekleşir.
Redoks tepkimelerinin nasıl eşitlendiğini hatırlamak için redoks tepkimeleri denkleştirme rehberimize göz atabilirsiniz.
Elektrokimyasal Hücre Türleri
Enerji dönüşümünün yönüne göre hücreler ikiye ayrılır. Aralarındaki en temel fark, tepkimenin kendiliğinden olup olmamasıdır.
| Özellik | Galvanik (Voltaik) Hücre | Elektrolitik Hücre (Elektroliz) |
|---|---|---|
| Enerji Dönüşümü | Kimyasal → Elektrik | Elektrik → Kimyasal |
| İstemlilik | İstemli (Kendiliğinden) | İstemsiz (Dış enerjiyle) |
| Anot İşareti | Negatif (-) | Pozitif (+) |
| Katot İşareti | Pozitif (+) | Negatif (-) |
| Kullanım Alanı | Piller, Aküler | Kaplamacılık, Metal Saflaştırma |
Standart Elektrot Potansiyelleri ve Aktiflik
Her metalin elektron verme (yükseltgenme) eğilimi farklıdır. Buna metalik aktiflik denir. Standart şartlarda (25°C, 1 atm, 1M çözelti) hidrojen elektroduna karşı ölçülen bu değerlere “Standart Elektrot Potansiyeli” denir. Bir pilin voltajı, anot ve katot arasındaki potansiyel farkına eşittir.
Nernst Denklemi: Standart Olmayan Koşullar
Piller her zaman 1 molar derişimde çalışmaz. Derişimler değiştikçe pil potansiyeli de değişir. Bu değişimi hesaplamak için Nernst Denklemi kullanılır:
Ehücre = E°hücre – (0,0592 / n) . logQ
- n: Alınan-verilen elektron sayısı
- Q: Tepki oranı (Ürünlerin derişimi / Girenlerin derişimi)
Faraday’ın Elektroliz Yasaları
Elektroliz işleminde devreden geçen akım miktarı ile elektrotlarda toplanan madde miktarı doğru orantılıdır. Faraday yasalarına göre 1 mol elektron akımı 1 Faraday (yaklaşık 96.500 Coulomb) yüke eşittir.
m = (Q . MA) / (n . 96500) formülü ile devreden geçen yük miktarına (Q=I.t) bağlı olarak biriken kütle hesaplanabilir.
Elektrokimyanın Kullanım Alanları
- Korozyondan Korunma: Metallerin paslanmasını önlemek için daha aktif bir metalin “kurban elektrot” olarak kullanılması.
- Galvanoplasti: Değersiz metallerin altın veya gümüş gibi metallerle elektroliz yöntemiyle kaplanması.
- Lityum-İyon Piller: Günümüz taşınabilir teknolojisinin enerji kaynağı.
Sıkça Sorulan Sorular
Tuz köprüsü ne işe yarar?
Tuz köprüsü, her iki yarı hücredeki yük denkliğini sağlar. Anyonlar anoda, katyonlar katoda giderek devrenin tamamlanmasını sağlar.
Elektronlar hangi yöne akar?
Dış devrede elektronlar her zaman yükseltgenmenin olduğu anottan, indirgenmenin olduğu katoda doğru akar.
Standart pil potansiyeli (E°) ne zaman sıfır olur?
Pil dengeye ulaştığında (bitmiş pil) potansiyel farkı sıfır olur. Ancak standart potansiyel, elementlerin cinsine bağlı sabit bir değerdir.
Sonuç
Elektrokimya, elektronların hareketini kontrol ederek enerji üretme veya madde dönüştürme sanatıdır. Sınavlarda başarılı olmak için “KİMYA” kodlamasını kavramak, aktiflik sıralamasını doğru yorumlamak ve Nernst/Faraday formüllerinde birimlere dikkat etmek kritik önem taşır. Bu temel prensipleri oturttuktan sonra derişim pilleri ve korozyon gibi ileri seviye konuları çok daha rahat anlayabilirsiniz.
