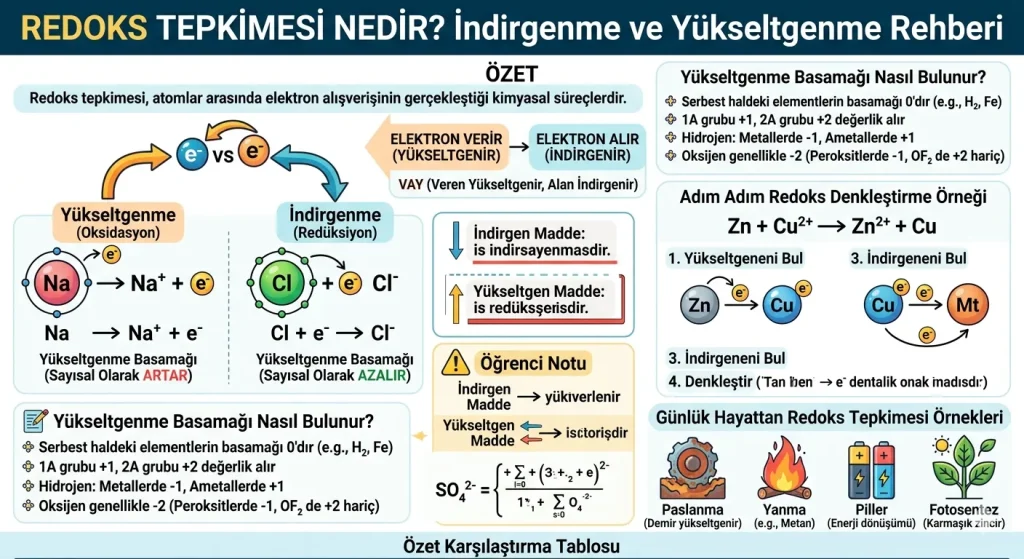
Özet: Redoks tepkimesi, atomlar arasında elektron alışverişinin gerçekleştiği kimyasal süreçlerdir. Bir maddenin elektron vererek yükseltgendiği, diğerinin ise bu elektronları alarak indirgendiği bu tepkimeler; pillerden paslanmaya, solunumdan yanmaya kadar hayatın her alanında karşımıza çıkar.
Redoks tepkimeleri, “Redüksiyon” (indirgenme) ve “Oksidasyon” (yükseltgenme) kelimelerinin birleşiminden oluşur. Kimyanın en temel konularından biri olan bu süreçte, toplam alınan elektron sayısı her zaman toplam verilen elektron sayısına eşittir. Bu denklik, tepkimelerin denkleştirilmesindeki temel kuraldır.
Temel Kavramlar: İndirgenme ve Yükseltgenme
Bir tepkimenin redoks olup olmadığını anlamak için atomların yükseltgenme basamaklarındaki değişime bakılır. Bu süreci aklınızda tutmak için şu basit kodlamayı kullanabilirsiniz: “VAY” (Veren Yükseltgenir, Alan İndirgenir).
Yükseltgenme (Oksidasyon) Nedir?
Bir atomun veya iyonun elektron vermesi olayına yükseltgenme denir. Elektron veren taneciğin yükseltgenme basamağı (değerliği) sayısal olarak artar. Örneğin, nötr bir sodyum (Na) atomu bir elektron verdiğinde Na+ iyonuna dönüşür ve yükseltgenmiş olur.
İndirgenme (Redüksiyon) Nedir?
Bir atomun veya iyonun elektron alması olayına indirgenme denir. Elektron alan taneciğin yükseltgenme basamağı sayısal olarak azalır. Örneğin, bir klor (Cl) atomu bir elektron aldığında Cl- iyonuna dönüşür ve indirgenmiş olur.
Öğrenci Notu: “Yükseltgen” ve “İndirgen” kavramları sıfat olarak kullanılır. Karşısındakini indirgeyen maddeye indirgen (kendisi yükseltgenir), karşısındakini yükseltgeyen maddeye yükseltgen (kendisi indirgenir) denir. Bu ters mantık sınavların en çok puan kaybettiren noktasıdır!
Yükseltgenme Basamağı Nasıl Bulunur?
Redoks tepkimelerini çözebilmek için atomların bileşik içindeki yüklerini doğru hesaplamak gerekir. Yükseltgenme basamağı bulunurken şu kurallar dikkate alınır:
- Serbest haldeki elementlerin (H2, O2, Na, Fe vb.) yükseltgenme basamağı 0’dır.
- 1A grubu metalleri her zaman +1, 2A grubu metalleri her zaman +2 değerlik alır.
- Hidrojen, metallerle yaptığı bileşiklerde -1, ametallerle yaptığı bileşiklerde +1 değerlik alır.
- Oksijen genellikle -2 değerlik alır (Peroksitlerde -1, OF2 bileşiğinde +2 hariç).
Kritik Hatırlatma: Çok atomlu iyonlarda (köklerde) atomların yükseltgenme basamakları toplamı, kökün toplam yüküne eşittir. Örneğin; Sülfat (SO4²⁻) kökünde toplam yük -2 iken, Nitrat (NO3⁻) kökünde toplam yük -1’dir.
Adım Adım Redoks Denkleştirme Örneği
Teorik bilgiyi pratik bir örnekle pekiştirelim. Aşağıdaki tepkimeyi inceleyelim:
Zn + Cu²⁺ → Zn²⁺ + Cu
- Yükleri Belirle: Zn (0), Cu (+2) → Zn (+2), Cu (0).
- Yükseltgeneni Bul: Çinko (Zn), 0’dan +2’ye çıkmış. 2 elektron vermiştir (Yükseltgenmiştir/İndirgen maddedir).
- İndirgeneni Bul: Bakır (Cu), +2’den 0’a inmiş. 2 elektron almıştır (İndirgenmiştir/Yükseltgen maddedir).
- Denkleştir: Alınan ve verilen elektron sayıları eşit (2e-) olduğu için bu tepkime şu an denktir.
Günlük Hayattan Redoks Tepkimesi Örnekleri
Redoks sadece laboratuvar ortamında gerçekleşmez; çevremizde sürekli devam eden süreçlerin temelidir:
- Paslanma: Demirin oksijenle tepkimeye girerek yükseltgenmesi bir redoks sürecidir.
- Yanma: Tüm yanma tepkimeleri (örneğin metan gazının yanması) birer redoks tepkimesidir.
- Piller: Kimyasal enerjiyi elektrik enerjisine dönüştüren piller, kontrollü redoks tepkimeleriyle çalışır.
- Fotosentez: Bitkilerin güneş enerjisiyle besin üretmesi karmaşık bir redoks zinciridir.
Özet: Redoks Tepkimeleri Karşılaştırma Tablosu
| Özellik | Yükseltgenme (Oksidasyon) | İndirgenme (Redüksiyon) |
|---|---|---|
| Elektron Durumu | Elektron Verilir | Elektron Alınır |
| Yükseltgenme Basamağı | Artar | Azalır |
| Maddenin Rolü | İndirgen Madde | Yükseltgen Madde |
Sıkça Sorulan Sorular
Her kimyasal tepkime bir redoks tepkimesi midir?
Hayır. Bir tepkimenin redoks olabilmesi için atomların yükseltgenme basamaklarında bir değişim olması gerekir. Örneğin, asit-baz tepkimelerinin çoğu redoks değildir; çünkü sadece iyon değişimi gerçekleşir.
Yanma tepkimeleri neden her zaman redokstur?
Yanma tepkimelerinde elementel haldeki oksijen (O2, yükü 0), bileşik oluştururken elektron alarak -2 yüküne indirgenir. Oksijen indirgendiği için yanma tepkimeleri mutlaka bir redoks sürecidir.
Redoks tepkimelerinde kütle korunur mu?
Evet, tüm kimyasal tepkimelerde olduğu gibi redoks tepkimelerinde de toplam kütle, atom türü ve sayısı her zaman korunur.
Sonuç
Redoks tepkimesi, elektron transferi prensibine dayanan ve kimyanın pek çok alt dalını birbirine bağlayan bir konudur. İndirgenme ve yükseltgenme kavramlarını, “Veren Yükseltgenir” kuralıyla kodlamak, denkleştirme sorularında hız kazanmanızı sağlar. Bu konuyu tam olarak kavramak için Kimyasal Tepkime Türleri .
