Hidrokarbonlar, yapısında sadece karbon (C) ve hidrojen (H) atomlarını bulunduran en temel organik bileşik sınıfıdır. Günlük hayatta kullandığımız doğal gaz, petrol, kömür ve LPG gibi enerji kaynaklarının ana bileşeni olan bu yapılar, organik kimyanın iskeletini oluşturur. Kimyasal bağ yapılarına göre temel olarak doymuş ve doymamış olmak üzere iki ana kategoride incelenirler.
Hidrokarbon Nedir? (Kısa Özet)
Hidrokarbonlar, karbon atomlarının birbirine bağlanarak oluşturduğu zincir veya halka yapılarına hidrojen atomlarının eklenmesiyle meydana gelir. Diğer tüm organik bileşikler (alkoller, eterler, karboksilik asitler vb.), hidrokarbon zincirlerine farklı fonksiyonel grupların bağlanmasıyla türetilir. Temel özellikleri şunlardır:
- Sadece C ve H atomlarından oluşurlar.
- Apolar yapıda oldukları için suda çözünmezler (hidrofobiktirler).
- Yüksek yanma ısısına sahiptirler, bu nedenle mükemmel yakıtlardır.
- Molekül büyüdükçe erime ve kaynama noktaları genellikle artar.
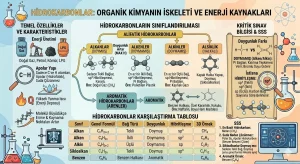
Hidrokarbonların Sınıflandırılması
Hidrokarbonlar, karbon atomları arasındaki bağların türüne ve molekülün geometrik dizilimine göre iki ana gruba ayrılır: Alifatik ve Aromatik hidrokarbonlar.
1. Alifatik Hidrokarbonlar
Düz zincirli, dallanmış veya halkalı yapıda olabilen bu grup, kendi içinde üç temel sınıfa ayrılır:
- Alkanlar: Karbonlar arasında sadece tekli bağlar bulunur. “Doymuş hidrokarbonlar” olarak adlandırılırlar. En basit üyesi metandır (CH₄).
- Alkenler: Yapısında en az bir adet ikili bağ bulunduran doymamış hidrokarbonlardır.
- Alkinler: Yapısında en az bir adet üçlü bağ içeren doymamış hidrokarbonlardır.
- Alisiklik (Halkalı) Hidrokarbonlar: Karbon atomlarının kapalı bir halka oluşturduğu yapılardır. Örneğin, altı karbonlu bir halkadan oluşan siklohekzan, bu grubun en yaygın örneğidir.
Daha detaylı bilgi için organik kimyaya giriş içeriğimize göz atabilirsiniz.
2. Aromatik Hidrokarbonlar (Arenler)
Yapılarında en az bir tane benzen halkası bulunduran bileşiklerdir. Benzen (C₆H₆), altı karbon atomunun birbirine bir tek, bir çift bağla bağlanarak oluşturduğu düzgün altıgen bir halka yapısına sahiptir. Bu özel yapı, moleküle yüksek kararlılık ve kendine has bir koku kazandırır. Benzenin yanı sıra naftalin ve antrasen bu grubun en bilinen örnekleridir.
Doymuş ve Doymamış Hidrokarbonlar Arasındaki Farklar
Kimya sınavlarında en sık karşılaşılan konulardan biri bağ doygunluğudur. Bu ayrım, molekülün kimyasal tepkime verme yatkınlığını belirler.
Doymuş Hidrokarbonlar: Karbon atomları arasındaki tüm bağlar tekli (sigma) bağdır. Karbon, bağlanabileceği maksimum hidrojen sayısına ulaşmıştır. Alkanlar bu gruptadır ve oldukça kararlıdırlar.
Doymamış Hidrokarbonlar: Karbon atomları arasında ikili veya üçlü bağlar (pi bağları) bulunur. Bu bağlar, molekülün dışarıdan hidrojen veya başka atomlar alarak “doyurulmasına” imkan tanır. Alkenler ve alkinler bu sınıfa girer.
Kritik Not: Bir hidrokarbonun doymamış olması, onun kimyasal olarak daha aktif olduğu ve katılma tepkimelerine (örneğin bromlu suyun rengini giderme) yatkın olduğu anlamına gelir.
Alkanlar, Alkenler ve Alkinler Karşılaştırma Tablosu
Aşağıdaki tablo, AYT Kimya ve genel kimya derslerinde en çok ihtiyaç duyacağınız genel formülleri ve özellikleri özetlemektedir:
| Özellik | Alkanlar | Alkenler | Alkinler |
|---|---|---|---|
| Genel Formül | CnH2n+2 | CnH2n | CnH2n-2 |
| Bağ Türü | Sadece Tekli Bağ | En az bir İkili Bağ | En az bir Üçlü Bağ |
| Doygunluk | Doymuş | Doymamış | Doymamış |
| Hibritleşme | sp3 | sp2 | sp |
Hibritleşme Notu: Tabloda yer alan hibritleşme türleri, karbon atomunun yaptığı bağ sayısına göre belirlenir. Sadece tekli bağ yapan karbonlar sp³, bir adet ikili bağ yapanlar sp², bir adet üçlü bağ yapanlar ise sp hibritleşmesi yapar. Bağ yapıları hakkında daha fazla teknik detay için kimyasal bağlar ve türleri yazımızı inceleyebilirsiniz.
Hidrokarbonların Temel Özellikleri ve Kullanım Alanları
Hidrokarbonlar modern sanayinin ve günlük yaşamın vazgeçilmezidir:
- Çözünürlük: Hidrokarbonlar apolardır; su gibi polar maddelerde çözünmezler, ancak benzen veya eter gibi organik çözücülerde iyi çözünürler.
- Yoğunluk: Genellikle sudan daha az yoğundurlar (su üzerinde yüzerler).
- Enerji Üretimi: Metan (doğal gaz), propan ve bütan (LPG), oktan (benzin) temel enerji kaynaklarıdır.
- Sanayi: Plastik (polietilen), sentetik kauçuk, boya, ilaç ve patlayıcı üretiminde ham madde olarak kullanılırlar.
Sıkça Sorulan Sorular (SSS)
1. En basit hidrokarbon hangisidir?
En basit hidrokarbon, alkanlar sınıfının ilk üyesi olan ve tek bir karbon atomu içeren Metan (CH₄) gazıdır.
2. Hidrokarbonlar suda neden çözünmez?
Kimyadaki “benzer benzeri çözer” ilkesi gereği, polar maddeler polar çözücülerde, apolar maddeler apolar çözücülerde çözünür. Su polar, hidrokarbonlar ise apolar olduğu için birbirleri içinde çözünmezler.
3. Sikloalkanlar doymuş mudur doymamış mıdır?
Sikloalkanlar, karbon atomları arasında sadece tekli bağlar içerdiği için doymuş hidrokarbonlar sınıfına girer; ancak genel formülleri halkalı yapıdan dolayı alkenlerle aynıdır (CnH2n).
4. Aromatik hidrokarbonların en bilinen örneği nedir?
En temel ve en bilinen aromatik hidrokarbon, altıgen halka yapısıyla karakterize edilen benzen (C₆H₆) molekülüdür.
Sonuç ve Özet
Hidrokarbonlar, sadece karbon ve hidrojen atomlarından oluşan, organik kimyanın en geniş ve en önemli bileşik grubudur. Alkanlar (doymuş), alkenler ve alkinler (doymamış) alifatik grubu oluştururken; benzen halkası içeren yapılar aromatik grup olarak adlandırılır. Bu bileşiklerin genel formüllerini, hibritleşme türlerini ve bağ yapılarını kavramak, organik kimya konularında başarı sağlamanın anahtarıdır.
