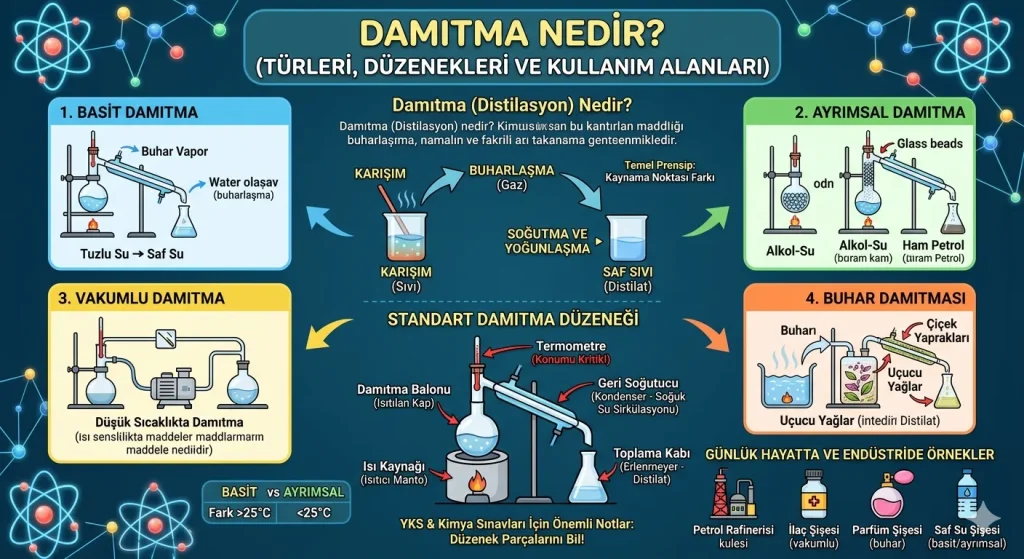
Damıtma, bir sıvı karışımındaki bileşenleri kaynama noktası farklarından yararlanarak birbirinden ayırma yöntemidir. Kimya biliminde “distilasyon” olarak da adlandırılan bu işlem, karışımın ısıtılarak buharlaştırılması ve ardından bu buharın soğutularak tekrar sıvı hale getirilmesi prensibine dayanır. Hem laboratuvar ortamında saflaştırma işlemlerinde hem de endüstride ham petrolün işlenmesi gibi kritik alanlarda en yaygın kullanılan fiziksel ayırma yöntemidir.
Damıtma (Distilasyon) Nedir? (Kısa Özet)
Damıtma, homojen karışımları ayırmak için kullanılan fiziksel bir yöntemdir. Maddelerin kimyasal yapısı değişmez; sadece fiziksel halleri (sıvıdan gaza, gazdan tekrar sıvıya) değişir.
- Temel Prensip: Bileşenlerin kaynama noktası farkı.
- Yöntem: Buharlaşma ve ardından yoğuşma (yoğunlaşma).
- Kullanım Amacı: Karışımları bileşenlerine ayırmak veya bir sıvıyı saflaştırmak.
Damıtma İşleminin Çalışma Prensibi
Damıtma işlemi iki ana aşamadan oluşur. İlk aşamada karışım, içindeki bileşenlerden birinin kaynama noktasına ulaşana kadar ısıtılır. Kaynama noktası düşük olan (uçucu olan) madde hızla buharlaşmaya başlar. İkinci aşamada ise oluşan bu buhar, bir soğutucu (kondenser) içinden geçirilerek tekrar sıvı faza dönüştürülür ve ayrı bir kapta toplanır. Bu toplanan sıvıya distilat denir.
Kaynama noktaları arasındaki fark ne kadar büyükse, ayırma işlemi o kadar verimli ve kolay olur. Eğer fark az ise daha gelişmiş teknikler olan ayrımsal damıtma devreye girer.
Damıtma Türleri Nelerdir?
Karışımın türüne ve bileşenlerin özelliklerine göre farklı damıtma teknikleri uygulanır:
1. Basit Damıtma
Kaynama noktaları arasında büyük fark (genellikle 25°C’den fazla) olan sıvı-sıvı karışımları veya katı-sıvı homojen karışımları ayırmak için kullanılır. Örneğin, tuzlu sudan saf su elde etmek için basit damıtma yöntemi tercih edilir. Bu yöntemde katı madde ısıtma kabında kalırken, sıvı buharlaşıp ayrı bir kapta toplanır.
2. Ayrımsal Damıtma
Kaynama noktaları birbirine yakın olan (25°C’den az fark olan) sıvı-sıvı homojen karışımları ayırmak için kullanılır. En klasik örneği alkol-su karışımıdır. Bu yöntemde, basit damıtma düzeneğine ek olarak bir fraksiyon kolonu kullanılır. Bu kolon, buharın defalarca yoğunlaşıp tekrar buharlaşmasını sağlayarak ayırma işleminin çok daha hassas gerçekleşmesini sağlar. Daha detaylı bilgi için karışımların sınıflandırılması içeriğimize göz atabilirsiniz.
3. Vakumlu Damıtma
Bazı maddelerin kaynama noktaları çok yüksektir veya bu maddeler yüksek sıcaklıkta kimyasal yapıları bozularak (dekompoze) özelliklerini kaybederler. Vakumlu damıtma yönteminde, düzenek içindeki hava boşaltılarak dış basınç düşürülür. Basınç düştükçe maddelerin kaynama noktası da düşer; böylece madde bozulmadan daha düşük sıcaklıklarda damıtılabilir.
4. Buhar Damıtması
Suyla karışmayan ancak uçucu olan maddeleri (özellikle bitkisel yağlar) ayırmak için kullanılır. Su buharı karışımın içinden geçirilerek, maddenin kendi kaynama noktasından çok daha düşük bir sıcaklıkta buharlaşması sağlanır. Parfüm ve esans üretiminde temel yöntemdir.
Damıtma Düzeneğinde Hangi Parçalar Bulunur?
Standart bir laboratuvar damıtma düzeneği şu temel parçalardan oluşur:
- Damıtma Balonu: Karışımın konulduğu ve ısıtıldığı kaptır.
- Isı Kaynağı: Karışımı buharlaştırmak için kullanılan ocak veya ısıtıcı mantodur.
- Termometre: Buharın sıcaklığını ölçer. Kritik Not: Termometrenin haznesi, tam olarak buharın soğutucuya yönlendiği çıkış borusunun (dirsek) hizasında olmalıdır. Bu, o an hangi maddenin buharlaştığını doğru tespit etmek için şarttır.
- Geri Soğutucu (Kondenser): Buharın içinden geçtiği ve dış çeperindeki soğuk su sirkülasyonu sayesinde buharı tekrar sıvıya dönüştüren cam borudur.
- Toplama Kabı (Erlenmeyer): Saflaştırılmış sıvının (distilat) biriktiği kaptır.
Karşılaştırma: Basit Damıtma vs. Ayrımsal Damıtma
Öğrencilerin sınavda en çok karşılaştığı farklar aşağıdaki tabloda özetlenmiştir:
| Özellik | Basit Damıtma | Ayrımsal Damıtma |
|---|---|---|
| Karışım Türü | Katı-Sıvı veya Kaynama noktası farkı > 25°C | Kaynama noktası farkı < 25°C olan Sıvı-Sıvı |
| Ekipman Farkı | Standart cam düzenek | Fraksiyon kolonu (cam boncuklu kolon) |
| Örnek | Tuzlu su, şekerli su | Alkol-su, Ham petrolün rafinasyonu |
| Saflık Derecesi | Orta | Çok Yüksek |
Günlük Hayatta ve Endüstride Damıtma Örnekleri
Damıtma, modern yaşamın devamlılığı için gerekli bir endüstriyel süreçtir:
- Petrol Rafinerileri: Ham petrol, devasa ayrımsal damıtma kulelerinde ısıtılarak benzin, mazot, jet yakıtı ve LPG gibi bileşenlerine ayrılır.
- İlaç ve Kimya Sanayisi: İlaç hammaddelerinin saflaştırılmasında vakumlu damıtma yaygın olarak kullanılır.
- Parfüm ve Esans Üretimi: Bitkilerdeki aromatik yağlar buhar damıtması yöntemiyle elde edilir.
- Saf Su Üretimi: Akü suyu veya laboratuvarlarda kullanılan saf sular damıtma ile hazırlanır.
Konuyla ilgili daha geniş bir perspektif için karışımları ayırma teknikleri rehberimizi inceleyebilirsiniz.
Sıkça Sorulan Sorular
1. Damıtma fiziksel mi yoksa kimyasal bir yöntem midir?
Damıtma, maddelerin kaynama noktası farkından yararlanan fiziksel bir ayırma yöntemidir; maddenin kimyasal yapısı değişmez.2. Damıtma ile ayırma hunisi arasındaki fark nedir?
Damıtma, homojen (birbiri içinde çözünmüş) karışımları ayırmak için kullanılır. Ayırma hunisi ise zeytinyağı-su gibi birbiriyle karışmayan heterojen sıvı-sıvı karışımları yoğunluk farkıyla ayırmak için kullanılır.3. Ayrımsal damıtmada neden fraksiyon kolonu kullanılır?
Fraksiyon kolonu, buharın yüzey alanını artırarak defalarca yoğunlaşıp tekrar buharlaşmasını sağlar. Bu sayede kaynama noktaları birbirine çok yakın olan sıvılar bile yüksek saflıkta birbirinden ayrılabilir.
Sonuç
Damıtma, kimya dünyasında karışımları ayırmak için kullanılan en temel ve etkili yöntemlerden biridir. Kaynama noktası farkına dayanan bu süreç; basit, ayrımsal, vakumlu ve buhar damıtması gibi çeşitleriyle geniş bir uygulama alanına sahiptir. Günlük hayatta kullandığımız yakıtlardan içtiğimiz saf suya, sürdüğümüz parfümden ilaç sanayisine kadar pek çok alanda damıtma yönteminin izlerini görmek mümkündür. Özellikle YKS ve lise kimya sınavlarında düzenek parçalarını (özellikle termometre konumu) ve yöntem farklarını bilmek size büyük avantaj sağlayacaktır.
