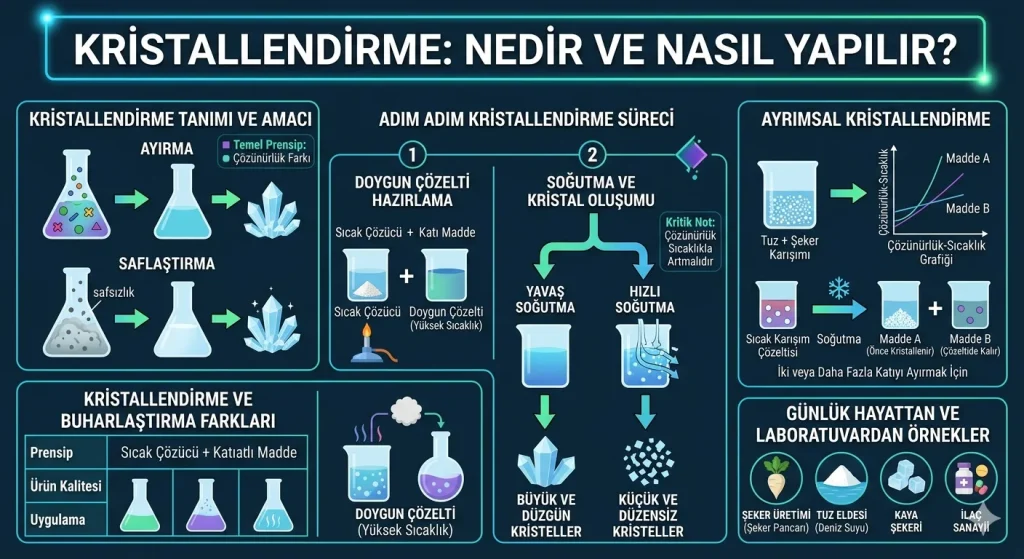
Kristallendirme, bir katının uygun bir çözücüde çözündükten sonra sıcaklık değişimi veya çözücü buharlaştırılması yoluyla tekrar katı fazına (kristal yapıya) geçirilmesi işlemidir. Temel prensibi çözünürlük farkıdır.
Kimya laboratuvarlarında ve endüstride en sık kullanılan yöntemlerden biri olan kristallendirme, saflaştırma ve ayırma amacıyla kullanılan bir tekniktir. Özellikle katı-sıvı homojen karışımları birbirinden ayırmak veya bir katı maddeyi içindeki safsızlıklardan arındırmak için bu yönteme başvurulur. Bu yazıda; kristallendirme sürecini, ayrımsal kristallendirmeyi ve bu yöntemin günlük hayattaki karşılıklarını detaylıca inceleyeceğiz.
Kristallendirme Yönteminin Tanımı ve Amacı
Kristallendirme, bir maddenin doymuş çözeltisinden kristal formunda katılaşarak ayrılması sürecidir. Bu yöntemin temel amacı, bir karışım içerisindeki istenen katı maddeyi en saf haliyle elde etmektir. Çözünürlüğü sıcaklıkla değişen maddeler için oldukça etkili bir ayırma tekniğidir.
Bu yöntem şu iki temel amaç için kullanılır:
- Ayırma: Bir sıvı içerisinde çözünmüş olan katıyı geri kazanmak.
- Saflaştırma: Bir katı maddenin yapısındaki istenmeyen yabancı maddeleri (safsızlıkları) uzaklaştırmak.
Kristallendirme Nasıl Yapılır? (Adım Adım Süreç)
Kristallendirme işlemi rastgele bir soğutma süreci değildir; belirli aşamaların dikkatle uygulanmasını gerektirir. İşte adım adım kristallendirme süreci:
1. Doygun Çözelti Hazırlama
İlk adımda, ayrılmak istenen katı madde uygun bir çözücü içerisinde (genellikle yüksek sıcaklıkta) çözülür. Çözelti, maddenin o sıcaklıktaki maksimum miktarını içerecek şekilde “doygun” hale getirilir.
2. Soğutma ve Kristal Oluşumu
Hazırlanan sıcak ve doygun çözelti yavaşça soğumaya bırakılır. Sıcaklık düştükçe çözücünün o maddeyi tutma kapasitesi (çözünürlüğü) azalır. Fazlalık olan katı madde, düzgün geometrik şekillere sahip kristaller halinde çökmeye başlar.
Önemli Detay: Bu aşamada soğutma hızı kristal boyutunu doğrudan belirler. Yavaş soğutma daha büyük ve düzgün kristaller oluştururken, hızlı soğutma daha küçük ve düzensiz kristal yapılarına neden olur.
Kritik Not: Bir maddenin kristallendirme ile ayrılabilmesi için çözünürlüğünün sıcaklıkla belirgin bir şekilde değişmesi (genellikle sıcaklık arttıkça artması) gerekir.
Ayrımsal Kristallendirme Nedir?
Eğer bir çözeltinin içerisinde birden fazla katı madde çözünmüşse ve biz bu katıları birbirinden ayırmak istiyorsak ayrımsal kristallendirme yöntemini kullanırız. Bu yöntem, karışımda bulunan maddelerin çözünürlüklerinin sıcaklıkla farklı oranlarda değişmesi prensibine dayanır.
Ayrımsal kristallendirme işlemlerinde çözünürlük-sıcaklık grafikleri en kritik rehberdir. Grafikte çözünürlüğü sıcaklık düşüşüyle hızla azalan madde önce kristallenirken, çözünürlüğü sıcaklıktan daha az etkilenen madde çözeltide kalmaya devam eder.
Ayrımsal Kristallendirme ile Normal Kristallendirme Arasındaki Fark
Normal kristallendirme genellikle tek bir katıyı sıvıdan ayırmak veya saflaştırmak için kullanılırken; ayrımsal kristallendirme, iki veya daha fazla katının (örneğin tuz ve şeker karışımı) çözünürlük farkından yararlanarak birbirinden ayrılması işlemidir.
Daha fazla bilgi için: Karışımları ayırma teknikleri nelerdir?
Kristallendirme ve Buharlaştırma Arasındaki Farklar
Öğrenciler genellikle bu iki yöntemi birbiriyle karıştırır. Ancak aralarında temel uygulama ve sonuç farkları vardır:
| Özellik | Kristallendirme | Buharlaştırma |
|---|---|---|
| Temel Prensip | Çözünürlük farkı ve sıcaklık değişimi. | Kaynama noktası farkı. |
| Ürün Kalitesi | Daha saf ve düzenli kristaller elde edilir. | Katı madde düzensiz bir kütle halinde kalır. |
| Uygulama | Çözelti kontrollü soğutulur. | Çözücü tamamen uzaklaştırılır. |
Günlük Hayattan ve Laboratuvardan Kristallendirme Örnekleri
Kristallendirme sadece laboratuvarlarda değil, sanayinin birçok alanında karşımıza çıkar:
- Şeker Üretimi: Şeker pancarından elde edilen özütün kristallendirilerek toz şeker haline getirilmesi.
- Tuz Eldesi: Deniz suyunun havuzlarda bekletilerek suyunun buharlaştırılması ve tuzun kristallenmesi.
- Kaya Şekeri: Aşırı doymuş şekerli suyun yavaşça soğutularak büyük şeker kristallerinin elde edilmesi.
- İlaç Sanayii: İlaç ham maddelerinin safsızlıklardan arındırılması aşamasında en yaygın kullanılan yöntemdir.
Sıkça Sorulan Sorular
1. Kristallendirme hangi tür karışımlar için uygundur?
Genellikle katı-sıvı homojen karışımları (çözeltileri) bileşenlerine ayırmak veya saflaştırmak için kullanılır.
2. Ayrımsal kristallendirme için temel şart nedir?
Karışımdaki farklı katıların çözünürlüklerinin sıcaklıkla değişim hızlarının birbirinden farklı olması gerekir. Eğer iki maddenin çözünürlük eğrisi birbirine çok yakınsa bu yöntem verimli olmaz.
3. Şekerli su kristallendirme ile ayrılabilir mi?
Evet, şekerli suyun sıcaklığı düşürüldüğünde veya suyu bir miktar buharlaştırılıp soğumaya bırakıldığında şeker kristalleri dibe çöker.
4. Çözünürlüğü sıcaklıkla azalan bir madde kristallendirilebilir mi?
Evet, ancak bu durumda çözelti soğutularak değil, ısıtılarak kristallendirme gerçekleştirilir. Çoğu katının çözünürlüğü sıcaklıkla arttığı için soğutma yöntemi daha yaygındır.
Sonuç
Kristallendirme, kimyada maddeleri saflaştırmak ve karışımları bileşenlerine ayırmak için kullanılan en etkili yöntemlerden biridir. Çözünürlük farkına dayanan bu teknik, özellikle şeker ve ilaç endüstrisi gibi alanlarda vazgeçilmezdir. Lise kimya müfredatında ve YKS gibi sınavlarda “çözünürlük-sıcaklık grafikleri” üzerinden sıkça sorulan bu konuyu kavramak, karışımların ayrılması ünitesinde başarı sağlamak adına kritik bir adımdır.
Konuyla ilgili daha derinlemesine bilgi için Homojen ve heterojen karışım farkları başlıklı içeriğimize göz atabilirsiniz.
