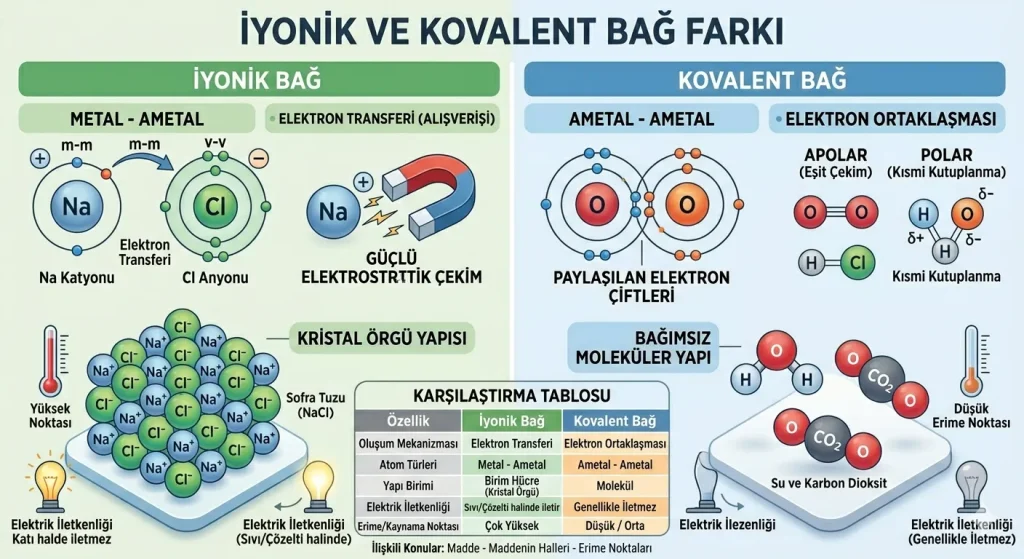
Kimyasal bağlar, atomların kararlı bir yapıya ulaşmak için birbirleriyle etkileşime girmesiyle oluşur. İyonik ve kovalent bağ farkı, temel olarak atomların elektronları nasıl kullandığına dayanır: İyonik bağda elektron alışverişi gerçekleşirken, kovalent bağda elektronlar ortaklaşa kullanılır. Bu temel fark, bileşiklerin erime noktasından elektrik iletkenliğine kadar tüm fiziksel ve kimyasal özelliklerini belirler.
Kısa Özet: İyonik vs. Kovalent Bağ
Zamanı kısıtlı olanlar için en temel farklar şunlardır:
- İyonik Bağ: Metal ve ametal atomları arasında, elektron transferi (alışverişi) ile oluşur.
- Kovalent Bağ: İki ametal atomu arasında, elektronların ortaklaşa kullanılmasıyla oluşur.
- İletkenlik: İyonik bileşikler sıvı halde veya çözeltide elektriği iletirken, kovalent bileşikler genellikle iletmez.
- Yapı: İyonik bağlar kristal örgü yapısındayken, kovalent bağlar bağımsız moleküler yapıdadır.
Daha kapsamlı bir temel için Kimyasal Türler Arası Etkileşimler Nelerdir? içeriğimize göz atabilirsiniz.
İyonik Bağ Nedir? (Elektron Alışverişi)
İyonik bağ, bir atomun (genellikle metal) elektron vererek pozitif yüklü katyona, diğer atomun (genellikle ametal) ise bu elektronu alarak negatif yüklü anyona dönüşmesi sonucu oluşur. Bu zıt yüklü iyonlar arasındaki güçlü elektrostatik çekim kuvvetine iyonik bağ denir. En bilinen örneği sofra tuzu olan Sodyum Klorür (NaCl) bileşiğidir.
İyonik Bağın Temel Özellikleri
- Metal + Ametal: Genellikle periyodik tablonun solundaki metaller ile sağındaki ametaller arasında kurulur.
- Yüksek Erime Noktası: Aradaki elektrostatik çekim çok güçlü olduğu için bu bağları koparmak yüksek enerji gerektirir.
- Katı Hal ve Kırılganlık: Oda koşullarında tamamı katı haldedir. Darbe aldıklarında kristal yapı kayar ve aynı yüklü iyonlar birbirini iterek yapının kırılmasına neden olur.
Kovalent Bağ Nedir? (Elektron Ortaklaşması)
Kovalent bağ, iki ametal atomunun kararlı hale (oktet veya dublet) gelebilmek için en dış katmanlarındaki elektronları ortaklaşa kullanmasıyla oluşur. Burada elektron transferi yoktur; her iki atom da aynı elektron çiftinden faydalanarak bağ kurar.
Polar ve Apolar Kovalent Bağlar
Kovalent bağlar, atomların elektronları çekme gücüne göre ikiye ayrılır:
- Apolar Kovalent Bağ: Aynı tür iki ametal atomu arasında oluşur (Örn: H-H, O=O, N≡N). Elektronlar her iki atom tarafından eşit kuvvetle çekilir.
- Polar Kovalent Bağ: Farklı tür iki ametal atomu arasında oluşur (Örn: H-Cl, H₂O). Elektronlar, elektronegatifliği daha yüksek olan atom tarafından daha güçlü çekilir, bu da molekülde kısmi kutuplanmaya yol açar.
Kovalent Bağın Temel Özellikleri
- Ametal + Ametal: Hidrojen, karbon, oksijen ve azot gibi ametal atomları arasında görülür.
- Moleküler Yapı: Bağımsız birimler olan moleküllerden oluşurlar (Örn: CO₂, CH₄).
- Fiziksel Hal: Oda koşullarında katı, sıvı veya gaz halde bulunabilirler. Erime ve kaynama noktaları iyonik bileşiklere göre genellikle daha düşüktür.
İyonik ve Kovalent Bağ Karşılaştırma Tablosu
Aşağıdaki tablo, sınav hazırlığında ve konu tekrarında en çok karşınıza çıkacak farkları özetlemektedir:
| Özellik | İyonik Bağ | Kovalent Bağ |
|---|---|---|
| Oluşum Mekanizması | Elektron Alışverişi | Elektron Ortaklaşması |
| Atom Türleri | Metal – Ametal | Ametal – Ametal |
| Yapı Birimi | Birim Hücre (Kristal Örgü) | Molekül |
| Elektrik İletkenliği | Sıvı ve çözelti halinde iletir | Genellikle iletmez |
| Erime/Kaynama Noktası | Çok Yüksek | Düşük / Orta |
| Oda Koşullarında Hal | Katı | Katı, Sıvı veya Gaz |
Bağ Türü Nasıl Belirlenir? (Elektronegatiflik Etkisi)
Bir bağın karakterini belirleyen en bilimsel ölçüt atomlar arasındaki elektronegatiflik farkıdır. Elektronegatiflik, bir atomun bağ elektronlarını kendine çekme isteğidir.
- Eğer iki atom arasındaki elektronegatiflik farkı 1.7’den büyükse, bağ iyonik karakterlidir.
- Eğer fark 1.7’den küçükse bağ kovalent karakterdedir.
- Fark sıfır ise (aynı iki ametal atomu arasında), bu bağa %100 apolar kovalent bağ denir.
Atomların yerini daha iyi kavramak için Periyodik Tablo: Gruplar ve Periyotlar Rehberi içeriğimize göz atabilirsiniz.
Sıkça Sorulan Sorular (SSS)
Hangi bağ türü daha güçlüdür?
Genel bir kural olarak, iyonik bağlar (elektrostatik çekim) moleküller arası etkileşimlerden çok daha güçlüdür. Ancak atomlar arasındaki tekil bağlar kıyaslandığında, kovalent bağlar da oldukça güçlü ve kararlı etkileşimlerdir.
Su (H₂O) iyonik mi yoksa kovalent bağ mı içerir?
Su, iki hidrojen (ametal) ve bir oksijen (ametal) atomundan oluştuğu için polar kovalent bağ içerir.
İyonik bileşikler neden katı halde elektriği iletmez?
Katı halde iyonlar kristal örgü içinde sabitlenmiştir ve hareket edemezler. Elektrik iletimi için iyonların hareketli olması gerekir; bu da ancak erime veya suda çözünme ile mümkündür.
Sonuç
İyonik ve kovalent bağlar, maddenin fiziksel ve kimyasal kimliğini oluşturan temel kuvvetlerdir. İyonik bağ metal-ametal arasında elektron transferiyle kristal yapılar oluştururken, kovalent bağ ametal-ametal arasında elektron ortaklaşmasıyla moleküler yapılar inşa eder. Bu farkları kavramak, kimya derslerinde bileşiklerin davranışlarını tahmin etmenizi kolaylaştıracaktır.
