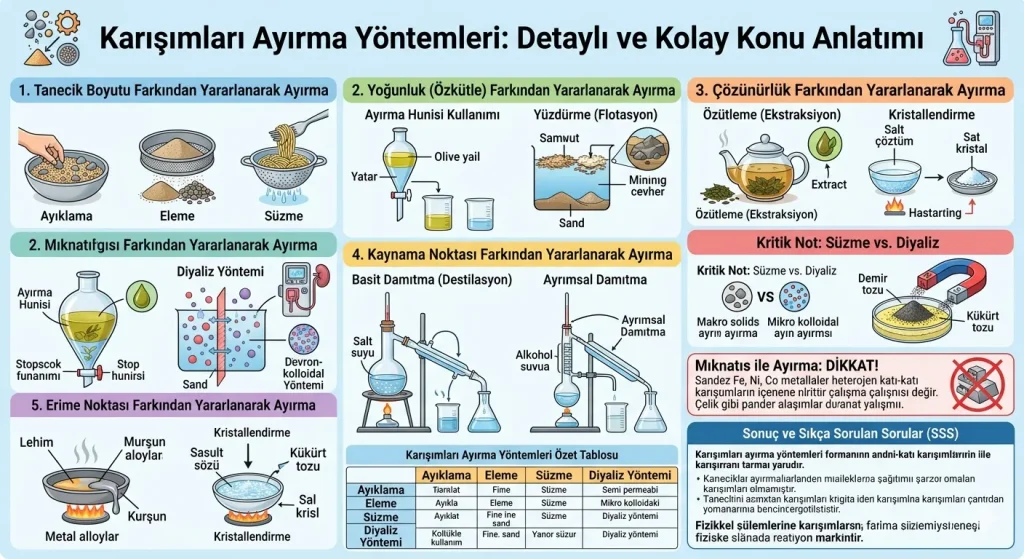
Karışımlar, birden fazla maddenin kimyasal özelliklerini kaybetmeden fiziksel yollarla bir araya gelmesiyle oluşur. Karışımları ayırma yöntemleri, bu maddeleri tekrar saf hallerine getirmek için bileşenlerin tanecik boyutu, yoğunluk, çözünürlük ve kaynama noktası gibi fiziksel özellik farklarından yararlanır. Bu rehberde, TYT Kimya müfredatına tam uyumlu olarak tüm ayırma tekniklerini güncel örneklerle inceleyeceğiz.
Karışımları Ayırma Yöntemleri Özet Tablosu
Hangi karışımın hangi yöntemle ayrılacağını hızlıca kavramak için hazırladığımız tabloyu inceleyebilirsiniz:
| Fiziksel Özellik Farkı | Ayırma Yöntemi | Örnek Karışım |
|---|---|---|
| Tanecik Boyutu | Ayıklama, Eleme, Süzme, Diyaliz | Kum-Çakıl, Makarna-Su, Kan |
| Yoğunluk (Özkütle) | Ayırma Hunisi, Yüzdürme (Flotasyon) | Zeytinyağı-Su, Talaş-Kum |
| Çözünürlük | Özütleme, Kristallendirme | Şekerli Su, Çay Demleme |
| Kaynama Noktası | Basit ve Ayrımsal Damıtma | Tuzlu Su, Alkol-Su |
| Erime Noktası | Erime Noktası Farkı ile Ayırma | Metal Alaşımları (Kurşun-Kalay) |
| Mıknatıslanma | Mıknatıs ile Ayırma | Demir Tozu-Kükürt |
1. Tanecik Boyutu Farkından Yararlanarak Ayırma
Bu yöntem, karışımı oluşturan maddelerin tanecik büyüklüklerinin birbirinden farklı olması esasına dayanır.
Ayıklama, Eleme ve Süzme
- Ayıklama: Şekil, renk veya büyüklükleri farklı olan katı-katı heterojen karışımlarda kullanılır. (Örn: Pirinç içindeki taşların ayıklanması)
- Eleme: Tanecik boyutları farklı olan katı-katı karışımları ayırmak için kullanılır. (Örn: Unun elenmesi, kum ve çakılın ayrılması)
- Süzme: Bir sıvı veya gaz içindeki katı tanecikleri ayırmak için kullanılır. (Örn: Haşlanmış makarnanın sudan ayrılması, fabrika bacalarındaki filtreler)
Diyaliz Yöntemi
Kolloidal karışımların (yarı geçirgen bir zardan geçemeyecek kadar büyük tanecikli karışımlar) ayrılmasında kullanılır. Özellikle böbrek hastalarında kanın temizlenmesi bu prensibe dayanır.
Editör Notu: Süzme ve diyaliz arasındaki temel fark boyuttur. Süzme işlemi gözle görülebilir makro düzeydeki katıları ayırırken; diyaliz, çıplak gözle seçilemeyen kolloidal (mikro) boyuttaki tanecikleri ayırmak için kullanılan bir nevi “mikro süzme” işlemidir.
2. Yoğunluk (Özkütle) Farkından Yararlanarak Ayırma
Birbirine karışmayan ve yoğunlukları farklı olan maddeleri ayırmak için tercih edilir.
Ayırma Hunisi Kullanımı
Birbiri içinde çözünmeyen sıvı-sıvı (heterojen) karışımları ayırmak için kullanılır. Ayırma hunisine konulan karışımda yoğunluğu büyük olan sıvı altta toplanır ve musluk açılarak başka bir kaba alınır. (Örn: Zeytinyağı-su, mazot-su)
Yüzdürme (Flotasyon) ve Çöktürme
- Yüzdürme (Flotasyon): Katı-katı heterojen karışımlarda, yoğunluğu sıvıdan küçük olan katının su yüzeyinde kalması sağlanır. (Örn: Maden cevherlerinin zenginleştirilmesi, kum ve talaş karışımı)
- Çöktürme: İki çözelti karıştırıldığında oluşan çözünmeyen katının (çökelek) dibe çökmesi işlemidir. Su arıtma tesislerinde kirleticilerin uzaklaştırılmasında sıkça kullanılır.
3. Çözünürlük Farkından Yararlanarak Ayırma
Maddelerin belirli bir çözücü içindeki çözünme kapasitelerinin farklı olmasından yararlanılır.
Özütleme (Ekstraksiyon)
Karışım içerisindeki bir maddenin, eklenen uygun bir çözücü yardımıyla bulunduğu ortamdan çekilip alınmasıdır. (Örn: Çayın demlenmesi, şeker pancarından şeker eldesi, ilaç ham maddelerinin bitkilerden elde edilmesi)
Kristallendirme ve Ayrımsal Kristallendirme
- Kristallendirme: Sıvı içinde çözünmüş bir katının, sıcaklık düşürülerek veya çözücü buharlaştırılarak katı halde çökertilmesidir.
- Ayrımsal Kristallendirme: Çözünürlükleri sıcaklıkla farklı şekilde değişen iki katının (Örn: Tuz ve şeker) karışımını ayırmak için kullanılır. Sıcaklık değiştirildiğinde çözünürlüğü daha hızlı azalan madde önce kristallenir.
4. Kaynama Noktası Farkından Yararlanarak Ayırma
Homojen karışımları (çözeltileri) bileşenlerine ayırmak için en yaygın kullanılan yöntemdir.
Basit Damıtma (Destilasyon)
Katı-sıvı homojen karışımlarda sıvıyı buharlaştırıp sonra başka bir kapta yoğuşturarak geri kazanma işlemidir. (Örn: Deniz suyundan saf su elde edilmesi)
Ayrımsal Damıtma
Kaynama noktaları birbirinden farklı olan sıvı-sıvı homojen karışımları ayırmak için kullanılır. Damıtma kolonunda kaynama noktası düşük olan sıvı önce buharlaşır ve yoğuşarak ayrı bir kapta toplanır. (Örn: Alkol-su karışımı, ham petrolün rafinasyonu)
5. Erime Noktası Farkından Yararlanarak Ayırma
Özellikle katı-katı homojen karışımlar olan alaşımları ayırmak için kullanılır. Karışım ısıtıldığında erime noktası düşük olan metal önce eriyerek sıvı hale geçer ve ortamdan uzaklaştırılır. (Örn: Kurşun ve kalaydan oluşan lehim alaşımının bileşenlerine ayrılması)
6. Mıknatıs ile Ayırma Yöntemi
Karışımdaki maddelerden birinin mıknatıs tarafından çekilme özelliği (ferromanyetik) taşıması gerekir. Demir (Fe), Nikel (Ni) ve Kobalt (Co) metalleri mıknatıs tarafından çekilir.
DİKKAT: Mıknatıs ile ayırma yöntemi sadece heterojen katı-katı karışımlarda işe yarar. Demir içeren bir alaşım (örneğin çelik) mıknatıs ile bileşenlerine ayrılamaz; çünkü alaşımlar homojen karışımlardır ve metalik bağlar nedeniyle fiziksel olarak çekilip koparılamazlar.
Homojen ve Heterojen Karışımlar Arasındaki Farklar yazımızı okuyarak karışım türleri hakkında daha fazla bilgi edinebilirsiniz.
Sıkça Sorulan Sorular
Soru: Zeytinyağı ve su karışımı hangi yöntemle ayrılır?
Cevap: Zeytinyağı ve su heterojen bir sıvı-sıvı karışımıdır. Yoğunlukları farklı olduğu için “Ayırma Hunisi” kullanılarak birbirinden ayrılırlar.
Soru: Tuzlu su karışımı nasıl ayrıştırılır?
Cevap: Tuzlu su homojen bir karışımdır. Suyu geri kazanmak istiyorsak “Basit Damıtma”, sadece tuzu elde etmek istiyorsak “Buharlaştırma” yöntemi kullanılır.
Soru: Ayrımsal damıtma ile basit damıtma arasındaki fark nedir?
Cevap: Basit damıtma katı-sıvı homojen karışımlar için kullanılırken; ayrımsal damıtma, kaynama noktaları birbirinden farklı olan sıvı-sıvı homojen karışımları ayırmak için kullanılır.
Sonuç ve Çalışma İpuçları
Karışımları ayırma yöntemlerini öğrenirken ezber yapmak yerine, yöntemin hangi fiziksel özellik farkına dayandığını kavramak sınav başarınızı artıracaktır. Özellikle TYT Kimya sorularında “yoğunluk farkı” ile “kaynama noktası farkı” arasındaki ayrım sıkça sorulur.
Unutmayın: Ayırma yöntemleri kimyasal değil, fiziksel işlemlerdir. Maddelerin kimlik özellikleri bu işlemler sırasında değişmez. Sadece fiziksel halleri veya konumları değişir.
