Toprak alkali metaller, periyodik tablonun 2A grubunda yer alan metal elementlerdir. Bu elementlerin son katmanlarında 2 değerlik elektronu bulunur. Bu elektronları vererek genellikle +2 yüklü iyon oluştururlar.
Bu grup, kimyada hem periyodik özellikleri anlamak hem de element gruplarını karşılaştırmak açısından önemlidir. Magnezyum, kalsiyum ve baryum gibi elementler günlük yaşamda, canlı yapısında ve endüstride önemli yer tutar.
Önemli bilgi: Toprak alkali metaller 2A grubunda yer alır. Alkali metallerden farklı olarak son katmanlarında 2 elektron bulunur ve genellikle +2 iyon oluştururlar.
Toprak Alkali Metal Nedir?
Toprak alkali metal, periyodik tablonun 2A grubunda bulunan ve metalik özellik gösteren elementlere verilen addır. Bu elementler s-blok elementleri arasında yer alır.
Toprak alkali metallerin ortak özelliği, son katmanlarında 2 değerlik elektronu bulundurmalarıdır. Bu iki elektronu vererek soygaz elektron düzenine yaklaşırlar ve genellikle +2 yüklü katyon oluştururlar.
Bu konuyu daha iyi anlamak için önce Periyodik Tablo Nedir?, Alkali Metaller Nedir? ve İyonlaşma Enerjisi Nedir? yazılarını inceleyebilirsin.
Toprak Alkali Metaller Hangileridir?
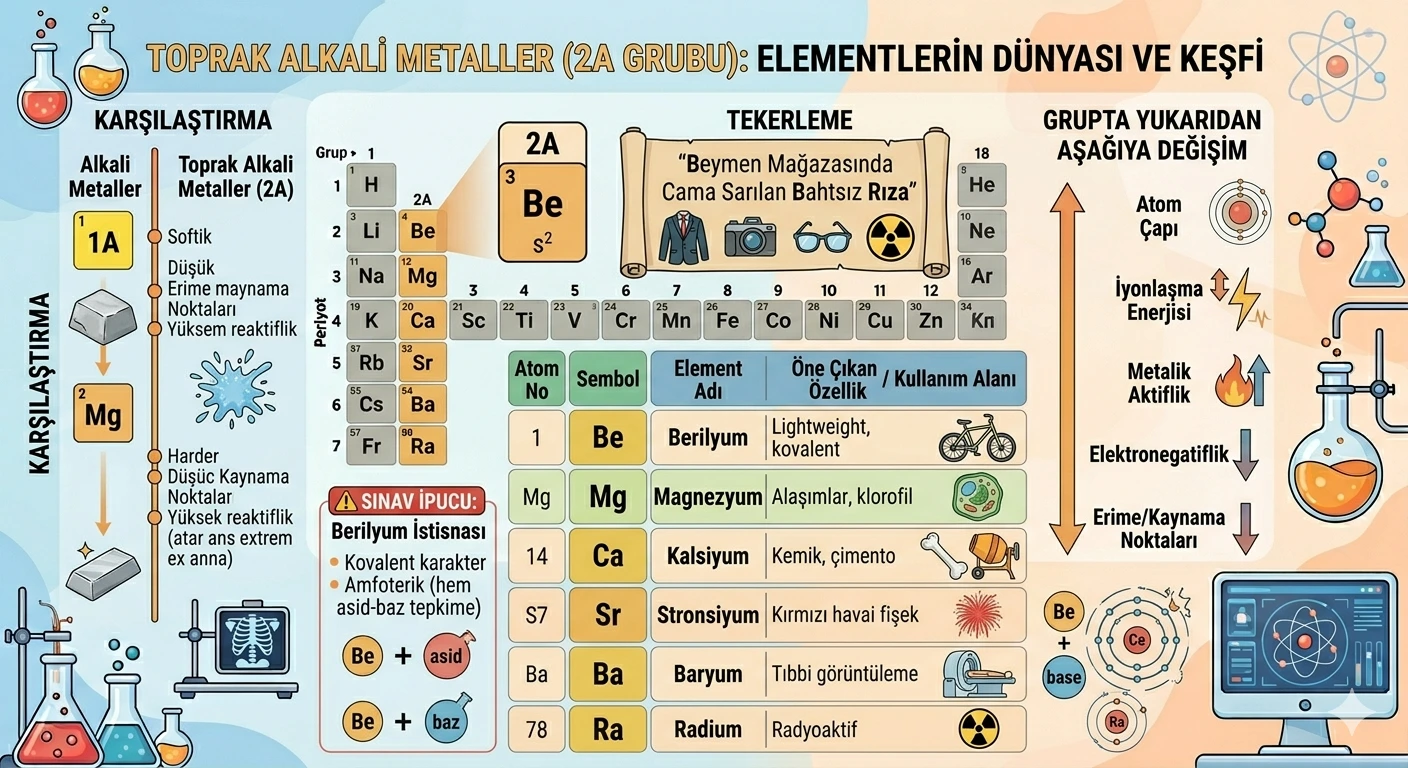
Toprak alkali metaller 2A grubunda bulunan şu elementlerden oluşur:
| Element | Sembol | Atom Numarası | Öne Çıkan Özellik / Kullanım Alanı |
|---|---|---|---|
| Berilyum | Be | 4 | Hafif ve serttir; bazı özellikleriyle grup içinde istisnadır. |
| Magnezyum | Mg | 12 | Hafif alaşımlarda ve canlılarda önemli görevlerde bulunur. |
| Kalsiyum | Ca | 20 | Kemik ve diş yapısında; kireç ve çimento üretiminde önemlidir. |
| Stronsiyum | Sr | 38 | Bazı bileşikleri havai fişeklere kırmızı renk verebilir. |
| Baryum | Ba | 56 | Baryum bileşikleri tıbbi görüntülemede kullanılabilir. |
| Radyum | Ra | 88 | Radyoaktif özellik gösterir. |
Toprak Alkali Metallerin Genel Özellikleri
- Periyodik tablonun 2A grubunda yer alırlar.
- Son katmanlarında 2 değerlik elektronu bulunur.
- Genellikle +2 yüklü iyon oluştururlar.
- Metalik özellik gösterirler.
- Isı ve elektriği iletirler.
- Alkali metallere göre genellikle daha serttirler.
- Alkali metallere göre genellikle daha az aktiftirler.
- Doğada çoğunlukla bileşikler hâlinde bulunurlar.
Toprak Alkali Metallerin Fiziksel Özellikleri
Toprak alkali metaller fiziksel özellikleri bakımından alkali metallerden daha dayanıklı olabilir. Bunun nedeni, metalik bağlarının daha güçlü olmasıyla ilişkilendirilebilir.
| Fiziksel Özellik | Açıklama | Örnek / Not |
|---|---|---|
| Fiziksel hâl | Oda sıcaklığında katı hâlde bulunurlar. | Mg, Ca, Ba |
| Sertlik | Alkali metallere göre genellikle daha serttirler. | 2A > 1A |
| Yoğunluk | Genellikle alkali metallere göre daha yoğundurlar. | Grup içinde değişebilir. |
| Erime noktası | Alkali metallere göre genellikle daha yüksektir. | Metalik bağ daha güçlüdür. |
| İletkenlik | Isı ve elektriği iletirler. | Metal özellik gösterirler. |
Toprak Alkali Metallerin Kimyasal Özellikleri
Toprak alkali metallerin kimyasal davranışları, son katmanlarında 2 elektron bulundurmalarıyla ilgilidir. Bu elektronları vererek +2 yüklü iyonlar oluşturabilirler.
| Kimyasal Özellik | Açıklama | Örnek |
|---|---|---|
| +2 iyon oluşturma | İki elektron vererek +2 yüklü katyon oluştururlar. | Mg → Mg2+ + 2e– |
| Aktiflik | Aktif metallerdir; ancak 1A grubuna göre daha az aktif olabilirler. | Ca, Ba |
| Oksit oluşturma | Oksijenle tepkimeye girerek metal oksitleri oluşturabilirler. | CaO, MgO |
| Su ile tepkime | Bazıları suyla tepkimeye girerek hidroksit ve hidrojen gazı oluşturabilir. | Ca + H2O |
Toprak Alkali Metallerin Su ile Tepkimesi
Toprak alkali metaller suyla tepkimeye girebilir; ancak bu tepkime alkali metaller kadar şiddetli değildir. Grup içinde aşağı inildikçe tepkime verme eğilimi genellikle artar.
Genel denklem: Toprak alkali metal + su → metal hidroksit + hidrojen gazı
Kalsiyumun su ile tepkimesi şu şekilde gösterilebilir:
Ca + 2H2O → Ca(OH)2 + H2
Berilyum oda sıcaklığında suyla kolay tepkime vermez. Magnezyum ise soğuk suyla çok yavaş, sıcak su veya su buharıyla daha belirgin tepkime verebilir.
Berilyum İstisnası
Berilyum, 2A grubunun en üstünde yer alır ve grubun diğer üyelerinden bazı yönleriyle ayrılır. Atom yarıçapının küçük olması ve yük yoğunluğunun yüksek olması nedeniyle bileşiklerinde daha fazla kovalent karakter görülebilir.
Berilyum ayrıca amfoter özellik gösterebilir. Yani hem asitlerle hem de kuvvetli bazlarla tepkimeye girebilir.
Sınav notu: Berilyum, 2A grubunda olmasına rağmen bazı özellikleriyle grup içinde önemli bir istisnadır.
2A Grubunda Aşağı İnildikçe Özellikler Nasıl Değişir?
Toprak alkali metallerde grupta yukarıdan aşağıya inildikçe katman sayısı artar. Buna bağlı olarak atom yarıçapı büyür, iyonlaşma enerjisi azalır ve metalik aktiflik genellikle artar.
| Özellik | Grupta Yukarıdan Aşağıya | Neden? |
|---|---|---|
| Atom yarıçapı | Artar. | Katman sayısı artar. |
| İyonlaşma enerjisi | Azalır. | Elektron çekirdekten uzaklaşır. |
| Metalik aktiflik | Artar. | Elektron verme kolaylaşır. |
| Elektronegatiflik | Genellikle azalır. | Bağ elektronlarını çekme gücü azalır. |
Alkali Metaller ve Toprak Alkali Metaller Arasındaki Farklar
| Özellik | Alkali Metaller | Toprak Alkali Metaller |
|---|---|---|
| Grup | 1A grubu | 2A grubu |
| Değerlik elektron sayısı | 1 | 2 |
| Oluşturduğu iyon | Genellikle +1 | Genellikle +2 |
| Aktiflik | Genellikle daha aktiftir. | Genellikle daha az aktiftir. |
| Sertlik | Daha yumuşaktır. | Genellikle daha serttir. |
| Örnek | Li, Na, K | Be, Mg, Ca |
Toprak Alkali Metallerin Kullanım Alanları
| Element | Kullanım Alanı | Neden Önemli? |
|---|---|---|
| Berilyum | Özel alaşımlar, bazı ileri teknoloji uygulamaları | Hafif ve serttir. |
| Magnezyum | Hafif alaşımlar, fotoğraf flaşları, canlı sistemleri | Hafif ve reaktiftir; klorofil yapısında bulunur. |
| Kalsiyum | Kemik ve diş yapısı, çimento, kireç | Canlılar ve yapı malzemeleri için önemlidir. |
| Stronsiyum | Havai fişekler | Bazı bileşikleri kırmızı renk oluşturabilir. |
| Baryum | Tıbbi görüntüleme, özel camlar | Baryum bileşikleri bazı görüntüleme işlemlerinde kullanılır. |
| Radyum | Tarihsel olarak ışıldayan boyalar ve bazı tıbbi uygulamalar | Radyoaktif özellik gösterir. |
Toprak Alkali Metaller Neden Doğada Serbest Hâlde Bulunmaz?
Toprak alkali metaller aktif oldukları için doğada genellikle serbest element hâlinde bulunmaz. Bunun yerine karbonat, sülfat, silikat veya oksit gibi bileşikler hâlinde bulunabilirler.
Örneğin kalsiyum doğada kireç taşı gibi bileşiklerde, magnezyum ise bazı minerallerde bulunur.
Sık Yapılan Hatalar
1. Toprak alkali metalleri 1A grubu sanmak
Toprak alkali metaller 2A grubunda yer alır. Alkali metaller ise 1A grubundadır.
2. 2A grubu elementlerinin +1 iyon oluşturduğunu düşünmek
Toprak alkali metaller son katmanlarında 2 elektron bulundurur ve genellikle +2 yüklü iyon oluşturur.
3. Berilyumu diğer 2A elementleriyle tamamen aynı düşünmek
Berilyum, küçük atom yarıçapı ve farklı bileşik özellikleri nedeniyle grup içinde önemli bir istisnadır.
4. Grupta aşağı indikçe aktifliğin azaldığını sanmak
Toprak alkali metallerde aşağı inildikçe iyonlaşma enerjisi azalır ve metalik aktiflik genellikle artar.
Toprak Alkali Metaller Konu Özeti
- Toprak alkali metaller 2A grubunda yer alır.
- Son katmanlarında 2 değerlik elektronu bulunur.
- Genellikle +2 yüklü iyon oluştururlar.
- Alkali metallere göre daha sert ve daha az aktiftirler.
- Doğada genellikle bileşikler hâlinde bulunurlar.
- Berilyum grup içinde önemli bir istisnadır.
- Grupta aşağı doğru inildikçe atom yarıçapı ve metalik aktiflik artar.
- Grupta aşağı doğru inildikçe iyonlaşma enerjisi genellikle azalır.
Toprak Alkali Metaller Mini Test
1. Toprak alkali metaller hangi grupta yer alır?
- A) 1A
- B) 2A
- C) 7A
- D) 8A
Doğru cevap: B
Açıklama: Toprak alkali metaller periyodik tablonun 2A grubunda yer alır.
2. Toprak alkali metaller genellikle kaç değerlik elektronuna sahiptir?
- A) 1
- B) 2
- C) 7
- D) 8
Doğru cevap: B
Açıklama: 2A grubu elementlerinin son katmanında 2 değerlik elektronu bulunur.
3. Toprak alkali metaller genellikle hangi yüklü iyonu oluşturur?
- A) +1
- B) +2
- C) -1
- D) -2
Doğru cevap: B
Açıklama: Toprak alkali metaller iki elektron vererek genellikle +2 yüklü iyon oluşturur.
4. Aşağıdakilerden hangisi toprak alkali metaldir?
- A) Sodyum
- B) Potasyum
- C) Kalsiyum
- D) Klor
Doğru cevap: C
Açıklama: Kalsiyum 2A grubunda yer alan bir toprak alkali metaldir.
5. Berilyum için aşağıdakilerden hangisi doğrudur?
- A) Grup içinde bazı istisna özellikler gösterir.
- B) 1A grubunda yer alır.
- C) Genellikle -1 iyon oluşturur.
- D) Soygazdır.
Doğru cevap: A
Açıklama: Berilyum, küçük atom yarıçapı ve bazı bileşik özellikleri nedeniyle 2A grubunda istisna kabul edilir.
Sıkça Sorulan Sorular
Toprak alkali metal nedir?
Toprak alkali metal, periyodik tablonun 2A grubunda yer alan ve genellikle +2 yüklü iyon oluşturan metal elementtir.
Toprak alkali metaller hangileridir?
Berilyum, magnezyum, kalsiyum, stronsiyum, baryum ve radyum toprak alkali metallerdir.
Toprak alkali metaller kaç değerlik elektronu taşır?
Toprak alkali metaller son katmanlarında 2 değerlik elektronu taşır.
Toprak alkali metaller hangi iyonu oluşturur?
Genellikle iki elektron vererek +2 yüklü iyon oluştururlar.
Berilyum neden istisnadır?
Berilyum küçük atom yarıçapı ve yüksek yük yoğunluğu nedeniyle grup içinde farklı özellikler gösterebilir. Bileşiklerinde daha fazla kovalent karakter görülebilir.
Toprak alkali metaller doğada serbest hâlde bulunur mu?
Genellikle hayır. Aktif oldukları için doğada çoğunlukla bileşikler hâlinde bulunurlar.
Bu Konudan Sonra Ne Öğrenmeliyim?
Toprak alkali metaller konusunu öğrendikten sonra şu konulara geçebilirsin:
Bu konu şu rehberin parçasıdır: Atom ve Periyodik Sistem
