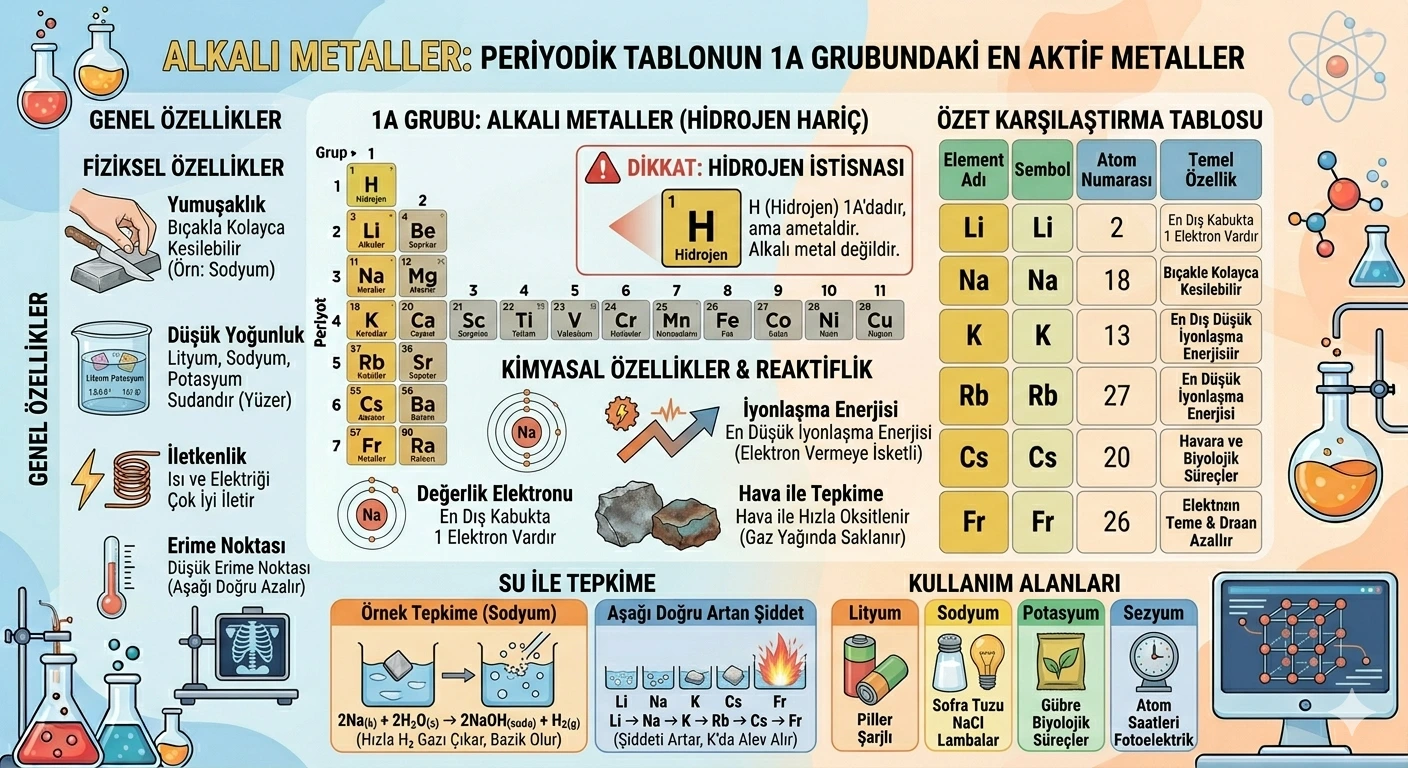
Alkali metaller, periyodik tablonun en sol sütununda yer alan 1A grubu elementleridir. Bu elementler son katmanlarında 1 elektron bulundurur ve bu elektronu kolayca vererek +1 yüklü iyon oluşturma eğilimindedir.
Kimyasal olarak oldukça aktif olan alkali metaller doğada genellikle saf hâlde bulunmaz. Bunun yerine bileşikler hâlinde bulunurlar. Sodyumun sofra tuzunda, potasyumun gübrelerde ve lityumun bataryalarda önemli kullanım alanları vardır.
Önemli bilgi: Hidrojen 1A grubunda yer alır; ancak alkali metal değildir. Hidrojen bir ametaldir.
Alkali Metal Nedir?
Alkali metal, periyodik tablonun 1A grubunda yer alan ve metalik özellik gösteren elementlere verilen addır. Bu elementlerin ortak özelliği, son katmanlarında 1 değerlik elektronu bulundurmalarıdır.
Alkali metaller bu tek elektronu vererek kararlı hâle geçme eğilimindedir. Bu nedenle genellikle +1 yüklü katyon oluştururlar.
Bu konuyu daha iyi anlamak için önce Periyodik Tablo Nedir?, Metal Nedir? ve İyonlaşma Enerjisi Nedir? yazılarını inceleyebilirsin.
Alkali Metaller Hangileridir?
1A grubunda hidrojen de yer alır; ancak hidrojen alkali metal değildir. Alkali metal olarak kabul edilen elementler şunlardır:
| Element | Sembol | Atom Numarası | Öne Çıkan Özellik |
|---|---|---|---|
| Lityum | Li | 3 | En hafif metallerden biridir; bataryalarda önemlidir. |
| Sodyum | Na | 11 | Sofra tuzu bileşiğinde bulunur. |
| Potasyum | K | 19 | Canlılarda ve gübrelerde önemlidir. |
| Rubidyum | Rb | 37 | Çok aktif bir alkali metaldir. |
| Sezyum | Cs | 55 | Atom saatlerinde kullanılabilir. |
| Fransiyum | Fr | 87 | Radyoaktif ve çok nadir bulunan alkali metaldir. |
Hidrojen Neden Alkali Metal Değildir?
Hidrojen periyodik tablonun 1A grubunda gösterilir; çünkü son katmanında 1 elektron bulunur. Ancak hidrojen metalik özellik göstermez.
Hidrojen oda koşullarında gaz hâlindedir, ametal özellik gösterir ve alkali metaller gibi yumuşak, parlak, iletken bir metal değildir.
Sınav notu: 1A grubunda yer alan hidrojen, alkali metal değildir. Hidrojen ametaldir.
Alkali Metallerin Genel Özellikleri
- Periyodik tablonun 1A grubunda yer alırlar.
- Son katmanlarında 1 değerlik elektronu bulunur.
- Bu elektronu vererek +1 yüklü iyon oluştururlar.
- Çok aktif metallerdir.
- Doğada genellikle saf hâlde bulunmazlar.
- Yumuşak metaller oldukları için bıçakla kesilebilirler.
- Isı ve elektriği iyi iletirler.
- Su ile tepkimeye girerek bazik çözelti ve hidrojen gazı oluşturabilirler.
Alkali Metallerin Fiziksel Özellikleri
Alkali metaller fiziksel özellikleri bakımından diğer metallerden bazı yönleriyle ayrılır. Özellikle yumuşak olmaları ve düşük yoğunlukları dikkat çeker.
| Fiziksel Özellik | Açıklama | Örnek / Not |
|---|---|---|
| Yumuşaklık | Birçok alkali metal bıçakla kesilebilecek kadar yumuşaktır. | Sodyum, potasyum |
| Yoğunluk | Yoğunlukları birçok metale göre düşüktür. | Lityum, sodyum ve potasyum sudan daha düşük yoğunluklu olabilir. |
| İletkenlik | Metalik yapı nedeniyle ısı ve elektriği iletirler. | Metal özellik gösterirler. |
| Erime noktası | Birçok metale göre daha düşük erime noktasına sahiptirler. | Grupta aşağı indikçe genellikle azalır. |
Alkali Metallerin Kimyasal Özellikleri
Alkali metallerin kimyasal özelliklerinin temel nedeni, son katmanlarında 1 elektron bulundurmalarıdır. Bu elektronu kolayca verdikleri için oldukça reaktiftirler.
| Kimyasal Özellik | Açıklama | Örnek |
|---|---|---|
| +1 iyon oluşturma | Bir elektron vererek +1 yüklü katyon oluştururlar. | Na → Na+ + e– |
| Düşük iyonlaşma enerjisi | Elektronlarını kolay verirler. | Sodyum ve potasyum aktiftir. |
| İndirgen özellik | Elektron verme eğilimleri yüksek olduğu için indirgen özellik gösterirler. | Alkali metaller güçlü indirgen olabilir. |
| Su ile tepkime | Su ile tepkimeye girerek baz ve hidrojen gazı oluştururlar. | Na + H2O tepkimesi |
Alkali Metallerin Su ile Tepkimesi
Alkali metaller suyla tepkimeye girerek metal hidroksit ve hidrojen gazı oluşturur. Oluşan metal hidroksit çözeltisi bazik özellik gösterir.
Genel denklem: Alkali metal + su → metal hidroksit + hidrojen gazı
Sodyumun su ile tepkimesi şu şekilde gösterilebilir:
2Na + 2H2O → 2NaOH + H2
Bu tepkime ekzotermiktir; yani ısı açığa çıkar. Grupta aşağı doğru inildikçe tepkimenin şiddeti genellikle artar.
Alkali Metallerin Aktifliği Nasıl Değişir?
Alkali metallerde grupta yukarıdan aşağıya inildikçe atom yarıçapı artar. Son katmandaki elektron çekirdekten uzaklaştığı için daha kolay koparılır.
Bu nedenle alkali metallerde grupta aşağıya doğru inildikçe metalik aktiflik genellikle artar.
| Yön | Atom Yarıçapı | İyonlaşma Enerjisi | Metalik Aktiflik |
|---|---|---|---|
| 1A grubunda aşağı doğru | Artar. | Azalır. | Artar. |
Kısa kural: Alkali metallerde aşağı indikçe elektron vermek kolaylaşır ve aktiflik artar.
Alkali Metaller Neden Doğada Saf Hâlde Bulunmaz?
Alkali metaller çok aktif oldukları için hava, su ve diğer maddelerle kolayca tepkimeye girer. Bu nedenle doğada saf element hâlinde değil, genellikle bileşikler hâlinde bulunurlar.
Örneğin sodyum doğada sofra tuzu olarak bilinen sodyum klorür bileşiğinde bulunabilir.
Alkali Metaller Nasıl Saklanır?
Alkali metaller hava ve nemle kolayca tepkimeye girebildiği için özel koşullarda saklanır. Laboratuvarlarda bazı alkali metaller gaz yağı veya parafin içinde saklanabilir.
Bu saklama yöntemi, metalin hava ve su buharıyla temasını azaltmak için kullanılır.
Alkali Metallerin Kullanım Alanları
| Alkali Metal | Kullanım Alanı | Neden Önemli? |
|---|---|---|
| Lityum | Şarj edilebilir bataryalar | Hafif ve yüksek enerji depolama kapasitesine sahiptir. |
| Sodyum | Sofra tuzu, bazı lambalar | Bileşikleri günlük hayatta yaygındır. |
| Potasyum | Gübreler, canlı sistemleri | Bitki gelişimi ve canlılarda iyon dengesi için önemlidir. |
| Sezyum | Atom saatleri | Hassas zaman ölçümünde kullanılabilir. |
Alkali Metaller ve Toprak Alkali Metaller Arasındaki Fark
| Özellik | Alkali Metaller | Toprak Alkali Metaller |
|---|---|---|
| Grup | 1A grubu | 2A grubu |
| Değerlik elektron sayısı | 1 | 2 |
| Oluşturduğu iyon | Genellikle +1 | Genellikle +2 |
| Aktiflik | Genellikle daha aktiftir. | Alkali metallere göre daha az aktif olabilir. |
| Örnek | Li, Na, K | Mg, Ca, Ba |
Sık Yapılan Hatalar
1. Hidrojeni alkali metal sanmak
Hidrojen 1A grubunda yer alır; ancak alkali metal değildir. Hidrojen ametaldir.
2. Alkali metallerin doğada saf hâlde yaygın bulunduğunu düşünmek
Alkali metaller çok reaktif oldukları için doğada genellikle bileşikler hâlinde bulunur.
3. Alkali metallerin +2 iyon oluşturduğunu sanmak
Alkali metaller son katmanlarında 1 elektron bulundurur ve genellikle +1 iyon oluşturur.
4. Grupta aşağı indikçe aktifliğin azaldığını düşünmek
Alkali metallerde aşağı inildikçe atom yarıçapı artar, iyonlaşma enerjisi azalır ve aktiflik genellikle artar.
Alkali Metaller Konu Özeti
- Alkali metaller 1A grubunda yer alır.
- Hidrojen alkali metal değildir.
- Alkali metallerin son katmanında 1 elektron bulunur.
- Genellikle +1 yüklü iyon oluştururlar.
- Çok aktif metallerdir.
- Doğada genellikle bileşikler hâlinde bulunurlar.
- Suyla tepkimeye girerek metal hidroksit ve hidrojen gazı oluşturabilirler.
- Grupta aşağı doğru inildikçe aktiflik genellikle artar.
Alkali Metaller Mini Test
1. Alkali metaller periyodik tabloda hangi grupta yer alır?
- A) 1A
- B) 2A
- C) 7A
- D) 8A
Doğru cevap: A
Açıklama: Alkali metaller periyodik tablonun 1A grubunda yer alır.
2. Aşağıdakilerden hangisi alkali metal değildir?
- A) Lityum
- B) Sodyum
- C) Potasyum
- D) Hidrojen
Doğru cevap: D
Açıklama: Hidrojen 1A grubunda yer alır; ancak alkali metal değil, ametaldir.
3. Alkali metaller genellikle kaç değerlik elektronuna sahiptir?
- A) 1
- B) 2
- C) 7
- D) 8
Doğru cevap: A
Açıklama: Alkali metallerin son katmanında genellikle 1 değerlik elektronu bulunur.
4. Alkali metaller genellikle hangi yüklü iyonu oluşturur?
- A) +1
- B) +2
- C) -1
- D) -2
Doğru cevap: A
Açıklama: Alkali metaller 1 elektron vererek genellikle +1 yüklü iyon oluşturur.
5. Alkali metallerde grupta aşağı inildikçe aktiflik genellikle nasıl değişir?
- A) Artar
- B) Azalır
- C) Değişmez
- D) Tamamen yok olur
Doğru cevap: A
Açıklama: Grupta aşağı inildikçe iyonlaşma enerjisi azalır ve elektron vermek kolaylaştığı için aktiflik genellikle artar.
Sıkça Sorulan Sorular
Alkali metal nedir?
Alkali metal, periyodik tablonun 1A grubunda yer alan ve genellikle +1 yüklü iyon oluşturan aktif metaldir.
Alkali metaller hangileridir?
Lityum, sodyum, potasyum, rubidyum, sezyum ve fransiyum alkali metallerdir. Hidrojen alkali metal değildir.
Hidrojen alkali metal midir?
Hayır. Hidrojen 1A grubunda yer almasına rağmen alkali metal değildir; ametaldir.
Alkali metaller neden doğada saf hâlde bulunmaz?
Çok aktif oldukları için hava, su ve diğer maddelerle kolayca tepkimeye girerler. Bu nedenle doğada genellikle bileşikler hâlinde bulunurlar.
Alkali metaller suyla tepkime verir mi?
Evet. Alkali metaller suyla tepkimeye girerek metal hidroksit ve hidrojen gazı oluşturabilir.
En aktif alkali metal hangisidir?
Grupta aşağı inildikçe aktiflik genellikle artar. Fransiyum teorik olarak en aktif alkali metaldir; ancak radyoaktif ve çok nadirdir.
Bu Konudan Sonra Ne Öğrenmeliyim?
Alkali metaller konusunu öğrendikten sonra şu konulara geçebilirsin:
Bu konu şu rehberin parçasıdır: Atom ve Periyodik Sistem
