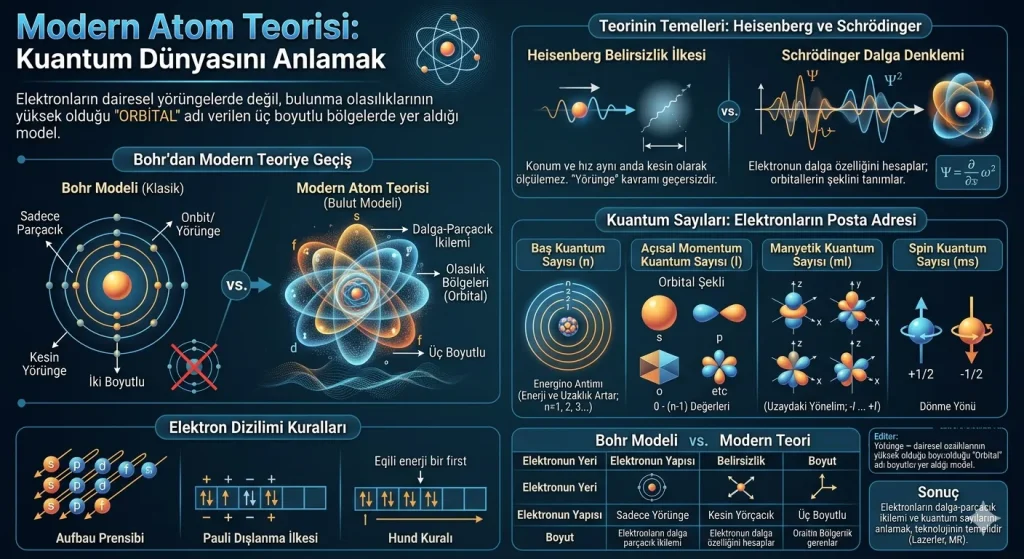
Modern atom teorisi, atomun yapısını günümüzde en iyi açıklayan modellerden biridir. Bu teoriye göre elektronlar, çekirdek etrafında gezegenler gibi belirli dairesel yörüngelerde dolaşmaz. Bunun yerine elektronların atom içinde bulunma olasılığının yüksek olduğu bölgeler vardır.
Bu bölgelere orbital denir. Modern atom teorisi, elektronların hem parçacık hem de dalga özelliği gösterebildiğini kabul eder. Bu nedenle elektronların konumu kesin çizgilerle değil, olasılıklarla açıklanır.
Önemli bilgi: Modern atom teorisinde elektronun kesin yeri değil, bulunma olasılığının yüksek olduğu bölge açıklanır.
Modern Atom Teorisi Nedir?
Modern atom teorisi, elektronların atom içindeki davranışını kuantum mekaniği ilkeleriyle açıklayan atom modelidir. Bu modele göre elektronların hem yeri hem de hızı aynı anda kesin olarak bilinemez.
Elektronlar, çekirdek çevresinde belirli enerji düzeylerinde ve orbitallerde bulunur. Orbitaller elektronların bulunma ihtimalinin yüksek olduğu üç boyutlu bölgelerdir.
Bu konuyu daha iyi anlamak için önce Atom Nedir?, Orbital Nedir? ve Değerlik Elektron Nedir? yazılarını inceleyebilirsin.
Modern Atom Teorisine Neden İhtiyaç Duyuldu?
Önceki atom modelleri, atomun yapısını açıklamada önemli adımlar atmıştır. Ancak özellikle çok elektronlu atomların davranışını, atom spektrumlarını ve elektronların dalga özelliğini açıklamada yetersiz kalmıştır.
Bohr atom modeli, elektronların belirli dairesel yörüngelerde bulunduğunu ileri sürüyordu. Bu model hidrojen atomunu açıklamada başarılı olsa da çok elektronlu atomları açıklamada yeterli değildi.
Modern atom teorisi, elektronların kesin yörüngelerde değil, olasılık bölgelerinde bulunduğunu savunarak bu eksiklikleri daha iyi açıklamıştır.
Bohr Atom Modeli ve Modern Atom Teorisi Farkı
| Özellik | Bohr Atom Modeli | Modern Atom Teorisi |
|---|---|---|
| Elektronun yeri | Belirli dairesel yörüngelerde bulunur. | Bulunma olasılığının yüksek olduğu orbitallerde bulunur. |
| Elektron hareketi | Gezegen benzeri hareketle açıklanır. | Dalga-parçacık özelliğiyle açıklanır. |
| Kesinlik | Elektronun yeri daha kesin düşünülür. | Elektronun yeri olasılıkla ifade edilir. |
| Boyut | Yörünge daha çok çizgisel/dairesel düşünülür. | Orbital üç boyutlu bölgedir. |
| Kapsam | Hidrojen atomunu açıklamada başarılıdır. | Çok elektronlu atomları açıklamada daha güçlüdür. |
Bohr atom modelini tekrar etmek için Bohr Atom Modeli yazısına geçebilirsin.
Yörünge ve Orbital Arasındaki Fark
Modern atom teorisini anlamak için yörünge ve orbital kavramlarını ayırmak gerekir.
| Kavram | Açıklama | Hangi Modelle İlişkili? |
|---|---|---|
| Yörünge | Elektronun belirli bir çizgi üzerinde döndüğünü varsayar. | Bohr atom modeli |
| Orbital | Elektronun bulunma olasılığının yüksek olduğu bölgedir. | Modern atom teorisi |
Dikkat: Orbital, elektronun izlediği kesin yol değildir. Elektronun bulunma olasılığının yüksek olduğu bölgedir.
Elektron Bulutu Modeli Nedir?
Modern atom teorisi bazen elektron bulutu modeli olarak da adlandırılır. Bunun nedeni, elektronların çekirdek etrafında net bir çizgi üzerinde değil, olasılık dağılımı şeklinde açıklanmasıdır.
Elektronun bulunma ihtimalinin yüksek olduğu bölgeler daha yoğun bir bulut gibi düşünülebilir. Bu ifade, elektronun tam konumunu değil, olasılık dağılımını anlatır.
Heisenberg Belirsizlik İlkesi
Heisenberg belirsizlik ilkesine göre bir elektronun konumu ve momentumu aynı anda kesin olarak bilinemez. Elektronun yerini çok hassas belirlemeye çalışmak, onun hareketiyle ilgili bilgiyi belirsizleştirir.
Bu ilke, elektronların atom içinde kesin yörüngeler izlediği düşüncesinin modern teoriyle neden uyuşmadığını açıklar.
Kısa açıklama: Elektronun hem yerini hem de hızını aynı anda kesin bilmek mümkün değildir.
Schrödinger Dalga Denklemi
Schrödinger dalga denklemi, elektronların atom içindeki davranışını dalga mekaniğiyle açıklayan matematiksel bir yaklaşımdır. Bu denklem, elektronun bulunma olasılığını ve orbitallerin yapısını anlamamıza yardım eder.
Denklemin çözümleri, elektronların atom içinde hangi enerji düzeylerinde ve hangi orbitallerde bulunabileceğini gösterir.
Kuantum Sayıları Nedir?
Kuantum sayıları, bir elektronun atom içindeki enerji düzeyini, orbital türünü, orbitalin yönelimini ve spin durumunu tanımlayan sayılardır.
Bir elektronu tanımlamak için dört kuantum sayısı kullanılır:
- Baş kuantum sayısı
- Açısal momentum kuantum sayısı
- Manyetik kuantum sayısı
- Spin kuantum sayısı
Kuantum Sayıları Tablosu
| Kuantum Sayısı | Sembol | Ne Anlama Gelir? | Basit Açıklama |
|---|---|---|---|
| Baş kuantum sayısı | n | Enerji düzeyi ve çekirdeğe ortalama uzaklık | Katman numarası gibi düşünülebilir. |
| Açısal momentum kuantum sayısı | l | Orbital türü ve şekli | s, p, d, f orbital türünü belirler. |
| Manyetik kuantum sayısı | ml | Orbitalin uzaydaki yönelimi | Orbitalin hangi yönde bulunduğunu ifade eder. |
| Spin kuantum sayısı | ms | Elektronun spin yönü | +1/2 veya -1/2 değerini alabilir. |
Baş Kuantum Sayısı
Baş kuantum sayısı n ile gösterilir. Elektronun temel enerji düzeyini ve çekirdeğe olan ortalama uzaklığını ifade eder.
n değeri arttıkça elektronun enerjisi ve çekirdeğe ortalama uzaklığı genellikle artar.
- n = 1
- n = 2
- n = 3
- n = 4
Açısal Momentum Kuantum Sayısı
Açısal momentum kuantum sayısı l ile gösterilir. Orbitalin türünü ve şeklini belirler.
| l Değeri | Orbital Türü | Orbital Kapasitesi |
|---|---|---|
| 0 | s | 2 elektron |
| 1 | p | 6 elektron |
| 2 | d | 10 elektron |
| 3 | f | 14 elektron |
Manyetik Kuantum Sayısı
Manyetik kuantum sayısı ml ile gösterilir. Orbitalin uzaydaki yönelimini ifade eder.
ml değeri -l ile +l arasında değerler alabilir. Örneğin p orbitalleri için l = 1 olduğundan ml değerleri -1, 0 ve +1 olabilir. Bu da p alt kabuğunda 3 orbital olduğunu gösterir.
Spin Kuantum Sayısı
Spin kuantum sayısı ms ile gösterilir. Elektronun spin yönünü ifade eder.
Spin kuantum sayısı +1/2 veya -1/2 değerini alabilir. Bir orbitalde en fazla iki elektron bulunabilir ve bu iki elektronun spinleri zıt olmalıdır.
Elektron Dizilimi Kuralları
Elektronlar orbitallere rastgele yerleşmez. Elektron dizilimi yapılırken belirli kurallar kullanılır.
| Kural | Açıklama | Kısa Anlamı |
|---|---|---|
| Aufbau prensibi | Elektronlar önce düşük enerjili orbitallere yerleşir. | En düşük enerjiden başlanır. |
| Pauli dışlanma ilkesi | Bir orbitalde en fazla iki elektron bulunur ve spinleri zıt olur. | Bir orbital en fazla iki elektron alır. |
| Hund kuralı | Eş enerjili orbitallere elektronlar önce tek tek yerleşir. | Önce boş orbitaller tek tek dolar. |
n + l Kuralı Nedir?
n + l kuralı, orbitallerin enerji sırasını belirlemede kullanılan bir kuraldır. n + l değeri küçük olan orbitalin enerjisi genellikle daha düşüktür.
Eğer iki orbitalin n + l değeri eşitse, baş kuantum sayısı yani n değeri küçük olan orbital daha düşük enerjilidir.
Örnek: 4s ve 3d orbitalleri karşılaştırılırken n + l kuralı kullanılabilir.
Modern Atom Teorisi ve Kimyasal Bağlar
Modern atom teorisi, kimyasal bağların neden ve nasıl oluştuğunu anlamak için önemlidir. Çünkü bağ oluşumunda elektronların orbitallerdeki yerleşimi, değerlik elektron sayısı ve atomların kararlı hale gelme eğilimi etkilidir.
Örneğin kovalent bağlarda atomlar değerlik elektronlarını ortaklaşa kullanır. İyonik bağlarda ise elektron alışverişi gerçekleşir.
Bu konuyu detaylı öğrenmek için Kimyasal Bağ Nedir? yazısına geçebilirsin.
Modern Atom Teorisi Nerelerde Kullanılır?
Modern atom teorisi yalnızca kimya derslerinde değil, birçok bilimsel ve teknolojik alanda temel öneme sahiptir.
| Alan | Modern Atom Teorisiyle İlişkisi |
|---|---|
| Kimyasal bağlar | Bağ oluşumunu ve elektron paylaşımını açıklar. |
| Yarı iletkenler | Elektronların enerji düzeyleri teknolojik malzemeleri anlamada kullanılır. |
| Lazerler | Elektronların enerji geçişleriyle ilişkilidir. |
| Spektroskopi | Atomların ışıkla etkileşimini açıklar. |
| Manyetik rezonans | Atom altı parçacıkların davranışlarını anlamaya dayanır. |
Sık Yapılan Hatalar
1. Elektronların kesin yörüngelerde döndüğünü sanmak
Modern atom teorisine göre elektronlar kesin çizgisel yörüngelerde değil, bulunma olasılığı yüksek orbitallerde yer alır.
2. Orbital ile yörüngeyi aynı sanmak
Yörünge belirli bir çizgisel yolu, orbital ise elektronun bulunma olasılığının yüksek olduğu üç boyutlu bölgeyi ifade eder.
3. Kuantum sayılarını sadece ezberlemek
Kuantum sayıları elektronun atom içindeki enerji düzeyini, orbital türünü, yönelimini ve spinini açıklamak için kullanılır.
4. Bir orbitalde üç elektron bulunabileceğini düşünmek
Pauli dışlanma ilkesine göre bir orbitalde en fazla iki elektron bulunabilir.
Modern Atom Teorisi Konu Özeti
- Modern atom teorisi elektronları olasılık bölgeleriyle açıklar.
- Elektronlar kesin yörüngelerde değil, orbitallerde bulunur.
- Orbital, elektronun bulunma olasılığının yüksek olduğu bölgedir.
- Heisenberg belirsizlik ilkesine göre elektronun konumu ve momentumu aynı anda kesin bilinemez.
- Schrödinger dalga denklemi orbitallerin anlaşılmasına katkı sağlar.
- Elektronlar dört kuantum sayısıyla tanımlanır.
- Elektron diziliminde Aufbau, Pauli ve Hund kuralları kullanılır.
- Modern atom teorisi kimyasal bağların anlaşılması için önemlidir.
Modern Atom Teorisi Mini Test
1. Modern atom teorisine göre elektronlar nerede bulunur?
- A) Kesin dairesel yörüngelerde
- B) Bulunma olasılığının yüksek olduğu orbitallerde
- C) Atom çekirdeğinin içinde
- D) Sadece protonların üzerinde
Doğru cevap: B
Açıklama: Modern atom teorisine göre elektronlar orbitallerde, yani bulunma olasılığının yüksek olduğu bölgelerde yer alır.
2. Orbital nedir?
- A) Elektronun kesin çizgisel yolu
- B) Elektronun bulunma olasılığının yüksek olduğu bölge
- C) Proton ve nötron toplamı
- D) Sadece atom çekirdeği
Doğru cevap: B
Açıklama: Orbital, elektronun bulunma olasılığının yüksek olduğu üç boyutlu bölgedir.
3. Heisenberg belirsizlik ilkesine göre hangisi doğrudur?
- A) Elektronun konumu ve momentumu aynı anda kesin olarak bilinemez.
- B) Elektronlar çekirdekte sabit durur.
- C) Her orbital üç elektron alır.
- D) Atomda elektron bulunmaz.
Doğru cevap: A
Açıklama: Heisenberg belirsizlik ilkesine göre elektronun konumu ve momentumu aynı anda kesin bilinemez.
4. Bir orbitalde en fazla kaç elektron bulunabilir?
- A) 1
- B) 2
- C) 6
- D) 10
Doğru cevap: B
Açıklama: Pauli dışlanma ilkesine göre bir orbitalde en fazla iki elektron bulunabilir.
5. Orbitalin şeklini hangi kuantum sayısı belirler?
- A) Baş kuantum sayısı
- B) Açısal momentum kuantum sayısı
- C) Spin kuantum sayısı
- D) Kütle numarası
Doğru cevap: B
Açıklama: Açısal momentum kuantum sayısı orbital türünü ve şeklini belirler.
Sıkça Sorulan Sorular
Modern atom teorisi nedir?
Modern atom teorisi, elektronların kesin yörüngelerde değil, bulunma olasılıklarının yüksek olduğu orbitallerde yer aldığını açıklayan atom modelidir.
Modern atom teorisine neden elektron bulutu modeli denir?
Elektronların kesin konumu bilinmediği için çekirdek çevresinde bulunma olasılıkları bir bulut gibi düşünülür. Bu nedenle elektron bulutu modeli adı kullanılır.
Orbital nedir?
Orbital, elektronun atom içinde bulunma olasılığının yüksek olduğu üç boyutlu bölgedir.
Heisenberg belirsizlik ilkesi nedir?
Bir elektronun konumu ve momentumu aynı anda kesin olarak bilinemez.
Kuantum sayıları ne işe yarar?
Kuantum sayıları elektronun enerji düzeyini, orbital türünü, orbitalin yönelimini ve spin durumunu tanımlar.
Modern atom teorisi Bohr modelinden nasıl farklıdır?
Bohr modeli elektronların belirli yörüngelerde bulunduğunu söylerken, modern atom teorisi elektronların orbitallerde olasılıksal olarak bulunduğunu açıklar.
Bu Konudan Sonra Ne Öğrenmeliyim?
Modern atom teorisini öğrendikten sonra şu konulara geçebilirsin:
Bu konu şu rehberin parçasıdır: Atom ve Periyodik Sistem
