
Kısa cevap: Orbital, elektronun atom içinde bulunma olasılığının yüksek olduğu üç boyutlu bölgedir. Elektronlar kesin çizgilerle belirlenmiş yörüngelerde değil, bulunma ihtimali yüksek olan orbitallerde yer alır. Başlıca orbital türleri s, p, d ve f orbitalleridir.
Orbital kavramı, modern atom teorisinin temel konularından biridir. Eski atom modellerinde elektronların çekirdek çevresinde belirli yörüngelerde döndüğü düşünülüyordu. Modern yaklaşıma göre ise elektronun nerede bulunacağı kesin olarak değil, olasılıkla ifade edilir.
Bu nedenle orbital, elektronun atom içinde bulunma ihtimalinin yüksek olduğu bölge olarak tanımlanır. Orbitallerin şekli, enerjisi ve alabileceği elektron sayısı farklıdır.
Önemli bilgi: Orbital, elektronun kesin yolu değildir. Elektronun bulunma olasılığının yüksek olduğu bölgedir.
Orbital Nedir?
Orbital, atom çekirdeği çevresinde elektronların bulunma olasılığının yüksek olduğu üç boyutlu bölgedir. Elektronlar atom içinde rastgele dağılmaz; belirli enerji düzeylerine ve orbital türlerine göre yerleşir.
Orbital kavramı, elektronların atom içindeki dağılımını, atomların kimyasal davranışlarını ve bağ oluşumunu anlamada kullanılır. Özellikle elektron dizilimi, değerlik elektron, periyodik tablo ve kimyasal bağ konularıyla yakından ilişkilidir.
Bu konuyu daha iyi anlamak için önce Atom Nedir?, Değerlik Elektron Nedir? ve Periyodik Tablo Nedir? yazılarını inceleyebilirsin.
Orbital ve Yörünge Aynı Şey mi?
Orbital ve yörünge aynı kavram değildir. Yörünge, elektronun belirli bir çizgi üzerinde hareket ettiği eski modele ait bir düşüncedir. Orbital ise elektronun bulunma olasılığının yüksek olduğu bölgedir.
| Kavram | Açıklama | Yaklaşım |
|---|---|---|
| Yörünge | Elektronun belirli bir çizgide döndüğünü varsayar. | Bohr atom modeli |
| Orbital | Elektronun bulunma olasılığının yüksek olduğu bölgeyi ifade eder. | Modern atom teorisi |
Orbital Türleri Nelerdir?
Atomlarda başlıca dört orbital türü bulunur:
- s orbitali
- p orbitalleri
- d orbitalleri
- f orbitalleri
Bu orbitallerin şekilleri, bulunabildikleri enerji düzeyleri ve alabilecekleri elektron sayıları farklıdır.
s Orbitali
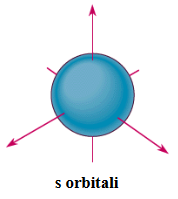
s orbitali küresel şekle sahiptir. Her enerji düzeyinde bir tane s orbitali bulunabilir ve bir s orbitali en fazla 2 elektron alır.
- Küresel şekillidir.
- Her enerji düzeyinde bulunabilir.
- En fazla 2 elektron alır.
- İkincil kuantum sayısı l = 0 değerine karşılık gelir.
p Orbitalleri

p orbitalleri ikinci enerji düzeyinden itibaren bulunur. p alt kabuğunda üç orbital vardır: px, py ve pz. Bu üç orbital toplamda en fazla 6 elektron alabilir.
- İkinci ve daha üst enerji düzeylerinde bulunur.
- Üç orbitalden oluşur.
- px, py ve pz şeklinde gösterilir.
- Toplamda en fazla 6 elektron alır.
- İkincil kuantum sayısı l = 1 değerine karşılık gelir.
d Orbitalleri

d orbitalleri üçüncü enerji düzeyinden itibaren bulunur. d alt kabuğunda 5 orbital vardır ve toplamda en fazla 10 elektron alabilir.
- Üçüncü ve daha üst enerji düzeylerinde bulunur.
- 5 orbitalden oluşur.
- Toplamda en fazla 10 elektron alır.
- Geçiş metalleriyle yakından ilişkilidir.
- İkincil kuantum sayısı l = 2 değerine karşılık gelir.
d orbitalleri özellikle Geçiş Metalleri konusunu anlamada önemlidir.
f Orbitalleri

f orbitalleri dördüncü enerji düzeyinden itibaren bulunur. f alt kabuğunda 7 orbital vardır ve toplamda en fazla 14 elektron alabilir.
- Dördüncü ve daha üst enerji düzeylerinde bulunur.
- 7 orbitalden oluşur.
- Toplamda en fazla 14 elektron alır.
- İç geçiş metalleriyle ilişkilidir.
- İkincil kuantum sayısı l = 3 değerine karşılık gelir.
Orbital Kapasiteleri
| Orbital Türü | Orbital Sayısı | Bir Orbitalin Alabileceği Elektron | Toplam Elektron Kapasitesi |
|---|---|---|---|
| s | 1 | 2 | 2 |
| p | 3 | 2 | 6 |
| d | 5 | 2 | 10 |
| f | 7 | 2 | 14 |
Orbitallere Elektron Dağılımı
Atom numarası bilinen bir atomun elektronlarının orbitallere yerleştirilmesine elektron dizilimi denir. Elektron dizilimi yapılırken elektronlar belirli kurallara göre orbitallere yerleştirilir.
Orbital gösteriminde orbitalin önüne enerji düzeyi, yanına orbital türü, sağ üst kısmına ise o orbitaldeki elektron sayısı yazılır.

Elektron Dizilimi Kuralları
Elektronların orbitallere yerleştirilmesinde üç temel kural kullanılır:
| Kural | Açıklama | Basit Anlamı |
|---|---|---|
| Aufbau Kuralı | Elektronlar önce düşük enerjili orbitallere yerleşir. | En düşük enerjiden başlanır. |
| Pauli İlkesi | Bir orbitalde en fazla iki elektron bulunur ve spinleri zıt olur. | Bir kutucukta en fazla iki elektron vardır. |
| Hund Kuralı | Eş enerjili orbitallere elektronlar önce tek tek yerleşir. | Önce boş kutular tek tek doldurulur. |
Aufbau Kuralı
Aufbau kuralına göre elektronlar önce en düşük enerjili orbitalden başlayarak daha yüksek enerjili orbitallere doğru yerleşir.
Örneğin elektron dizilimi yazılırken genellikle 1s orbitalinden başlanır.
Pauli İlkesi
Pauli ilkesine göre bir orbitalde en fazla iki elektron bulunabilir. Bu iki elektronun spinleri birbirine zıt olmalıdır.
Kısa kural: Bir orbital en fazla 2 elektron alır.
Hund Kuralı
Hund kuralına göre eş enerjili orbitallere elektronlar önce birer birer yerleşir. Daha sonra orbitallerdeki elektronlar eşleşir.
Örneğin p orbitallerine elektronlar yerleşirken önce px, py ve pz orbitallerine birer elektron yerleşir; sonra eşleşme başlar.
Küresel Simetri Nedir?
Küresel simetri, eş enerjili orbitallerin yarı dolu veya tam dolu olması durumunda ortaya çıkan kararlı elektron dizilimi durumudur.
Bir alt kabuğun yarı dolu veya tam dolu olması atomun kararlılığını artırabilir. Bu durum özellikle elektron dizilimi ve bazı periyodik özelliklerin yorumlanmasında önemlidir.
| Orbital Türü | Yarı Dolu Durum | Tam Dolu Durum |
|---|---|---|
| s | s1 | s2 |
| p | p3 | p6 |
| d | d5 | d10 |
| f | f7 | f14 |
Orbital ve Değerlik Elektron İlişkisi
Değerlik elektronlar, atomun en dış enerji düzeyindeki elektronlardır. Orbital bilgisi, bu elektronların hangi orbitalde bulunduğunu ve kimyasal bağlara nasıl katılabileceğini anlamaya yardım eder.
Örneğin sodyumun elektron dizilimi 1s2 2s2 2p6 3s1 şeklindedir. En dış enerji düzeyindeki 3s1 elektronu, sodyumun değerlik elektronudur.
Değerlik elektron konusunu tekrar etmek için Değerlik Elektron Nedir? yazısını inceleyebilirsin.
Orbital Konusunda Örnekler
| İfade | Doğru mu? | Açıklama |
|---|---|---|
| 1s orbitalinde en fazla 2 elektron bulunabilir. | Doğru | Bir orbital en fazla iki elektron alır. |
| p orbitalleri üç farklı yönde bulunur. | Doğru | px, py ve pz orbitalleri vardır. |
| Elektronlar atomda kesin yörüngelerde döner. | Yanlış | Modern atom teorisine göre elektronların bulunma olasılığı vardır. |
| d alt kabuğu toplamda en fazla 10 elektron alır. | Doğru | d alt kabuğunda 5 orbital bulunur ve her orbital 2 elektron alır. |
Sık Yapılan Hatalar
1. Orbitalleri elektronların kesin yörüngesi sanmak
Orbital elektronun kesin yolu değildir. Elektronun bulunma olasılığının yüksek olduğu bölgedir.
2. p orbitalini tek orbital sanmak
p alt kabuğunda üç orbital vardır: px, py ve pz.
3. Bir orbitalin üç elektron alabileceğini düşünmek
Bir orbital en fazla 2 elektron alabilir. Bu elektronların spinleri zıt olmalıdır.
4. d orbitallerini ikinci enerji düzeyinde aramak
d orbitalleri üçüncü enerji düzeyinden itibaren bulunur.
Orbital Konu Özeti
- Orbital, elektronun bulunma olasılığının yüksek olduğu bölgedir.
- Orbital kesin yörünge anlamına gelmez.
- s, p, d ve f olmak üzere temel orbital türleri vardır.
- s orbitali en fazla 2 elektron alır.
- p alt kabuğu 3 orbitalden oluşur ve toplamda 6 elektron alır.
- d alt kabuğu 5 orbitalden oluşur ve toplamda 10 elektron alır.
- f alt kabuğu 7 orbitalden oluşur ve toplamda 14 elektron alır.
- Elektron diziliminde Aufbau, Pauli ve Hund kuralları kullanılır.
- Küresel simetri yarı dolu veya tam dolu alt kabuklarla ilişkilidir.
Orbital Mini Test
1. Orbital nedir?
- A) Elektronun kesin olarak çizdiği yörünge
- B) Elektronun bulunma olasılığının yüksek olduğu bölge
- C) Atom çekirdeğindeki proton sayısı
- D) Kütle numarası
Doğru cevap: B
Açıklama: Orbital, elektronun atom içinde bulunma olasılığının yüksek olduğu bölgedir.
2. Bir orbital en fazla kaç elektron alabilir?
- A) 1
- B) 2
- C) 6
- D) 10
Doğru cevap: B
Açıklama: Pauli ilkesine göre bir orbital en fazla iki elektron alabilir.
3. p alt kabuğu toplamda en fazla kaç elektron alır?
- A) 2
- B) 6
- C) 10
- D) 14
Doğru cevap: B
Açıklama: p alt kabuğunda 3 orbital bulunur. Her biri 2 elektron alır, toplam kapasite 6’dır.
4. Elektronların önce düşük enerjili orbitallere yerleşmesini açıklayan kural hangisidir?
- A) Aufbau kuralı
- B) Kütle korunumu
- C) Tyndall etkisi
- D) Avogadro yasası
Doğru cevap: A
Açıklama: Aufbau kuralına göre elektronlar önce düşük enerjili orbitallere yerleşir.
5. d alt kabuğu toplamda en fazla kaç elektron alır?
- A) 2
- B) 6
- C) 10
- D) 14
Doğru cevap: C
Açıklama: d alt kabuğunda 5 orbital bulunur. Her orbital 2 elektron alır, toplam kapasite 10’dur.
Sıkça Sorulan Sorular
Orbital nedir?
Orbital, elektronun atom içinde bulunma olasılığının yüksek olduğu üç boyutlu bölgedir.
Orbital ile yörünge aynı şey midir?
Hayır. Yörünge elektronun kesin çizgisel yolu gibi düşünülürken, orbital elektronun bulunma olasılığının yüksek olduğu bölgedir.
Bir orbital kaç elektron alır?
Bir orbital en fazla 2 elektron alabilir.
s, p, d ve f orbitalleri kaç elektron alır?
s alt kabuğu en fazla 2, p alt kabuğu 6, d alt kabuğu 10, f alt kabuğu 14 elektron alır.
Hund kuralı nedir?
Hund kuralına göre eş enerjili orbitallere elektronlar önce birer birer yerleşir, sonra eşleşme başlar.
Küresel simetri nedir?
Eş enerjili orbitallerin yarı dolu veya tam dolu olmasıyla oluşan daha kararlı elektron dizilimi durumudur.
Bu Konudan Sonra Ne Öğrenmeliyim?
Orbital konusunu öğrendikten sonra şu konulara geçebilirsin:
Bu konu şu rehberin parçasıdır:Atom ve Periyodik Sistem
