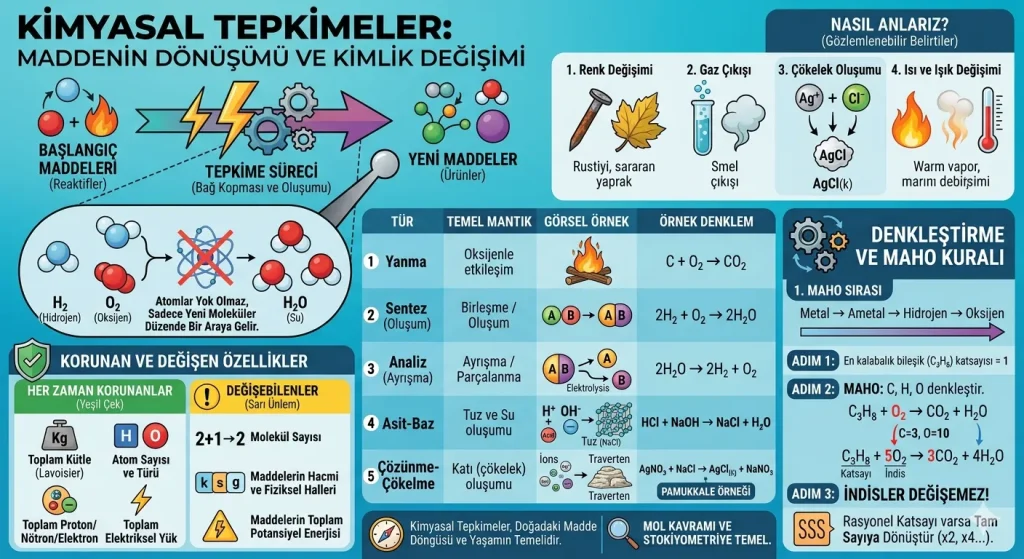
Kimyasal tepkime, bir veya daha fazla maddenin atomları arasındaki bağların kopması ve yeni bağların oluşması sonucunda, başlangıçtaki maddelerden tamamen farklı kimyasal özelliklere sahip yeni maddelerin meydana gelmesi sürecidir. Bu süreçte tepkimeye giren maddelere reaktifler, tepkime sonucunda oluşan yeni maddelere ise ürünler denir. Özetle kimyasal tepkime, maddenin kimlik değiştirerek yeni bir yapıya bürünmesidir.
Önemli Not: Bir kimyasal tepkimede atomların türü ve sayısı asla değişmez; sadece atomların birbirleriyle olan dizilimleri ve bağ yapıları değişir. Örneğin, hidrojen ve oksijen gazları birleşerek suyu oluşturduğunda atomlar yok olmaz, sadece yeni bir moleküler düzende bir araya gelirler.
Kimyasal Tepkimenin Gerçekleştiğini Nasıl Anlarız?
Bir değişimin sadece fiziksel mi kaldığını yoksa kimyasal bir tepkimeye mi dönüştüğünü anlamak için bazı gözlemlenebilir belirtiler vardır. Bir olayda aşağıdaki değişimlerden biri veya birkaçı görülüyorsa kimyasal bir süreçten söz edilebilir:
- Renk Değişimi: Maddenin renginin kalıcı olarak değişmesi (Örn: Demirin paslanması veya sonbaharda yaprakların sararması).
- Gaz Çıkışı: Tepkime sırasında kabarcık oluşumu veya karakteristik bir koku yayılması.
- Çökelek Oluşumu: İki sıvı çözelti karıştırıldığında, suda çözünmeyen katı bir maddenin dibe çökmesi.
- Isı ve Işık Değişimi: Ortamın ısınması (ekzotermik), soğuması (endotermik) veya bir alev/ışık yayılması.
Kimyasal Tepkime Türleri
Kimyada gerçekleşen tepkimeler, maddelerin etkileşim biçimlerine göre beş ana grupta incelenir. Bu türleri bilmek, kimyasal hesaplamalar yaparken denklemi doğru kurmanızı sağlar.
1. Yanma Tepkimeleri
Bir maddenin oksijen (O₂) gazı ile tepkimeye girmesidir. Yanma tepkimeleri genellikle dışarıya ısı verir. Organik bileşikler (karbon ve hidrojen içerenler) yandığında her zaman CO₂ ve H₂O açığa çıkar.
2. Sentez (Oluşum) Tepkimeleri
İki veya daha fazla basit maddenin birleşerek daha karmaşık tek bir madde oluşturmasıdır. Genel formülü A + B → AB şeklindedir.
3. Analiz (Ayrışma) Tepkimeleri
Bir bileşiğin ısı veya elektrik enerjisi (elektroliz) yardımıyla daha basit maddelere ayrışmasıdır. Sentez tepkimesinin tam tersidir. Genel formülü AB → A + B şeklindedir.
4. Asit-Baz Tepkimeleri
Bir asit ile bir bazın etkileşime girerek tuz ve genellikle su oluşturduğu tepkimelerdir. Eğer su oluşuyorsa bu tepkimelere “nötralleşme tepkimesi” de denir. Konu hakkında daha derin bilgi için asitler ve bazlar rehberimizi inceleyebilirsiniz.
5. Çözünme-Çökelme Tepkimeleri
İki sulu çözelti karıştırıldığında, çözeltideki iyonların birleşerek suda çözünmeyen katı bir madde (çökelek) oluşturmasıdır. Pamukkale travertenlerinin oluşumu bu tepkimeye doğal bir örnektir.
| Tepkime Türü | Temel Mantık | Örnek Denklem |
|---|---|---|
| Yanma | Oksijenle etkileşim | C + O₂ → CO₂ |
| Sentez | Birleşme / Oluşum | N₂ + 3H₂ → 2NH₃ |
| Analiz | Ayrışma / Parçalanma | 2H₂O → 2H₂ + O₂ |
| Asit-Baz | Tuz ve Su oluşumu | HCl + NaOH → NaCl + H₂O |
| Çözünme-Çökelme | Katı (çökelek) oluşumu | AgNO₃ + NaCl → AgCl(k) + NaNO₃ |
Kimyasal Tepkimelerde Korunan ve Değişen Özellikler
Tepkimeler sırasında bazı özellikler doğa yasaları gereği asla değişmezken, bazıları maddelerin yeni formuna göre farklılık gösterebilir.
Her Zaman Korunanlar:
- Toplam kütle (Kütlenin Korunumu Kanunu).
- Atom sayısı ve atom türü.
- Toplam proton, nötron ve elektron sayısı.
- Toplam elektriksel yük.
Değişebilenler:
- Molekül sayısı (Katsayılara bağlı olarak artabilir veya azalabilir).
- Maddelerin hacmi ve fiziksel halleri (katı, sıvı, gaz).
- Maddelerin toplam potansiyel enerjisi.
Kimyasal Tepkime Denkleştirme ve MAHO Kuralı
Tepkime denkleştirmenin amacı, girenler ve ürünler tarafındaki atom sayılarını eşitlemektir. Denkleştirme yaparken şu adımları izlemek işinizi kolaylaştıracaktır:
İpucu: MAHO Kuralı
Karmaşık denklemleri çözerken atomları şu sırayla denkleştirin:
Metal → Ametal → Hidrojen → Oksijen.
- En kalabalık atom grubuna sahip bileşiğin katsayısını genellikle 1 kabul edin.
- MAHO sırasını takip ederek atom sayılarını eşitleyin.
- Katsayıları her zaman bileşiğin başına yazın; formülün altındaki sayıları (indisleri) asla değiştirmeyin.
- Eğer rasyonel sayı (1/2 gibi) kullandıysanız, tüm denklemi genişleterek tam sayılara dönüştürün.
Örnek Uygulama: C₃H₈ + O₂ → CO₂ + H₂O tepkimesini denkleştirelim.
- Sol tarafta 3 Karbon (C) var; sağdaki CO₂ başına 3 yazılır.
- Sol tarafta 8 Hidrojen (H) var; sağdaki H₂O başına 4 yazılır.
- Sağda toplam 10 Oksijen oldu (3×2 + 4×1); soldaki O₂ başına 5 yazılır.
- Sonuç: C₃H₈ + 5O₂ → 3CO₂ + 4H₂O
Sıkça Sorulan Sorular (SSS)
Kimyasal tepkimelerde kütle her zaman korunur mu?
Evet, Lavoisier tarafından ortaya konan Kütlenin Korunumu Kanunu’na göre, kapalı bir sistemde girenlerin kütlesi ürünlerin kütlesine her zaman eşittir.
Katalizör nedir ve tepkimeyi nasıl etkiler?
Katalizör, bir kimyasal tepkimeye girerek tepkimeyi hızlandıran ancak tepkime sonunda yapısı değişmeden çıkan maddedir. Tepkime denkleminde okun üzerine yazılır, reaktif veya ürün olarak kabul edilmez.
Fiziksel değişim ile kimyasal tepkime arasındaki temel fark nedir?
Fiziksel değişimde sadece maddenin dış görünüşü ve hali değişir (buzun erimesi gibi). Kimyasal tepkimede ise maddenin atomlar arası bağları kopar ve tamamen yeni bir kimlik kazanır (kağıdın yanması gibi).
Tepkime denkleştirirken neden indisleri değiştiremiyoruz?
Çünkü indisler (H₂O’daki 2 gibi) maddenin kimyasal formülünü belirler. İndisi değiştirmek, maddeyi başka bir şeye dönüştürmek demektir (Örneğin H₂O sudur, H₂O₂ ise hidrojen peroksittir). Biz sadece madde miktarını (katsayıyı) değiştirebiliriz.
Sonuç
Kimyasal tepkimeler, doğadaki madde döngüsünün ve yaşamın temelidir. Soluk alıp vermekten yemeklerin pişmesine, endüstriyel üretimden araçların çalışmasına kadar her yerde bu dönüşümler mevcuttur. Tepkime türlerini ve denkleştirme mantığını kavramak, kimya derslerinde daha karmaşık konular olan mol kavramı ve stokiyometri problemlerini çözmek için en önemli adımdır. Bu temel kuralları öğrenerek kimya dünyasını çok daha rahat anlamlandırabilirsiniz.
