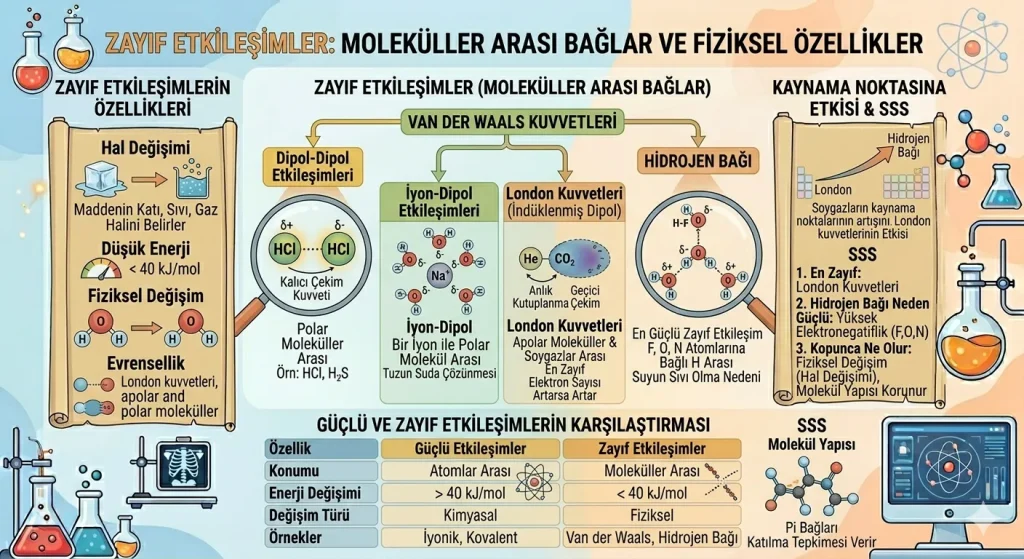
Kimyada maddelerin davranışlarını anlamak için yalnızca atomlar arasındaki güçlü bağları bilmek yeterli değildir. Moleküller arasında gerçekleşen zayıf etkileşimler de maddenin fiziksel özelliklerini belirlemede çok önemlidir.
Bir maddenin oda sıcaklığında katı, sıvı veya gaz olması; kaynama noktasının yüksek ya da düşük olması; bazı maddelerin suda çözünüp bazılarının çözünmemesi zayıf etkileşimlerle yakından ilişkilidir.
Önemli bilgi: Zayıf etkileşimler koptuğunda genellikle yeni madde oluşmaz. Bu nedenle zayıf etkileşimlerin kopması çoğu zaman fiziksel değişimle ilişkilidir.
Zayıf Etkileşim Nedir?
Zayıf etkileşim, genellikle moleküller arasında oluşan ve kimyasal bağlara göre daha düşük enerjili olan çekim kuvvetidir. Bu etkileşimler maddelerin fiziksel özelliklerini etkiler.
Zayıf etkileşimler, atomlar arası güçlü bağlardan farklıdır. Güçlü bağlar atomları veya iyonları bir arada tutarken, zayıf etkileşimler çoğunlukla moleküllerin birbirini çekmesiyle ortaya çıkar.
Güçlü bağları tekrar etmek için Kimyasal Bağ Nedir? yazısını inceleyebilirsin.
Zayıf Etkileşimlerin Genel Özellikleri
- Genellikle moleküller arasında görülür.
- Kimyasal bağlara göre daha düşük enerjilidir.
- Maddenin fiziksel hâlini etkiler.
- Erime ve kaynama noktası üzerinde etkilidir.
- Çözünürlük gibi fiziksel özellikleri etkileyebilir.
- Koptuklarında çoğu zaman maddenin kimyasal kimliği değişmez.
- Soygazlar dahil birçok kimyasal tür arasında London kuvvetleri görülebilir.
Zayıf Etkileşim Türleri Nelerdir?
Zayıf etkileşimler temel olarak iki ana grupta incelenebilir:
- Van der Waals kuvvetleri
- Hidrojen bağı
Van der Waals kuvvetleri kendi içinde dipol-dipol, iyon-dipol ve London kuvvetleri gibi alt türlere ayrılır.
1. Van der Waals Kuvvetleri
Van der Waals kuvvetleri, moleküller veya kimyasal türler arasında oluşan zayıf çekim kuvvetlerinin genel adıdır. Bu kuvvetler molekülün polar veya apolar olmasına göre farklı şekillerde ortaya çıkabilir.
Dipol-Dipol Etkileşimleri
Dipol-dipol etkileşimleri, polar moleküller arasında görülen çekim kuvvetleridir. Polar moleküllerde kısmi pozitif ve kısmi negatif uçlar bulunur.
Bir polar molekülün kısmi pozitif ucu, başka bir polar molekülün kısmi negatif ucunu çeker. Bu çekim dipol-dipol etkileşimi olarak adlandırılır.
- HCl molekülleri arasında
- H2S molekülleri arasında
- SO2 molekülleri arasında
İyon-Dipol Etkileşimleri
İyon-dipol etkileşimi, bir iyon ile polar bir molekül arasında gerçekleşen çekim kuvvetidir. Bu etkileşim özellikle bazı maddelerin suda çözünmesinde önemlidir.
Örneğin sofra tuzu suya atıldığında Na+ ve Cl– iyonları su molekülleri tarafından çevrelenir. Su polar bir molekül olduğu için iyonlarla etkileşime girebilir.
Örnek: NaCl’nin suda çözünmesi sırasında iyon-dipol etkileşimleri önemli rol oynar.
London Kuvvetleri
London kuvvetleri, elektronların anlık hareketleri sonucunda oluşan geçici kutuplaşmalardan kaynaklanan zayıf etkileşimlerdir.
London kuvvetleri tüm moleküllerde ve soygazlarda görülebilir. Ancak apolar moleküllerde baskın etkileşim genellikle London kuvvetleridir.
- Soygaz atomları arasında
- O2 molekülleri arasında
- N2 molekülleri arasında
- CH4 molekülleri arasında
Dikkat: London kuvvetleri tüm moleküllerde bulunur; fakat apolar moleküllerde genellikle etkin olan tek zayıf etkileşim türüdür.
2. Hidrojen Bağı
Hidrojen bağı, hidrojen atomunun flor (F), oksijen (O) veya azot (N) gibi elektronegatifliği yüksek atomlara bağlı olduğu moleküller arasında görülen güçlü bir zayıf etkileşim türüdür.
Hidrojen bağı, zayıf etkileşimler arasında en güçlü olanlardan biridir. Suyun beklenenden yüksek kaynama noktasına sahip olmasının temel nedenlerinden biri su molekülleri arasındaki hidrojen bağlarıdır.
Hidrojen Bağı Hangi Atomlarla Oluşur?
Hidrojen bağı genellikle hidrojenin doğrudan şu atomlara bağlı olduğu moleküllerde görülür:
- Flor (F)
- Oksijen (O)
- Azot (N)
Bu üçlü kolay hatırlanması için genellikle F, O, N şeklinde ifade edilir.
Hidrojen Bağı Örnekleri
- Su molekülleri arasında: H2O
- Amonyak molekülleri arasında: NH3
- Hidrojen florür molekülleri arasında: HF
- DNA’daki bazı baz çiftleri arasında
Zayıf Etkileşimlerin Güç Sıralaması
Zayıf etkileşimlerin gücü molekül yapısına, polariteye, elektron sayısına ve molekül kütlesine bağlı olarak değişebilir. Genel olarak şu sıralama kullanılabilir:
Hidrojen bağı > Dipol-dipol etkileşimi > London kuvvetleri
Ancak bu sıralama her durumda mutlak değildir. Molekül büyüklüğü ve elektron sayısı arttıkça London kuvvetleri de güçlenebilir.
Güçlü ve Zayıf Etkileşimler Arasındaki Farklar
| Özellik | Güçlü Etkileşimler | Zayıf Etkileşimler |
|---|---|---|
| Görüldüğü yer | Atomlar veya iyonlar arasında | Genellikle moleküller arasında |
| Örnekler | İyonik bağ, kovalent bağ, metalik bağ | London kuvvetleri, dipol-dipol, hidrojen bağı |
| Enerji | Genellikle daha yüksektir. | Genellikle daha düşüktür. |
| Kopunca ne olur? | Kimyasal değişim gerçekleşebilir. | Genellikle fiziksel değişim gerçekleşir. |
| Etkilediği özellikler | Maddenin kimyasal yapısını belirler. | Kaynama noktası, erime noktası ve fiziksel hâli etkiler. |
Zayıf Etkileşimlerin Kaynama Noktasına Etkisi
Bir maddenin kaynaması, moleküllerinin birbirinden uzaklaşması anlamına gelir. Bu nedenle kaynama sırasında moleküller arası zayıf etkileşimlerin aşılması gerekir.
Zayıf etkileşimler ne kadar güçlü olursa, bir maddeyi kaynatmak için o kadar fazla enerji gerekir. Bu yüzden daha güçlü zayıf etkileşimlere sahip maddelerin kaynama noktaları genellikle daha yüksektir.
| Madde | Baskın Zayıf Etkileşim | Kaynama Noktasına Etki |
|---|---|---|
| CH4 | London kuvvetleri | Daha düşük kaynama noktası |
| HCl | Dipol-dipol + London | CH4’e göre daha yüksek olabilir |
| H2O | Hidrojen bağı | Beklenenden yüksek kaynama noktası |
London Kuvvetleri ve Molekül Kütlesi İlişkisi
Aynı tür zayıf etkileşime sahip maddelerde molekül kütlesi ve elektron sayısı arttıkça London kuvvetleri genellikle güçlenir.
Bu nedenle soygazlarda aşağı doğru inildikçe atom büyüklüğü ve elektron sayısı artar. Buna bağlı olarak London kuvvetleri güçlenir ve kaynama noktası yükselir.
| Soygaz | Elektron Sayısı | London Kuvveti |
|---|---|---|
| Helyum | 2 | Çok zayıf |
| Neon | 10 | Daha güçlü |
| Argon | 18 | Daha güçlü |
| Kripton | 36 | Argona göre daha güçlü |
Zayıf Etkileşim ve Hal Değişimi İlişkisi
Hal değişimleri sırasında maddenin kimyasal kimliği değişmez. Sadece tanecikler arasındaki uzaklık ve hareketlilik değişir.
Örneğin buz eridiğinde veya su buharlaştığında H2O molekülünün içindeki kovalent bağlar kopmaz. Değişen şey, su molekülleri arasındaki zayıf etkileşimlerdir.
Örnek: Su kaynarken H2O molekülleri parçalanmaz. Sadece su molekülleri arasındaki etkileşimler aşılır ve su buharı oluşur.
Sık Yapılan Hatalar
1. Zayıf etkileşimleri önemsiz sanmak
Zayıf etkileşimler kimyasal bağlara göre daha düşük enerjili olabilir; ancak maddenin erime, kaynama ve çözünürlük gibi özelliklerini belirlemede çok önemlidir.
2. Su kaynarken H2O molekülünün parçalandığını sanmak
Su kaynarken su molekülünün içindeki kovalent bağlar kopmaz. Sadece moleküller arası zayıf etkileşimler aşılır.
3. Hidrojen bulunan her molekülde hidrojen bağı olduğunu düşünmek
Hidrojen bağı için hidrojenin doğrudan F, O veya N atomuna bağlı olması gerekir.
4. London kuvvetlerinin sadece apolar moleküllerde olduğunu sanmak
London kuvvetleri tüm moleküllerde bulunur. Ancak apolar moleküllerde genellikle baskın etkileşim London kuvvetleridir.
Zayıf Etkileşimler Konu Özeti
- Zayıf etkileşimler genellikle moleküller arasında görülür.
- Zayıf etkileşimler kimyasal bağlara göre daha düşük enerjilidir.
- Maddenin erime noktası, kaynama noktası ve fiziksel hâli üzerinde etkilidir.
- Van der Waals kuvvetleri ve hidrojen bağı başlıca zayıf etkileşim türleridir.
- Dipol-dipol etkileşimleri polar moleküller arasında görülür.
- London kuvvetleri tüm moleküllerde bulunabilir.
- Hidrojen bağı genellikle H-F, H-O veya H-N içeren moleküller arasında görülür.
- Zayıf etkileşimlerin kopması çoğu zaman fiziksel değişimle ilişkilidir.
Zayıf Etkileşimler Mini Test
1. Zayıf etkileşimler genellikle nerede görülür?
- A) Atom çekirdeğinde
- B) Moleküller arasında
- C) Sadece protonlar arasında
- D) Sadece metal atomlarının içinde
Doğru cevap: B
Açıklama: Zayıf etkileşimler genellikle moleküller arasında görülür.
2. Aşağıdakilerden hangisi zayıf etkileşim türüdür?
- A) İyonik bağ
- B) Kovalent bağ
- C) London kuvvetleri
- D) Metalik bağ
Doğru cevap: C
Açıklama: London kuvvetleri zayıf etkileşim türlerinden biridir.
3. Hidrojen bağı genellikle hangi atomlara bağlı hidrojen içeren moleküllerde görülür?
- A) F, O, N
- B) Na, K, Li
- C) Fe, Cu, Zn
- D) He, Ne, Ar
Doğru cevap: A
Açıklama: Hidrojen bağı genellikle hidrojenin F, O veya N atomlarına bağlı olduğu moleküllerde görülür.
4. Su kaynarken hangi etkileşimler aşılır?
- A) Su molekülünün içindeki kovalent bağlar
- B) Su molekülleri arasındaki zayıf etkileşimler
- C) Atom çekirdeği bağları
- D) Protonlar arası bağlar
Doğru cevap: B
Açıklama: Su kaynarken H2O molekülü parçalanmaz; moleküller arası zayıf etkileşimler aşılır.
5. London kuvvetleri için aşağıdakilerden hangisi doğrudur?
- A) Sadece iyonik bileşiklerde bulunur.
- B) Sadece metallerde bulunur.
- C) Tüm moleküllerde görülebilir.
- D) Sadece atom çekirdeğinde oluşur.
Doğru cevap: C
Açıklama: London kuvvetleri tüm moleküllerde bulunabilir; apolar moleküllerde genellikle baskındır.
Sıkça Sorulan Sorular
Zayıf etkileşim nedir?
Zayıf etkileşim, genellikle moleküller arasında görülen ve kimyasal bağlara göre daha düşük enerjili olan çekim kuvvetidir.
Zayıf etkileşim türleri nelerdir?
Başlıca zayıf etkileşim türleri London kuvvetleri, dipol-dipol etkileşimleri, iyon-dipol etkileşimleri ve hidrojen bağıdır.
En güçlü zayıf etkileşim hangisidir?
Genellikle hidrojen bağı, zayıf etkileşimler arasında en güçlü olanlardan biridir.
London kuvvetleri hangi maddelerde görülür?
London kuvvetleri tüm moleküllerde ve soygazlarda görülebilir. Apolar moleküllerde genellikle baskın etkileşimdir.
Su kaynarken kimyasal bağlar kopar mı?
Hayır. Su kaynarken H2O molekülünün içindeki kovalent bağlar kopmaz. Moleküller arası zayıf etkileşimler aşılır.
Hidrojen bağı her hidrojen içeren molekülde görülür mü?
Hayır. Hidrojen bağı için hidrojenin doğrudan F, O veya N atomuna bağlı olması gerekir.
Bu Konudan Sonra Ne Öğrenmeliyim?
Zayıf etkileşimler konusunu öğrendikten sonra şu konulara geçebilirsin:
Bu konu şu rehberin parçasıdır: Atom ve Periyodik Sistem – Ogreniyo.com
