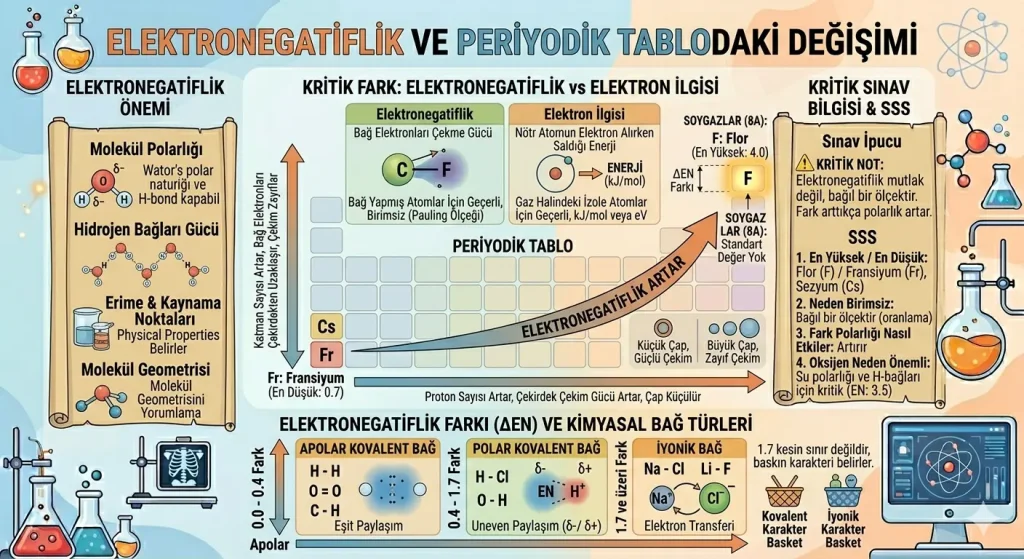
Elektronegatiflik, atomların kimyasal bağ yaparken elektronları ne kadar güçlü çektiğini açıklayan önemli bir kavramdır. Bir atom bağ elektronlarını ne kadar fazla kendine çekiyorsa, elektronegatifliği o kadar yüksektir.
Bu konu özellikle kimyasal bağ türlerini, molekül polarlığını ve maddelerin bazı fiziksel-kimyasal özelliklerini anlamak için önemlidir. Örneğin su molekülünün polar yapıda olması, oksijenin hidrojene göre daha elektronegatif olmasıyla ilgilidir.
Önemli bilgi: Elektronegatiflik, tek başına duran atom için değil; kimyasal bağ yapmış atomların bağ elektronlarını çekme eğilimi için kullanılan bir kavramdır.
Elektronegatiflik Nedir?
Elektronegatiflik, bir atomun başka bir atomla bağ oluştururken ortaklaşa kullanılan elektronları kendine çekme gücüdür. Bu değer, atomların bağ içerisindeki davranışını anlamamızı sağlar.
Elektronegatifliği yüksek olan atom, bağ elektronlarını kendine daha fazla çeker. Elektronegatifliği düşük olan atom ise bağ elektronlarını daha zayıf çeker.
Bu konuyu daha iyi anlamak için önce Atom Nedir?, Periyodik Tablo Nedir? ve Kimyasal Bağ Nedir? konularını bilmek faydalı olur.
Elektronegatiflik Ne İşe Yarar?
- Atomların bağ elektronlarını çekme gücünü gösterir.
- Kimyasal bağın türünü tahmin etmeye yardımcı olur.
- Polar ve apolar bağ ayrımını anlamayı sağlar.
- Molekül polarlığını yorumlamada kullanılır.
- Elementlerin periyodik özelliklerini anlamayı kolaylaştırır.
- Atomların kimyasal davranışlarını karşılaştırmada kullanılır.
Elektronegatiflik Nasıl Değişir?
Elektronegatiflik periyodik tabloda belirli yönlerde düzenli değişim gösterir. Bu değişimin temel nedeni atom yarıçapı, çekirdek yükü ve elektronların çekirdeğe olan uzaklığıdır.
| Yön | Elektronegatiflik Değişimi | Neden? |
|---|---|---|
| Soldan sağa | Genellikle artar. | Proton sayısı artar, atom yarıçapı küçülür. |
| Yukarıdan aşağıya | Genellikle azalır. | Katman sayısı artar, atom yarıçapı büyür. |
Periyodik Tabloda Elektronegatiflik
Periyodik tabloda elektronegatiflik genellikle sağa ve yukarı doğru artar. Bu nedenle elektronegatifliği en yüksek element periyodik tablonun sağ üst tarafında yer alan flor elementidir.
Metaller genellikle düşük elektronegatifliğe sahiptir. Ametaller ise özellikle sağ üst bölgede daha yüksek elektronegatiflik değerleri gösterir.
Kısa kural: Elektronegatiflik genellikle sağa ve yukarı doğru artar.
Aynı Periyotta Soldan Sağa Değişim
Aynı periyotta soldan sağa gidildikçe proton sayısı artar. Katman sayısı çok değişmediği için çekirdek bağ elektronlarını daha güçlü çekebilir.
Bu nedenle aynı periyotta soldan sağa doğru elektronegatiflik genellikle artar.
Aynı Grupta Yukarıdan Aşağıya Değişim
Aynı grupta yukarıdan aşağıya inildikçe katman sayısı artar. Atom yarıçapı büyür ve bağ elektronları çekirdekten uzaklaşır.
Bu nedenle aynı grupta yukarıdan aşağıya doğru elektronegatiflik genellikle azalır.
Elektronegatifliği En Yüksek Element Hangisidir?
Elektronegatifliği en yüksek element flor elementidir. Florun atom yarıçapı küçüktür ve bağ elektronlarını çok güçlü çeker.
Pauling ölçeğine göre florun elektronegatiflik değeri yaklaşık 4,0 kabul edilir. Bu nedenle flor, elektronegatiflik karşılaştırmalarında önemli bir referans noktasıdır.
Elektronegatifliği En Düşük Elementler Hangileridir?
Elektronegatifliği düşük elementler genellikle periyodik tablonun sol alt tarafında yer alır. Sezyum ve fransiyum gibi alkali metaller elektronegatifliği düşük elementler arasında gösterilir.
Bu elementler bağ elektronlarını güçlü çekmek yerine elektron verme eğilimindedir.
Pauling Ölçeği Nedir?
Elektronegatiflik için en yaygın kullanılan ölçeklerden biri Pauling ölçeğidir. Bu ölçekte elementlere bağ elektronlarını çekme güçlerine göre sayısal değerler verilir.
Pauling ölçeği bağıl bir ölçektir. Yani elektronegatiflik doğrudan enerji gibi ölçülen bir büyüklük değil, atomların birbirine göre elektron çekme gücünü ifade eden karşılaştırmalı bir değerdir.
| Element | Yaklaşık Elektronegatiflik | Yorum |
|---|---|---|
| Flor | 4,0 | En yüksek elektronegatifliğe sahiptir. |
| Oksijen | 3,5 | Çok yüksek elektronegatifliğe sahiptir. |
| Azot | 3,0 | Yüksek elektronegatiflik gösterir. |
| Klor | 3,0 civarı | Elektronegatifliği yüksek ametaldir. |
| Sodyum | 0,9 civarı | Elektronegatifliği düşüktür. |
Soygazların Elektronegatifliği Var mı?
Soygazlar genellikle kararlı elektron düzenine sahip oldukları için bağ yapma eğilimleri düşüktür. Bu nedenle birçok temel kaynakta soygazlar için elektronegatiflik değeri verilmez veya sınırlı şekilde ele alınır.
Ancak ksenon ve kripton gibi bazı ağır soygazlar özel koşullarda bileşik oluşturabilir. Bu durumda bu elementler için bazı elektronegatiflik değerleri hesaplanabilir.
Elektronegatiflik ve Elektron İlgisi Arasındaki Fark
Elektronegatiflik ve elektron ilgisi sıkça karıştırılır. İkisi de elektronlarla ilgili olsa da aynı kavram değildir.
| Özellik | Elektronegatiflik | Elektron İlgisi |
|---|---|---|
| Tanım | Bağ elektronlarını çekme gücüdür. | Gaz halindeki nötr atomun elektron almasıyla ilgili enerji değişimidir. |
| Geçerli olduğu durum | Bağ yapmış atomlar için kullanılır. | İzole gaz atomları için kullanılır. |
| Birim | Genellikle birimsizdir. | kJ/mol veya eV gibi enerji birimleriyle ifade edilir. |
| Kullanım amacı | Bağ türünü ve polarlığı yorumlamada kullanılır. | Atomun elektron alma eğilimini anlamada kullanılır. |
Elektronegatiflik ve İyonlaşma Enerjisi Arasındaki Fark
Elektronegatiflik ile iyonlaşma enerjisi de birbiriyle ilişkilidir; fakat aynı değildir.
| Kavram | Ne Anlama Gelir? | Temel Fark |
|---|---|---|
| Elektronegatiflik | Bağ elektronlarını çekme eğilimidir. | Kimyasal bağ içindeki elektronlarla ilgilidir. |
| İyonlaşma enerjisi | Atomdan elektron koparmak için gereken enerjidir. | Elektronu atomdan tamamen uzaklaştırma ile ilgilidir. |
İyonlaşma enerjisini öğrenmek için İyonlaşma Enerjisi Nedir? yazısını inceleyebilirsin.
Elektronegatiflik Farkı Nedir?
İki atom arasında bağ oluştuğunda, bu atomların elektronegatiflik değerleri arasındaki fark bağın karakterini anlamada kullanılır.
Bu fark ne kadar büyükse, bağ elektronları bir atom tarafından o kadar fazla çekilir. Bu durumda bağın polarlığı ve iyonik karakteri artar.
Elektronegatiflik farkı = Büyük elektronegatiflik değeri – Küçük elektronegatiflik değeri
Elektronegatiflik Farkına Göre Bağ Türleri
Elektronegatiflik farkı, bağın apolar kovalent, polar kovalent veya iyonik karakterde olup olmadığını anlamaya yardımcı olur. Ancak bu sınırlar kesin değildir; bağ karakteri keskin çizgilerle ayrılmayabilir.
| Elektronegatiflik Farkı | Bağ Türü | Örnek |
|---|---|---|
| 0 – 0,4 | Apolar kovalent bağ | H-H, O=O, Cl-Cl |
| 0,4 – 1,7 | Polar kovalent bağ | H-Cl, O-H, N-H |
| 1,7 ve üzeri | İyonik karakter artar | NaCl, LiF |
Dikkat: 1,7 sınırı kesin bir duvar gibi düşünülmemelidir. Elektronegatiflik farkı arttıkça bağın iyonik karakteri artar.
Apolar Kovalent Bağ ve Elektronegatiflik
Apolar kovalent bağ, elektronegatiflik farkının çok küçük olduğu bağlarda görülür. Genellikle aynı tür ametal atomları arasında oluşur.
- H2
- O2
- N2
- Cl2
Bu moleküllerde bağ elektronları atomlar arasında yaklaşık eşit paylaşılır.
Polar Kovalent Bağ ve Elektronegatiflik
Polar kovalent bağ, elektronegatiflik farkının belirgin olduğu fakat elektron alışverişinin tam gerçekleşmediği bağlarda görülür.
Elektronegatifliği yüksek olan atom bağ elektronlarını daha fazla çeker ve kısmi negatif yük kazanır. Diğer atom ise kısmi pozitif hale gelir.
- HCl
- H2O
- NH3
- HF
İyonik Bağ ve Elektronegatiflik
Elektronegatiflik farkı çok büyük olduğunda elektronlar bir atom tarafından çok güçlü çekilir. Bu durumda bağ iyonik karakter kazanır.
İyonik bağ genellikle metal ve ametal atomları arasında görülür. Metal atomu elektron verir, ametal atomu elektron alır ve zıt yüklü iyonlar arasında çekim oluşur.
- NaCl
- LiF
- MgO
Elektronegatiflik Molekül Polarlığını Nasıl Etkiler?
Bağların polar olması, molekülün de kesin olarak polar olduğu anlamına gelmez. Molekülün polar olup olmadığını anlamak için hem bağ polarlığına hem de molekül geometrisine bakılır.
Örneğin CO2 molekülünde C-O bağları polardır. Ancak molekül doğrusal ve simetrik olduğu için molekül genel olarak apolar kabul edilir.
H2O molekülünde ise O-H bağları polardır ve molekül açısal yapıya sahiptir. Bu nedenle su molekülü polardır.
| Molekül | Bağ Durumu | Geometri | Molekül Polarlığı |
|---|---|---|---|
| CO2 | Polar bağlar içerir. | Doğrusal ve simetrik | Apolar molekül |
| H2O | Polar bağlar içerir. | Açısal | Polar molekül |
| CH4 | C-H bağları çok az polardır. | Simetrik | Genellikle apolar kabul edilir. |
Sık Yapılan Hatalar
1. Elektronegatifliği elektron alma isteğiyle aynı sanmak
Elektronegatiflik bağ elektronlarını çekme gücüdür. Elektron ilgisi ise izole gaz atomunun elektron almasıyla ilgili enerji değişimidir.
2. Elektronegatifliğin aşağı doğru arttığını düşünmek
Aynı grupta yukarıdan aşağıya inildikçe atom yarıçapı artar ve elektronegatiflik genellikle azalır.
3. Polar bağ içeren her molekülü polar sanmak
Bir molekülün polar olup olmadığını anlamak için bağ polarlığıyla birlikte molekül geometrisine de bakılır.
4. 1,7 sınırını kesin ve değişmez kabul etmek
Elektronegatiflik farkı bağ karakterini anlamaya yardımcı olur; ancak sınırlar kesin değildir.
Elektronegatiflik Konu Özeti
- Elektronegatiflik, atomun bağ elektronlarını çekme gücüdür.
- Elektronegatiflik bağ yapmış atomlar için kullanılan bir kavramdır.
- Periyodik tabloda genellikle soldan sağa artar.
- Aynı grupta yukarıdan aşağıya genellikle azalır.
- Elektronegatifliği en yüksek element flordur.
- Elektronegatiflik farkı bağın polar veya iyonik karakterini anlamaya yardımcı olur.
- Elektronegatiflik elektron ilgisiyle aynı şey değildir.
- Molekül polarlığı için bağ polarlığıyla birlikte molekül geometrisi de dikkate alınır.
Elektronegatiflik Mini Test
1. Elektronegatiflik nedir?
- A) Atomun bağ elektronlarını kendine çekme eğilimi
- B) Atomun nötron sayısı
- C) Atomun kütle numarası
- D) Karışımı ayırma yöntemi
Doğru cevap: A
Açıklama: Elektronegatiflik, bir atomun kimyasal bağ içindeki elektronları çekme eğilimidir.
2. Periyodik tabloda elektronegatiflik genellikle hangi yönde artar?
- A) Sola ve aşağıya
- B) Sağa ve yukarıya
- C) Sadece aşağıya
- D) Sadece sola
Doğru cevap: B
Açıklama: Elektronegatiflik genel olarak periyodik tabloda sağa ve yukarı doğru artar.
3. Elektronegatifliği en yüksek element hangisidir?
- A) Sodyum
- B) Flor
- C) Kalsiyum
- D) Potasyum
Doğru cevap: B
Açıklama: Flor, elektronegatifliği en yüksek elementtir.
4. Elektronegatiflik farkı arttıkça bağın hangi özelliği artar?
- A) İyonik karakteri
- B) Atom numarası
- C) Nötron sayısı
- D) Kütle numarası
Doğru cevap: A
Açıklama: Elektronegatiflik farkı arttıkça bağın polarlığı ve iyonik karakteri artar.
5. Polar bağ içeren her molekül polar mıdır?
- A) Evet, her zaman polardır.
- B) Hayır, molekül geometrisine de bakılır.
- C) Sadece metallerde polardır.
- D) Sadece iyonlarda polardır.
Doğru cevap: B
Açıklama: Molekül polarlığı için bağ polarlığı yanında molekül geometrisi de dikkate alınır.
Sıkça Sorulan Sorular
Elektronegatiflik nedir?
Elektronegatiflik, bir atomun kimyasal bağ yaparken bağ elektronlarını kendine çekme eğilimidir.
Elektronegatiflik periyodik tabloda nasıl değişir?
Elektronegatiflik genellikle soldan sağa artar, yukarıdan aşağıya azalır.
Elektronegatifliği en yüksek element hangisidir?
Elektronegatifliği en yüksek element flordur.
Elektronegatiflik birimli midir?
Elektronegatiflik bağıl bir ölçektir ve genellikle birimsiz olarak kabul edilir.
Elektronegatiflik ile elektron ilgisi aynı şey midir?
Hayır. Elektronegatiflik bağ elektronlarını çekme gücüdür; elektron ilgisi ise izole bir atomun elektron almasıyla ilgili enerji değişimidir.
Elektronegatiflik farkı ne işe yarar?
Elektronegatiflik farkı, kimyasal bağın apolar kovalent, polar kovalent veya iyonik karakterde olup olmadığını yorumlamaya yardımcı olur.
Bu Konudan Sonra Ne Öğrenmeliyim?
Elektronegatiflik konusunu öğrendikten sonra şu konulara geçebilirsin:
- Kimyasal Bağ Nedir?
- İyonlaşma Enerjisi Nedir?
- Periyodik Tablo Nedir?
- Zayıf Etkileşimler ve Fiziksel Bağlar
Bu konu şu rehberin parçasıdır: Atom ve Periyodik Sistem
