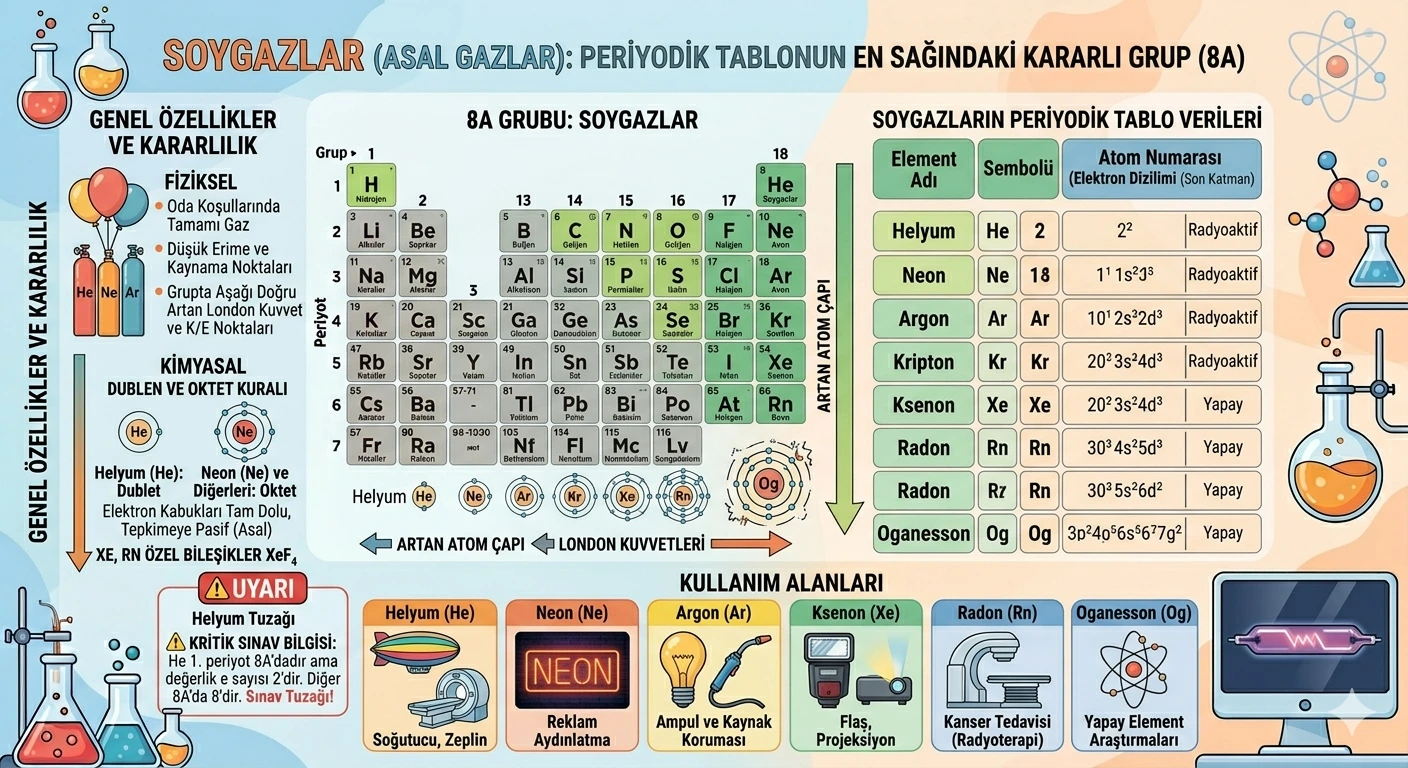
Soygazlar, periyodik tablonun en sağında yer alan ve kimyasal tepkimeye girme eğilimleri düşük olan element grubudur. Bu elementler kararlı elektron düzenlerine sahip oldukları için genellikle elektron alma, verme veya ortaklaşa kullanma ihtiyacı duymazlar.
Helyum, neon ve argon günlük hayatta en bilinen soygazlardır. Helyum balonlarda ve soğutma sistemlerinde, neon ışıklı tabelalarda, argon ise ampuller ve kaynak işlemlerinde kullanılabilir.
Önemli bilgi: Helyumun son katmanında 2 elektron bulunur; buna rağmen 8A grubunda yer alır. Bu yüzden “8A grubundaki tüm elementlerin son katmanında 8 elektron vardır” ifadesi yanlıştır.
Soygaz Nedir?
Soygaz, periyodik tablonun 8A grubunda bulunan ve kimyasal olarak oldukça kararlı olan elementlere verilen addır. Soygazlar, kararlı elektron dizilimleri nedeniyle genellikle başka atomlarla bağ yapmaya isteksizdir.
Soygazlar doğada çoğunlukla tek atomlu gazlar hâlinde bulunur. Yani hidrojen gibi H2 molekülü oluşturmak yerine helyum He, neon Ne ve argon Ar gibi tek atomlu yapıda bulunurlar.
Bu konuyu daha iyi anlamak için önce Periyodik Tablo Nedir?, Atom Nedir? ve Kimyasal Bağ Nedir? yazılarını inceleyebilirsin.
Soygazlar Hangileridir?
| Element | Sembol | Atom Numarası | Öne Çıkan Özellik |
|---|---|---|---|
| Helyum | He | 2 | Son katmanında 2 elektron bulundurur ve dublet düzenindedir. |
| Neon | Ne | 10 | Işıklı tabelalarda kullanımıyla bilinir. |
| Argon | Ar | 18 | Atmosferde en bol bulunan soygazdır. |
| Kripton | Kr | 36 | Aydınlatma ve bazı özel lambalarda kullanılabilir. |
| Ksenon | Xe | 54 | Özel koşullarda bazı bileşikler oluşturabilir. |
| Radon | Rn | 86 | Radyoaktif bir soygazdır. |
| Oganesson | Og | 118 | Yapay ve radyoaktif bir elementtir. |
Soygazların Genel Özellikleri
- Periyodik tablonun 8A grubunda yer alırlar.
- Oda koşullarında gaz hâlindedirler.
- Renksiz, kokusuz ve tatsız gazlardır.
- Doğada genellikle tek atomlu hâlde bulunurlar.
- Kimyasal tepkimeye girme eğilimleri düşüktür.
- Helyum hariç son katmanlarında genellikle 8 elektron bulunur.
- Helyum son katmanında 2 elektron bulundurur ve dublet düzenindedir.
- Erime ve kaynama noktaları genellikle düşüktür.
Soygazlar Neden Kararlıdır?
Soygazların kararlı olmasının temel nedeni, değerlik elektron katmanlarının dolu olmasıdır. Bu durum atomun elektron alma, verme veya ortaklaşa kullanma eğilimini azaltır.
Helyumun son katmanında 2 elektron vardır ve bu onun için kararlı bir düzendir. Neon, argon, kripton, ksenon ve radon gibi soygazlarda ise son katmanda genellikle 8 elektron bulunur.
| Kural | Açıklama | Örnek |
|---|---|---|
| Dublet | Son katmanda 2 elektronla kararlı olma durumudur. | Helyum |
| Oktet | Son katmanda 8 elektronla kararlı olma durumudur. | Neon, argon |
Helyum Neden İstisnadır?
Helyum, 8A grubunda yer almasına rağmen son katmanında 8 elektron değil, 2 elektron bulundurur. Çünkü helyumun sadece bir enerji katmanı vardır ve bu katman en fazla 2 elektron alabilir.
Bu nedenle helyum dublet düzeniyle kararlıdır. Helyumun bu durumu, soygazlar konusunda en sık karıştırılan noktalardan biridir.
Sınav notu: 8A grubundaki helyumun değerlik elektron sayısı 2’dir. Diğer soygazların son katmanında genellikle 8 elektron bulunur.
Soygazlar Doğada Nasıl Bulunur?
Soygazlar kararlı oldukları için doğada genellikle tek atomlu gazlar hâlinde bulunur. Yani kendi atomlarıyla bile kolayca bağ kurmazlar.
Örneğin oksijen doğada O2 molekülü hâlinde bulunabilirken, argon Ar şeklinde tek atomlu gaz olarak bulunur.
| Element | Doğadaki Yaygın Yapı | Açıklama |
|---|---|---|
| Helyum | He | Tek atomlu gazdır. |
| Neon | Ne | Tek atomlu gazdır. |
| Argon | Ar | Tek atomlu gazdır. |
Soygazlar Bileşik Oluşturur mu?
Soygazlar genel olarak bileşik oluşturma eğilimi düşük elementlerdir. Ancak bazı ağır soygazlar özel koşullar altında bileşik oluşturabilir.
Özellikle ksenon gibi büyük atomlu soygazların flor ve oksijen gibi elektronegatifliği yüksek elementlerle bazı bileşikler oluşturabildiği bilinmektedir.
Dikkat: “Soygazlar hiçbir koşulda bileşik oluşturmaz” ifadesi doğru değildir. Daha doğru ifade: “Soygazlar genellikle bileşik oluşturmaya isteksizdir.” şeklindedir.
Soygazların Fiziksel Özellikleri
Soygazların tamamı oda koşullarında gaz hâlindedir. Erime ve kaynama noktaları genellikle düşüktür. Bunun nedeni, atomları arasında yalnızca zayıf London kuvvetlerinin bulunmasıdır.
| Fiziksel Özellik | Açıklama |
|---|---|
| Fiziksel hâl | Oda koşullarında gazdırlar. |
| Renk, koku, tat | Genellikle renksiz, kokusuz ve tatsızdırlar. |
| Erime-kaynama noktası | Genellikle düşüktür. |
| Çözünürlük | Suda çözünürlükleri genellikle düşüktür. |
| Elektrik iletkenliği | Normal koşullarda elektrik akımını iyi iletmezler. |
Soygazlarda Erime ve Kaynama Noktası Nasıl Değişir?
Soygazlarda grupta yukarıdan aşağıya inildikçe atom numarası ve elektron sayısı artar. Bu durum atomlar arasındaki London kuvvetlerinin güçlenmesine neden olur.
London kuvvetleri güçlendikçe atomları birbirinden ayırmak için daha fazla enerji gerekir. Bu nedenle soygazlarda grupta aşağı inildikçe erime ve kaynama noktaları genellikle artar.
| Yön | London Kuvvetleri | Erime / Kaynama Noktası | Neden? |
|---|---|---|---|
| He’den Rn’ye doğru | Artar. | Genellikle artar. | Elektron sayısı ve atom büyüklüğü artar. |
London kuvvetlerini detaylı öğrenmek için Zayıf Etkileşimler ve Fiziksel Bağlar yazısını inceleyebilirsin.
Soygazların Kullanım Alanları
| Soygaz | Kullanım Alanı | Neden Kullanılır? |
|---|---|---|
| Helyum | Balonlar, soğutma sistemleri, MR cihazları | Yanıcı değildir ve çok düşük sıcaklıklarda kullanılabilir. |
| Neon | Işıklı tabelalar | Elektrik etkisiyle parlak renkli ışık yayabilir. |
| Argon | Ampuller, kaynak işlemleri | Tepkimeye girme eğilimi düşük olduğu için koruyucu atmosfer sağlar. |
| Kripton | Özel lambalar, bazı aydınlatma sistemleri | Işık yayma özelliklerinden yararlanılır. |
| Ksenon | Flaş lambaları, projektörler, özel far sistemleri | Yoğun ve parlak ışık oluşturabilir. |
| Radon | Radyoaktif özellikleri nedeniyle sınırlı özel alanlar | Radyoaktif bir gazdır. |
Soygazlar ve Halojenler Arasındaki Fark
| Özellik | Soygazlar | Halojenler |
|---|---|---|
| Grup | 8A grubu | 7A grubu |
| Değerlik elektron sayısı | Helyum hariç genellikle 8 | 7 |
| Kimyasal aktiflik | Genellikle düşüktür. | Yüksektir. |
| Doğadaki yapı | Genellikle tek atomlu gazdır. | Genellikle iki atomlu molekül veya bileşik hâlinde bulunabilir. |
| Örnek | He, Ne, Ar | F, Cl, Br |
Sık Yapılan Hatalar
1. Helyumun değerlik elektron sayısını 8 sanmak
Helyum 8A grubundadır; ancak son katmanında 2 elektron bulunur. Bu nedenle dublet düzenindedir.
2. Soygazların her koşulda bileşik oluşturmadığını sanmak
Soygazlar genel olarak bileşik oluşturmaya isteksizdir; ancak bazı ağır soygazlar özel koşullarda bileşik oluşturabilir.
3. Soygazların iki atomlu molekül hâlinde bulunduğunu düşünmek
Soygazlar genellikle tek atomlu gazlar hâlinde bulunur.
4. Soygazların erime-kaynama noktalarının aşağı doğru azaldığını sanmak
Grupta aşağı inildikçe London kuvvetleri güçlenir ve erime-kaynama noktaları genellikle artar.
Soygazlar Konu Özeti
- Soygazlar periyodik tablonun 8A grubunda yer alır.
- Helyum, neon, argon, kripton, ksenon, radon ve oganesson soygazlardır.
- Oda koşullarında gaz hâlindedirler.
- Doğada genellikle tek atomlu bulunurlar.
- Kimyasal tepkimeye girme eğilimleri düşüktür.
- Helyum dublet, diğer soygazlar genellikle oktet düzenindedir.
- Helyumun son katmanında 2 elektron bulunur.
- Grupta aşağı inildikçe erime ve kaynama noktaları genellikle artar.
Soygazlar Mini Test
1. Soygazlar periyodik tabloda hangi grupta yer alır?
- A) 1A
- B) 2A
- C) 7A
- D) 8A
Doğru cevap: D
Açıklama: Soygazlar periyodik tablonun 8A grubunda yer alır.
2. Helyumun değerlik elektron sayısı kaçtır?
- A) 1
- B) 2
- C) 7
- D) 8
Doğru cevap: B
Açıklama: Helyumun son katmanında 2 elektron bulunur ve dublet düzenindedir.
3. Soygazlar doğada genellikle nasıl bulunur?
- A) Tek atomlu gazlar hâlinde
- B) Daima sıvı hâlde
- C) İyonik kristal hâlinde
- D) Metalik bağ yaparak
Doğru cevap: A
Açıklama: Soygazlar kararlı oldukları için genellikle tek atomlu gazlar hâlinde bulunur.
4. Soygazlarda grupta aşağı inildikçe erime ve kaynama noktası genellikle neden artar?
- A) London kuvvetleri güçlendiği için
- B) Proton sayısı sıfırlandığı için
- C) Atomlar tamamen iyonlaştığı için
- D) Elektron sayısı azaldığı için
Doğru cevap: A
Açıklama: Grupta aşağı inildikçe elektron sayısı ve atom büyüklüğü artar, London kuvvetleri güçlenir.
5. Aşağıdakilerden hangisi soygazdır?
- A) Klor
- B) Sodyum
- C) Neon
- D) Oksijen
Doğru cevap: C
Açıklama: Neon 8A grubunda yer alan bir soygazdır.
Sıkça Sorulan Sorular
Soygaz nedir?
Soygaz, periyodik tablonun 8A grubunda yer alan ve kimyasal tepkimeye girme eğilimi düşük olan kararlı elementtir.
Soygazlar hangileridir?
Helyum, neon, argon, kripton, ksenon, radon ve oganesson soygazlar grubunda yer alır.
Soygazlar neden kararlıdır?
Değerlik elektron katmanları dolu olduğu için elektron alma, verme veya ortaklaşa kullanma eğilimleri düşüktür.
Helyumun değerlik elektron sayısı kaçtır?
Helyumun değerlik elektron sayısı 2’dir. Helyum dublet düzeniyle kararlıdır.
Soygazlar doğada nasıl bulunur?
Soygazlar genellikle tek atomlu gazlar hâlinde bulunur.
Soygazlar bileşik oluşturur mu?
Genellikle bileşik oluşturmaya isteksizdirler. Ancak ksenon gibi bazı ağır soygazlar özel koşullarda bileşik oluşturabilir.
Bu Konudan Sonra Ne Öğrenmeliyim?
Soygazlar konusunu öğrendikten sonra şu konulara geçebilirsin:
Bu konu şu rehberin parçasıdır: Atom ve Periyodik Sistem
