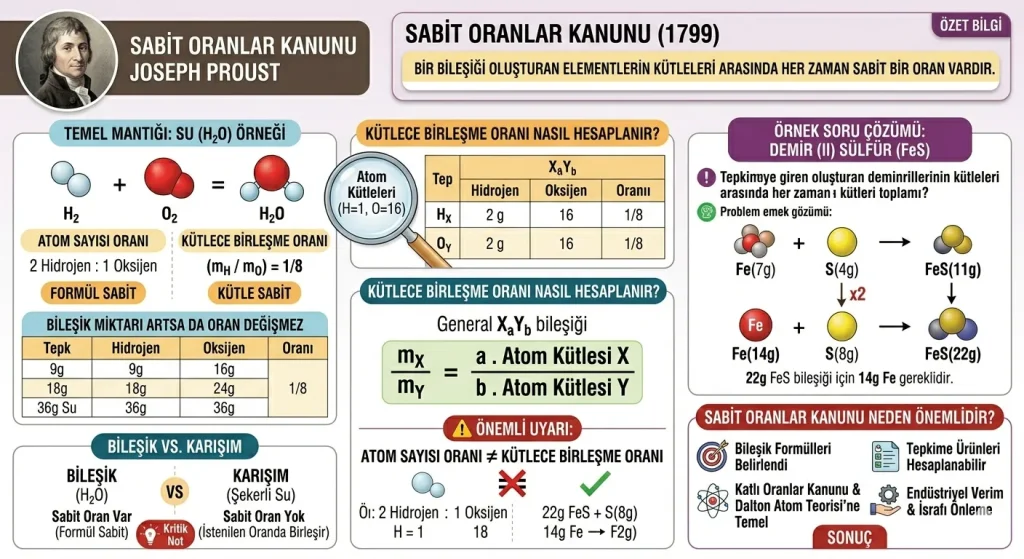
Sabit oranlar kanunu, bir bileşiği oluşturan elementlerin kütleleri arasında her zaman değişmeyen, sabit bir oran olduğunu belirten temel bir kimya yasasıdır. Bu kanuna göre, bir bileşiğin miktarı ne kadar değişirse değişsin, onu meydana getiren elementlerin birbirine oranı asla değişmez. Kimya derslerinde, özellikle 10. sınıf müfredatında karşımıza çıkan bu konu, kimyasal hesaplamaların temel taşlarından biridir.
Özet Bilgi: Sabit oranlar kanunu, bir bileşiğin kütlesi artsa da azalsa da onu oluşturan elementlerin kütlece birleşme oranının her zaman aynı kalacağını ifade eder.
Sabit Oranlar Kanunu Tanımı: Joseph Proust Ne Dedi?
Sabit oranlar kanunu, 1799 yılında Fransız kimyacı Joseph Proust tarafından ortaya atılmıştır. Proust, yaptığı deneyler sonucunda bir bileşiğin hangi yöntemle elde edilirse edilsin veya hangi kaynaktan alınırsa alınsın, bileşenlerinin kütlece her zaman aynı oranda birleştiğini kanıtlamıştır. Bu yasa, Antoine Lavoisier tarafından ortaya atılan Kütlenin Korunumu Kanunu ile birlikte modern kimyanın temelini oluşturur.
Proust’un bu keşfi, maddelerin rastgele değil, belirli bir düzen ve matematiksel denge içinde birleştiğini gösterir. Bu durum, kimyanın bir bilim dalı olarak gelişmesinde ve atom teorilerinin şekillenmesinde büyük rol oynamıştır.
Sabit Oranlar Kanunu’nun Temel Mantığı
Bir bileşiğin formülü sabit olduğu için, o bileşiği oluşturan atomların sayıları ve dolayısıyla kütleleri de sabittir. Örneğin, saf su (H₂O) dünyanın neresinde olursa olsun her zaman 2 hidrojen ve 1 oksijen atomundan oluşur. Bu atomların kütleleri toplandığında, hidrojenin oksijene kütlece oranı her zaman aynı kalır.
Bileşik ve Karışım Arasındaki Fark
Sabit oranlar kanununu anlamak için bileşiklerin genel özellikleri ile karışımlar arasındaki farkı bilmek kritik önem taşır. Karışımlarda (örneğin şekerli su veya tuzlu su) maddeler istenilen her oranda birleştirilebilir. Ancak bileşiklerde durum farklıdır.
Kritik Not: Sabit oranlar kanunu sadece bileşikler için geçerlidir. Karışımlarda sabit bir birleşme oranı aranmaz. Sınavlarda karşınıza çıkan “Aşağıdakilerin hangisinde sabit oran vardır?” sorularında mutlaka bir bileşik aramalısınız.
Kütlece Birleşme Oranı Nasıl Hesaplanır?
Kütlece birleşme oranı, bir bileşikteki elementlerin toplam kütlelerinin birbirine bölünmesiyle bulunur. Bu hesaplama yapılırken elementlerin atom kütleleri (mol kütleleri) ve bileşikteki atom sayıları kullanılır.
Sabit Oranlar Kanunu Formülü
Bir XaYb bileşiği için kütlece birleşme oranı şu formülle hesaplanır:
mX / mY = (a . Atom Kütlesi X) / (b . Atom Kütlesi Y)
⚠️ Önemli Uyarı: Atom sayısı oranı ile kütlece birleşme oranını birbirine karıştırmayın! Örneğin suda atom sayısı oranı 2/1 iken, kütlece birleşme oranı 1/8’dir. Hesaplamalarda her zaman atom kütlelerini (mol kütlesi) kullanmalısınız.
Aşağıdaki tabloda, su (H₂O) bileşiği üzerinden kütlece birleşme oranının nasıl sabit kaldığını görebilirsiniz (H: 1, O: 16):
| Bileşik Miktarı (Su) | Hidrojen Kütlesi (mH) | Oksijen Kütlesi (mO) | Kütlece Oran (mH / mO) |
|---|---|---|---|
| 9 gram | 1 gram | 8 gram | 1/8 |
| 18 gram | 2 gram | 16 gram | 1/8 |
| 36 gram | 4 gram | 32 gram | 1/8 |
Sabit Oranlar Kanunu Örnek Soru Çözümü
Soru: Demir (II) sülfür (FeS) bileşiğinde demir (Fe) elementinin kükürt (S) elementine kütlece birleşme oranı 7/4’tür. Buna göre 22 gram FeS bileşiği elde etmek için kaç gram demir gereklidir?
Çözüm:
- Öncelikle orandan yola çıkarak toplam bileşik kütlesini bulalım: 7 gram Fe + 4 gram S = 11 gram FeS oluşur.
- Soruda bizden 22 gram FeS isteniyor. Bu, 11 gramın 2 katıdır (22 / 11 = 2).
- Sabit oran bozulmayacağı için her iki elementin miktarını da 2 ile çarpmalıyız.
- Demir miktarı: 7 x 2 = 14 gram Fe gereklidir.
Sabit Oranlar Kanunu Neden Önemlidir?
Bu kanun, modern kimyanın doğuşuna zemin hazırlamıştır. Sabit oranlar kanunu sayesinde:
- Bileşiklerin formülleri bilimsel yöntemlerle belirlenebilmiştir.
- Kimyasal tepkimelerde ne kadar ürün oluşacağı önceden hesaplanabilir hale gelmiştir.
- John Dalton’un geliştirdiği Katlı Oranlar Kanunu ve Dalton Atom Teorisi’ne temel oluşturmuştur.
- Endüstriyel üretimde hammadde israfı önlenerek verimli üretim yapılması sağlanmıştır.
Sıkça Sorulan Sorular (SSS)
Sabit oranlar kanununu kim bulmuştur?
Bu kanun, 1799 yılında Fransız kimyacı Joseph Proust tarafından deneysel çalışmalar sonucunda bulunmuştur.
Sabit oranlar kanunu karışımlar için geçerli midir?
Hayır, karışımların (hava, deniz suyu, çelik vb.) belirli bir birleşme oranı yoktur. Bu kanun sadece saf bileşikler için geçerlidir.
Sabit oranlar kanunu ve katlı oranlar kanunu arasındaki fark nedir?
Sabit oranlar kanunu tek bir bileşiğin içindeki elementlerin oranını inceler. Katlı oranlar kanunu ise aynı iki elementten oluşan iki farklı bileşik arasındaki (örneğin CO ve CO₂) oranları inceler.
Su (H₂O) örneğinde sabit oran kaçtır?
Suyun kütlece birleşme oranı (mH / mO) her zaman 1/8’dir. Yani her 1 gram hidrojene karşılık 8 gram oksijen tepkimeye girer.
Sonuç
Sabit oranlar kanunu, doğadaki düzenin kimyasal bir yansımasıdır. Joseph Proust’un ortaya koyduğu bu ilke, bileşiklerin her zaman belirli kütle oranlarında birleştiğini kanıtlayarak kimyasal hesaplamaların (stokiyometri) önünü açmıştır. Bu konuyu iyi kavramak, kimyanın temel kanunları başlığı altındaki diğer yasaları anlamanızı da kolaylaştıracaktır.
Kimya derslerinizde başarılar dileriz! Konuyla ilgili eksiklerinizi tamamlamak için sitemizdeki diğer özet notlara göz atmayı unutmayın.