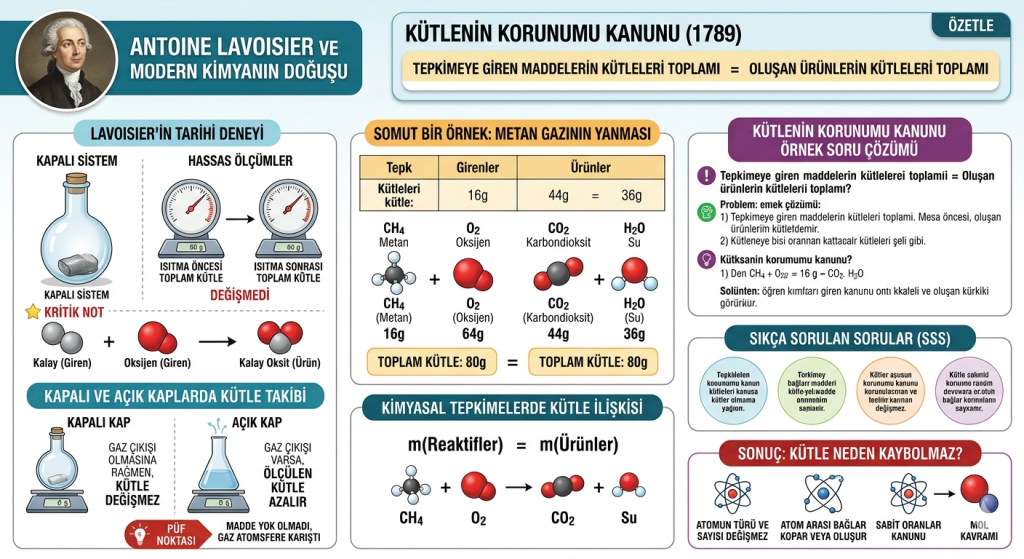
Kimyasal bir tepkimede hiçbir madde yoktan var olmaz, var olan madde de yok edilemez. 18. yüzyılda Antoine Lavoisier tarafından sistemleştirilen kütlenin korunumu kanunu, modern kimyanın en temel yasasıdır. Bu kurala göre, bir tepkimeye giren maddelerin kütleleri toplamı, tepkime sonucunda oluşan ürünlerin kütleleri toplamına her zaman eşittir.
Özetle: Kapalı bir sistemde gerçekleştirilen fiziksel veya kimyasal değişimlerde, başlangıçtaki toplam kütle ile sonuçtaki toplam kütle birbirine eşittir.
Antoine Lavoisier ve Modern Kimyanın Doğuşu
Kütlenin korunumu yasası denildiğinde akla gelen ilk isim Fransız bilim insanı Antoine Lavoisier‘dir. Lavoisier, yaptığı hassas ölçümlerle kimya bilimi tarihinde simyadan bilimsel kimyaya geçişin kapılarını aralamıştır. O döneme kadar yanma olayının “filojiston” adı verilen gizemli bir maddenin çıkışıyla gerçekleştiği düşünülüyordu; ancak Lavoisier yaptığı deneylerle bu teoriyi çürütmüştür.
Lavoisier’in Tarihi Deneyi
Lavoisier, bir miktar kalay metalini içi hava dolu cam bir balona koymuş ve ağzını kapatarak tartmıştır. Ardından balonu ısıtmış, kalayın beyaz bir toza (kalay oksit) dönüştüğünü gözlemlemiştir. Isıtma işleminden sonra cam balonu tekrar tarttığında, toplam kütlenin hiç değişmediğini kanıtlamıştır. Bu deney, kimyasal tepkimelerde kütlenin korunduğunu bilimsel olarak ispatlayan en önemli çalışmadır.
Kimyasal Tepkimelerde Kütle İlişkisi
Bir kimyasal tepkimeyi matematiksel bir denklem gibi düşünebilirsiniz. Tepkimeye giren maddeler (reaktifler) sol tarafta, oluşan maddeler (ürünler) ise sağ tarafta yer alır. Atomların türü ve sayısı değişmediği için toplam kütle korunur.
Somut Bir Örnek: Metan Gazının Yanması
Aşağıdaki tablo, metan gazının oksijenle yanması sonucu oluşan kütle dengesini göstermektedir:
| Bileşenler | Metan (Giren) | Oksijen (Giren) | Karbondioksit (Ürün) | Su (Ürün) |
|---|---|---|---|---|
| Kütle (Gram) | 16 g | 64 g | 44 g | 36 g |
| Toplam Kütle | 80 gram | 80 gram | ||
Görüldüğü üzere, girenlerin toplamı (16+64=80) ile ürünlerin toplamı (44+36=80) birbirine tam olarak eşittir.
Kapalı ve Açık Kaplarda Kütle Takibi
Öğrencilerin en çok yanıldığı nokta açık kaplarda gerçekleşen tepkimelerdir. Eğer bir tepkime sonucunda gaz açığa çıkıyorsa ve kap açıksa, gaz sistemden uzaklaşacağı için terazi daha düşük bir değer gösterir.
- Kapalı Kap: Gaz çıkışı olsa bile madde sistemden ayrılamaz, kütle değişimi gözlenmez.
- Açık Kap: Gaz çıkışı varsa ölçülen kütle azalır; gaz girişi varsa (örneğin demirin paslanırken havadan oksijen alması) ölçülen kütle artabilir.
Püf Noktası: Sınav sorularında “açık kapta kütle azaldı” ifadesini görürseniz, bu kütlenin yok olduğu anlamına gelmez. Sadece oluşan gazın uçup gittiğini ve kütlenin korunumu kanununun aslında hala geçerli olduğunu unutmamalısınız.
Kütlenin Korunumu Kanunu Örnek Soru Çözümü
Soru: 20 gram X maddesi ile bir miktar Y maddesi artansız tepkimeye girerek 35 gram Z maddesini oluşturuyor. Buna göre tepkimede kullanılan Y maddesi kaç gramdır?
Çözüm:
Kütlenin korunumu kanununa göre: m(X) + m(Y) = m(Z)
20 + m(Y) = 35
m(Y) = 35 – 20
m(Y) = 15 gram olarak bulunur.
Bu temel mantık, kimyasal tepkime türleri ne olursa olsun her zaman geçerlidir.
Sıkça Sorulan Sorular (SSS)
Kütlenin korunumu kanununu kim bulmuştur?
Bu kanun, 1789 yılında Antoine Lavoisier tarafından sistemli bir şekilde ortaya konulmuştur.
Fiziksel değişimlerde de kütle korunur mu?
Evet, kütlenin korunumu sadece kimyasal tepkimelerde değil, erime veya donma gibi fiziksel değişimlerde de geçerlidir. Örneğin 100 gram buz eridiğinde yine 100 gram su oluşur.
Açık bir kapta kağıt yandığında kütle neden azalır?
Kağıt yandığında karbondioksit gazı ve su buharı açığa çıkar. Kap açık olduğu için bu gazlar atmosfere karışır. Terazi üzerinde sadece kül kaldığı için kütle azalmış gibi görünür; ancak çıkan gazlar tartılabilseydi toplam kütlenin değişmediği ispatlanırdı.
Nükleer tepkimelerde kütle korunur mu?
Klasik kimya sınırları içerisinde kütle korunur. Ancak nükleer (çekirdek) tepkimelerde çok küçük bir miktar kütle enerjiye (E=mc²) dönüşebilir. Bu durum lise kimya müfredatındaki genel kimya yasalarının dışındaki özel bir durumdur.
Sonuç: Kütle Neden Kaybolmaz?
Kütlenin korunumu kanunu, evrendeki madde dengesinin temelidir. Kimyasal tepkimeler sırasında atomlar arası bağlar kopar veya yeni bağlar oluşur; ancak atomların kendileri yok olmaz veya başka bir atoma dönüşmez. Bu nedenle tepkime öncesindeki atom sayısı ve türü, tepkime sonrasıyla aynı kalır, bu da kütleyi sabit tutar.
Kimyanın diğer temel yasalarını öğrenmek için sabit oranlar kanunu nedir içeriğimize göz atabilir veya hesaplamalarınızı geliştirmek için mol kavramı konu anlatımı sayfamızı ziyaret edebilirsiniz.
