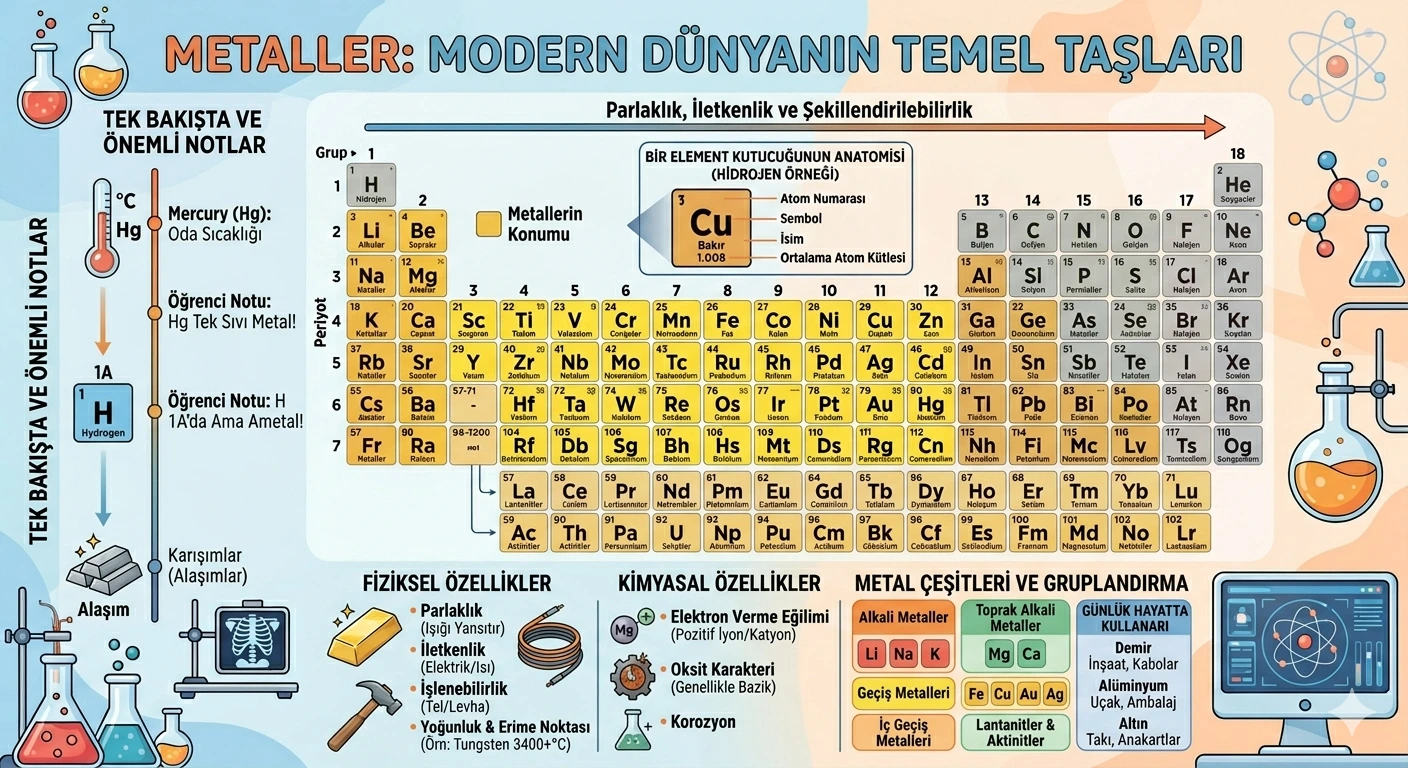
Metaller, günlük yaşamda ve sanayide en çok karşılaştığımız element gruplarından biridir. Demir, bakır, alüminyum, altın, gümüş, sodyum ve kalsiyum metallere örnek verilebilir.
Metallerin önemli özellikleri; elektrik ve ısıyı iyi iletmeleri, parlak olmaları, şekillendirilebilmeleri ve elektron verme eğiliminde olmalarıdır. Bu özellikler, metallerin inşaat, elektrik, ulaşım, teknoloji ve tıp gibi alanlarda yaygın kullanılmasını sağlar.
Önemli bilgi: Cıva hariç metallerin çoğu oda sıcaklığında katıdır. Hidrojen ise 1A grubunda yer almasına rağmen metal değil, ametaldir.
Metal Nedir?
Metal, genellikle parlak görünümlü, ısı ve elektriği iyi ileten, şekillendirilebilen ve elektron verme eğiliminde olan elementlere verilen addır.
Kimyasal açıdan metaller, değerlik elektronlarını vererek pozitif yüklü iyonlar yani katyonlar oluşturma eğilimindedir. Bu nedenle metaller ametallerle tepkimeye girerek genellikle iyonik bağlı bileşikler oluşturabilir.
Metallerin periyodik tablodaki yerini daha iyi anlamak için Periyodik Tablo Nedir? yazısını inceleyebilirsin.
Metallerin Genel Özellikleri
- Genellikle parlak yüzeye sahiptirler.
- Isı ve elektriği iyi iletirler.
- Tel ve levha haline getirilebilirler.
- Oda sıcaklığında cıva hariç çoğu katıdır.
- Elektron verme eğilimindedirler.
- Genellikle pozitif yüklü iyon oluştururlar.
- Ametallerle iyonik bağlı bileşikler oluşturabilirler.
- Kendi aralarında alaşımları oluşturabilirler.
Metallerin Fiziksel Özellikleri
Metallerin fiziksel özellikleri, onların günlük hayatta ve sanayide yaygın kullanılmasının temel nedenidir.
| Fiziksel Özellik | Açıklama | Örnek |
|---|---|---|
| Parlaklık | Metaller ışığı yansıtır ve metalik parlaklık gösterir. | Altın, gümüş, bakır |
| Elektrik iletkenliği | Serbest elektronlar sayesinde elektriği iyi iletirler. | Bakır kablo |
| Isı iletkenliği | Isıyı hızlı iletebilirler. | Tencere, tava |
| İşlenebilirlik | Tel ve levha haline getirilebilirler. | Alüminyum folyo, bakır tel |
| Fiziksel hâl | Cıva hariç çoğu oda sıcaklığında katıdır. | Demir, alüminyum, altın |
Metallerin Kimyasal Özellikleri
Metallerin kimyasal özellikleri, elektron verme eğilimleriyle yakından ilişkilidir. Bir metal atomu elektron verdiğinde pozitif yüklü iyon haline gelir.
| Kimyasal Özellik | Açıklama | Örnek |
|---|---|---|
| Elektron verme | Metaller elektron vererek katyon oluşturabilir. | Na → Na+ + e– |
| Ametallerle bağ yapma | Ametallerle iyonik bağlı bileşikler oluşturabilirler. | NaCl |
| Oksit oluşturma | Oksijenle tepkimeye girerek metal oksitleri oluşturabilirler. | MgO, CaO |
| Korozyon | Bazı metaller hava ve suyla tepkimeye girerek aşınabilir. | Demirin paslanması |
Metaller Periyodik Tabloda Nerede Bulunur?
Metaller periyodik tablonun genellikle sol ve orta kısmında yer alır. 1A grubu, 2A grubu, geçiş metalleri, lantanitler ve aktinitler büyük ölçüde metal özellik gösterir.
Periyodik tablonun sağ tarafında ise ametaller daha yoğun bulunur. Metaller ile ametaller arasında bazı yarı metaller yer alır.
Dikkat: Hidrojen 1A grubunda yer alır; ancak metal değil, ametaldir.
Metal Çeşitleri Nelerdir?
Metaller, periyodik tablodaki konumlarına ve kimyasal özelliklerine göre farklı gruplara ayrılır.
1. Alkali Metaller
Alkali metaller, periyodik tablonun 1A grubunda yer alan metallerdir. Hidrojen bu grupta yer alsa da alkali metal değildir.
- Lityum
- Sodyum
- Potasyum
- Rubidyum
- Sezyum
- Fransiyum
Alkali metaller çok aktif oldukları için doğada genellikle serbest halde bulunmazlar.
2. Toprak Alkali Metaller
Toprak alkali metaller, periyodik tablonun 2A grubunda yer alır. Alkali metallere göre daha az aktif olsalar da yine de tepkimeye girmeye yatkındırlar.
- Berilyum
- Magnezyum
- Kalsiyum
- Stronsiyum
- Baryum
- Radyum
3. Geçiş Metalleri
Geçiş metalleri, periyodik tablonun orta kısmında yer alan metallerdir. Demir, bakır, çinko, gümüş ve altın bu gruba örnektir.
Geçiş metalleri genellikle sert, dayanıklı, parlak ve iyi iletken elementlerdir.
4. İç Geçiş Metalleri
Periyodik tablonun alt kısmında ayrı gösterilen lantanitler ve aktinitler iç geçiş metalleri olarak değerlendirilir.
Bu elementlerin bazıları ileri teknoloji, mıknatıslar, nükleer enerji ve özel alaşımlarda kullanılabilir.
Metaller ve Metalik Bağ
Metallerin elektrik ve ısıyı iyi iletmesi, işlenebilir olması ve parlak görünmesi metalik bağ ile ilişkilidir. Metalik bağ, metal atomlarını bir arada tutan güçlü etkileşimdir.
Metallerde değerlik elektronları atomlar arasında serbestçe hareket edebilir. Bu durum genellikle elektron denizi modeli ile açıklanır.
Bu konuyu detaylı öğrenmek için Metalik Bağ Nedir? yazısına geçebilirsin.
Metaller Alaşım Oluşturur mu?
Evet. Metaller kendi aralarında homojen karışımlar oluşturabilir. Bu metal karışımlarına alaşım denir.
Alaşımlar, saf metallerden daha dayanıklı veya daha kullanışlı özelliklere sahip olabilir.
| Alaşım | İçeriği | Kullanım Alanı |
|---|---|---|
| Çelik | Demir + karbon | İnşaat, otomotiv, makine |
| Pirinç | Bakır + çinko | Musluk, süs eşyası, müzik aleti |
| Tunç | Bakır + kalay | Heykel, madalya, tarihi araçlar |
Metallerin Kullanım Alanları
Metaller sahip oldukları özellikler nedeniyle çok geniş kullanım alanlarına sahiptir.
| Metal | Öne Çıkan Özellik | Kullanım Alanı |
|---|---|---|
| Demir | Dayanıklı ve yaygın | İnşaat, çelik üretimi |
| Bakır | Elektriği iyi iletir | Elektrik kabloları |
| Alüminyum | Hafif ve dayanıklı | Uçak, ambalaj, pencere profili |
| Altın | Parlak, değerli, iletken | Takı, elektronik |
| Gümüş | Yüksek iletkenlik | Elektronik, takı, kaplama |
Metal, Ametal ve Yarı Metal Farkı
| Özellik | Metal | Ametal | Yarı Metal |
|---|---|---|---|
| İletkenlik | Genellikle iyi iletir. | Genellikle iyi iletmez. | Yarı iletken özellik gösterebilir. |
| Görünüm | Genellikle parlaktır. | Genellikle mattır. | Metal veya ametal gibi görünebilir. |
| Elektron eğilimi | Elektron verme eğilimindedir. | Elektron alma veya ortaklaşa kullanma eğilimindedir. | Koşula göre farklı davranabilir. |
| Örnek | Demir, bakır, sodyum | Oksijen, azot, kükürt | Bor, silisyum, germanyum |
Sık Yapılan Hatalar
1. Hidrojeni metal sanmak
Hidrojen 1A grubunda yer alır; ancak metal değil, ametaldir.
2. Tüm metallerin katı olduğunu düşünmek
Cıva oda sıcaklığında sıvı halde bulunan bir metaldir.
3. Metallerin kendi aralarında bileşik oluşturduğunu sanmak
Metaller kendi aralarında genellikle bileşik değil, alaşım adı verilen homojen karışımlar oluşturur.
4. Metallerin elektriği neden ilettiğini ezberlemek
Metallerin elektriği iletmesi, serbest hareket edebilen elektronlarla yani metalik bağ yapısıyla ilgilidir.
Metaller Konu Özeti
- Metaller periyodik tablonun genellikle sol ve orta kısmında yer alır.
- Metaller genellikle parlak görünümlüdür.
- Isı ve elektriği iyi iletirler.
- Tel ve levha haline getirilebilirler.
- Elektron vererek pozitif iyon oluşturma eğilimindedirler.
- Cıva oda sıcaklığında sıvı olan metaldir.
- Hidrojen 1A grubunda olsa da metal değildir.
- Metaller kendi aralarında alaşım oluşturabilir.
Metaller Mini Test
1. Metaller için aşağıdakilerden hangisi genellikle doğrudur?
- A) Isı ve elektriği iyi iletirler.
- B) Her zaman gaz halindedirler.
- C) Elektron alma eğilimindedirler.
- D) Daima mat görünürler.
Doğru cevap: A
Açıklama: Metaller serbest elektronları sayesinde ısı ve elektriği iyi iletir.
2. Oda sıcaklığında sıvı olan metal hangisidir?
- A) Demir
- B) Cıva
- C) Bakır
- D) Sodyum
Doğru cevap: B
Açıklama: Cıva oda sıcaklığında sıvı halde bulunan metaldir.
3. Hidrojen için aşağıdakilerden hangisi doğrudur?
- A) 1A grubunda yer alır ama metal değildir.
- B) Geçiş metalidir.
- C) Oda sıcaklığında sıvı metaldir.
- D) Lantanit grubundadır.
Doğru cevap: A
Açıklama: Hidrojen 1A grubunda bulunmasına rağmen ametaldir.
4. Metaller kendi aralarında genellikle ne oluşturur?
- A) Alaşım
- B) Asit
- C) Tuz
- D) Gaz karışımı
Doğru cevap: A
Açıklama: Metaller kendi aralarında alaşım adı verilen homojen karışımlar oluşturabilir.
5. Metallerin elektrik iletmesi hangi yapı ile açıklanır?
- A) Elektron denizi modeli
- B) Süspansiyon
- C) İzoelektronik yapı
- D) Tyndall etkisi
Doğru cevap: A
Açıklama: Metallerde serbest hareket eden elektronlar elektrik iletkenliğini sağlar.
Sıkça Sorulan Sorular
Metal nedir?
Metal, genellikle parlak, ısı ve elektriği iyi ileten, şekillendirilebilen ve elektron verme eğiliminde olan elementtir.
Metallerin özellikleri nelerdir?
Metaller genellikle parlak, iletken, işlenebilir ve elektron verme eğiliminde olan elementlerdir.
Oda sıcaklığında sıvı olan metal hangisidir?
Oda sıcaklığında sıvı halde bulunan metal cıvadır.
Hidrojen metal midir?
Hayır. Hidrojen 1A grubunda yer alsa da metal değil, ametaldir.
Metaller neden elektriği iyi iletir?
Metallerde serbest hareket edebilen elektronlar bulunur. Bu elektronlar elektrik akımını iletir.
Metaller kendi aralarında ne oluşturur?
Metaller kendi aralarında genellikle alaşım adı verilen homojen karışımlar oluşturur.
Bu Konudan Sonra Ne Öğrenmeliyim?
Metaller konusunu öğrendikten sonra şu konulara geçebilirsin:
Bu konu şu rehberin parçasıdır: Atom ve Periyodik Sistem
