Hızlı Bakış: Kritik Notlar
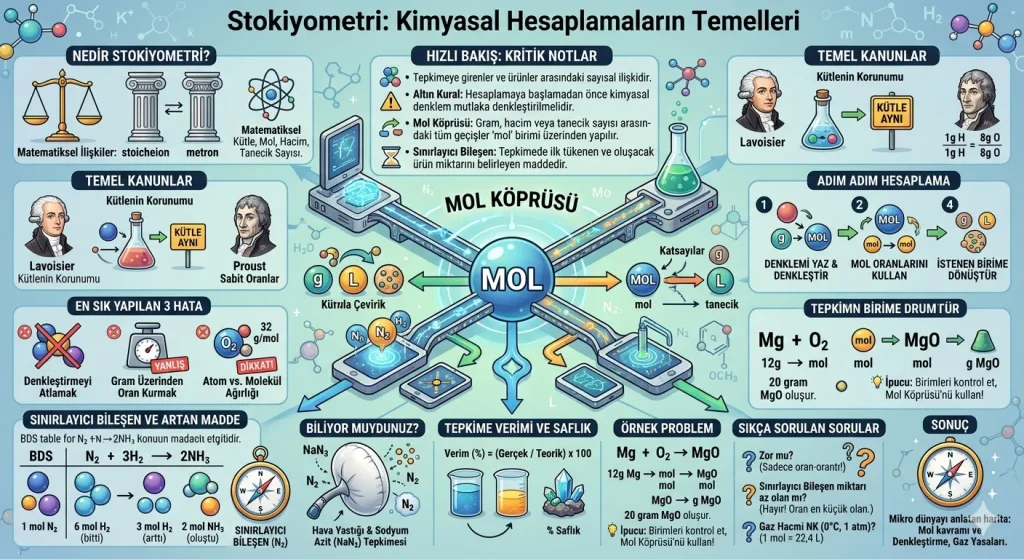
- Stokiyometri: Tepkimeye girenler ve ürünler arasındaki sayısal ilişkidir.
- Altın Kural: Hesaplamaya başlamadan önce kimyasal denklem mutlaka denkleştirilmelidir.
- Mol Köprüsü: Gram, hacim veya tanecik sayısı arasındaki tüm geçişler “mol” birimi üzerinden yapılır.
- Sınırlayıcı Bileşen: Tepkimede ilk tükenen ve oluşacak ürün miktarını belirleyen maddedir.
Kimyasal bir tepkime gerçekleştirmek, bir yemek tarifini kusursuz uygulamaya benzer. Elinizdeki malzemelerin miktarına göre ne kadar ürün elde edeceğinizi bilmeniz gerekir. Stokiyometri, kimyasal denklemleri kullanarak bu miktarları kesin bir şekilde hesaplamamıza olanak tanır. İster laboratuvarda hassas bir deney yapın, ister endüstriyel ölçekte üretim gerçekleştirin; doğru sonuçlar için stokiyometrik hesaplamalar kimyanın temel dilidir.
Stokiyometri Nedir?
Stokiyometri, Yunanca “stoicheion” (element) ve “metron” (ölçmek) kelimelerinden türetilmiştir. En basit tanımıyla; kimyasal tepkimelerdeki kütle, mol, hacim ve tanecik sayısı gibi niceliklerin birbirleriyle olan matematiksel ilişkisidir. Bu hesaplamaların temelinde, evrendeki atomların yok olmadığı, sadece yeni bağlar kurarak yeniden düzenlendiği gerçeği yatar.
Stokiyometrinin Dayandığı Temel Kanunlar
Kimyasal hesaplamalar rastgele yapılmaz; iki evrensel kanun üzerine inşa edilir:
1. Kütlenin Korunumu Kanunu
Antoine Lavoisier tarafından ortaya konan bu kanuna göre, kapalı bir sistemde gerçekleşen kimyasal tepkimede giren maddelerin toplam kütlesi, oluşan ürünlerin toplam kütlesine her zaman eşittir. Hiçbir atom yoktan var olmaz ve yok edilemez.
2. Sabit Oranlar Kanunu
Joseph Proust’un tanımladığı bu kanun, bir bileşiği oluşturan elementlerin kütleleri arasında her zaman sabit bir oran olduğunu belirtir. Örneğin, su (H₂O) oluşurken hidrojen ve oksijen her zaman belirli bir kütle oranında birleşir; bu oran değişirse madde artık su olmaz.
Adım Adım Stokiyometrik Hesaplama Nasıl Yapılır?
Bir stokiyometri problemini hatasız çözmek için şu işlem sırasını takip etmelisiniz:
- Denklemi Yazın ve Denkleştirin: En kritik adımdır. Denklem denkleşmemişse katsayılar yanlış olacak, bu da tüm sonucu etkileyecektir. Kimyasal Tepkime Türleri ve Denkleştirme rehberimizden yardım alabilirsiniz.
- Verilen Miktarı Mole Çevirin: Soruda verilen değer gram, litre (NK) veya tanecik sayısı olabilir. Bunları mutlaka mol birimine dönüştürün. Mol Kavramı ve Hesaplamaları bu noktada temel aracınızdır.
- Mol Oranlarını (Katsayıları) Kullanın: Denkleştirilmiş denklemdeki katsayıları kullanarak, miktarı bilinen maddeden istenen maddeye geçiş yapın.
- İstenen Birime Dönüştürün: Bulduğunuz mol sayısını soruda istenen gram, hacim veya tanecik sayısı birimine geri çevirerek işlemi tamamlayın.
Stokiyometride En Sık Yapılan 3 Hata
- Denkleştirmeyi Atlamak: Tepkimeyi denkleştirmeden katsayıları kullanmak, yanlış oran kurmanıza neden olur.
- Gram Üzerinden Oran Kurmak: En yaygın hatadır. Maddeler birbirleriyle kütlece değil, molce (tanecik sayısıca) belirli oranlarda tepkimeye girer.
- Atom vs. Molekül Ağırlığı: O₂ gibi diatomik moleküllerin mol kütlesini alırken sadece O atomunun ağırlığını (16) kullanmak yerine molekül ağırlığını (32) kullanmaya dikkat edin.
Sınırlayıcı Bileşen ve Artan Madde Kavramı
Gerçek hayatta maddeler her zaman tam gereken oranlarda karıştırılmaz. Tepkimede tamamen tükenen ve oluşacak ürün miktarını belirleyen maddeye sınırlayıcı bileşen denir. Diğer madde ise “artan madde”dir.
Sınırlayıcı bileşeni bulmak için Başlangıç-Değişim-Sonuç (BDS) tablosu kullanmak en güvenli yöntemdir. Örneğin; N₂ + 3H₂ → 2NH₃ tepkimesinde elimizde 1 mol N₂ ve 6 mol H₂ olduğunu varsayalım:
| Aşama | N₂ (Azot) | 3H₂ (Hidrojen) | 2NH₃ (Amonyak) |
|---|---|---|---|
| Başlangıç | 1 mol | 6 mol | 0 mol |
| Değişim | -1 mol | -3 mol | +2 mol |
| Sonuç | 0 mol (Bitti) | 3 mol (Arttı) | 2 mol (Oluştu) |
Bu tabloda görüldüğü gibi, N₂ tamamen bittiği için sınırlayıcı bileşendir. Ürün miktarı N₂’ye göre hesaplanır.
Biliyor muydunuz?
Araçlardaki hava yastıklarının (airbag) milisaniyeler içinde doğru miktarda şişmesi, sodyum azit (NaN₃) maddesinin stokiyometrik olarak tam hesaplanmış bir tepkimeyle azot gazı açığa çıkarmasına dayanır. Az miktar şişirmez, fazla miktar ise patlamaya neden olabilir!
Tepkime Verimi ve Saflık Hesaplamaları
Kağıt üzerinde hesaplanan maksimum ürün miktarına teorik verim denir. Ancak laboratuvarda yan tepkimeler veya madde kaybı nedeniyle daha az ürün elde edilebilir. Buna gerçek verim denir.
Verim (%) = (Gerçek Verim / Teorik Verim) x 100
Ayrıca, kullanılan ham maddeler %100 saf olmayabilir. Bu durumda hesaplamaya başlamadan önce maddenin saflık yüzdesi üzerinden “net” miktarını bulup mole çevirmelisiniz.
Örnek Stokiyometri Problemi
Soru: 12 gram Magnezyum (Mg) metali yeterli miktarda Oksijen (O₂) ile yakıldığında kaç gram Magnezyum Oksit (MgO) oluşur? (Mg: 24, O: 16)
Çözüm:
- Denkleştirme: 2Mg + O₂ → 2MgO
- Mole Çevirme: n(Mg) = 12g / 24g/mol = 0,5 mol Mg.
- Mol Oranı: Denklemde 2 mol Mg’den 2 mol MgO oluşuyor (1:1 oranı). O halde 0,5 mol Mg’den 0,5 mol MgO oluşur.
- Gram Birimine Dönüş: MgO’nun mol kütlesi = 24 + 16 = 40 g/mol. m(MgO) = 0,5 mol x 40 g/mol = 20 gram MgO oluşur.
💡 İpucu: Her zaman önce birimleri kontrol edin. Soruda verilen ve istenen birimler farklıysa (Litre verilip Gram istenmesi gibi) mol köprüsünü kullanmayı unutmayın.
Sıkça Sorulan Sorular
- Stokiyometri neden zordur? Genellikle mol kavramı eksikliğinden veya denklemi denkleştirmeden işleme başlandığı için zor gelir. Temel adımları izlerseniz sadece oran-orantıdan ibarettir.
- Sınırlayıcı bileşen her zaman miktarı az olan mıdır? Hayır. Miktarı az olan değil, mol sayısı katsayısına bölündüğünde en küçük oranı veren madde sınırlayıcıdır.
- Hacim hesaplamalarında neye dikkat edilmeli? Gazlar için Normal Koşullar (0°C, 1 atm) altında 1 mol gazın 22,4 litre hacim kapladığı bilgisini kullanmalısınız.
Sonuç
Stokiyometri, kimyanın en temel ve uygulama alanı en geniş konularından biridir. Mol kavramını iyi kavramak ve denkleştirilmiş bir denklemi doğru okumak, karmaşık görünen problemleri basit birer matematik işlemine dönüştürür. Sınavlarda ve laboratuvar çalışmalarında başarılı olmak için sınırlayıcı bileşen ve verim hesaplamaları üzerinde bolca pratik yapmanız önerilir. Konuyu daha iyi pekiştirmek için Stokiyometri Çözümlü Örnekler sayfamıza göz atabilir veya bir sonraki aşama olan Gaz Yasaları konusuna geçebilirsiniz.
