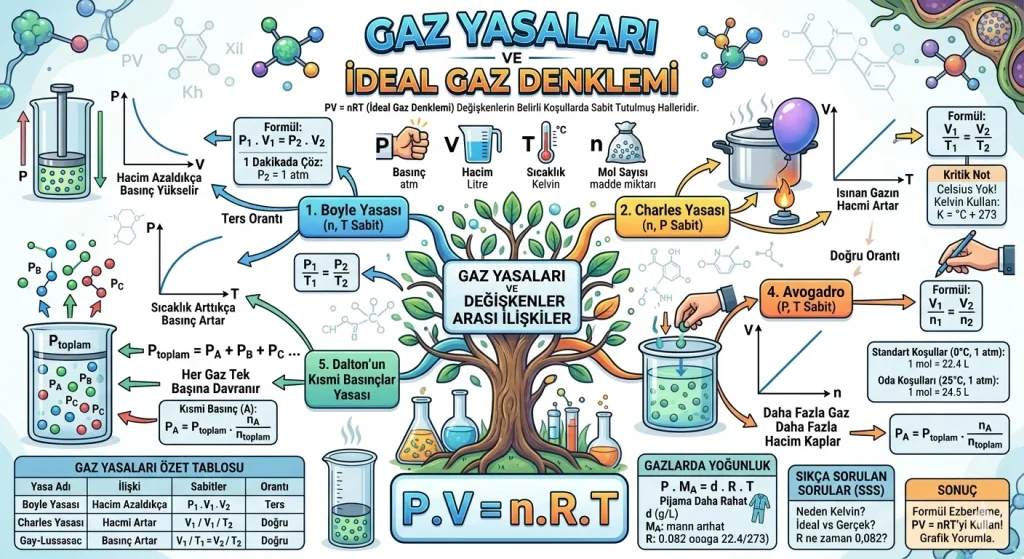
Gaz yasaları; bir gaz örneğinin basınç (P), hacim (V), sıcaklık (T) ve mol sayısı (n) arasındaki matematiksel ilişkileri açıklar. 11. sınıf kimya müfredatının ve AYT Kimya sınavının temel taşlarından biri olan bu yasalar, gazların fiziksel davranışlarını öngörmemizi sağlar. Tüm gaz yasaları, aslında PV = nRT (İdeal Gaz Denklemi) formülündeki değişkenlerin belirli koşullarda sabit tutulmuş halleridir.
Gaz Yasaları Nedir? (Kısa Özet)
Gazların davranışlarını anlamak için dört temel değişkeni bilmek gerekir:
- Basınç (P): Gaz taneciklerinin kap çeperine uyguladığı kuvvettir (Birim: atm).
- Hacim (V): Gazın içinde bulunduğu kabın hacmidir (Birim: Litre).
- Sıcaklık (T): Mutlak sıcaklıktır. Gaz yasalarında daima Kelvin (K) kullanılır.
- Mol Sayısı (n): Gazın madde miktarıdır.
1. Boyle Yasası: Basınç – Hacim İlişkisi
Sabit sıcaklıkta ve sabit miktardaki bir gazın basıncı ile hacmi ters orantılıdır. Hacim azaldıkça birim hacimdeki çarpma sayısı artacağı için basınç yükselir.
Formül: P1 . V1 = P2 . V2
1 Dakikada Çöz: 2 atm basınçta 4 litre hacim kaplayan bir gazın, sıcaklığı sabit tutularak hacmi 8 litreye çıkarılırsa son basıncı ne olur?
Çözüm: 2 . 4 = P2 . 8 => P2 = 1 atm.
2. Charles Yasası: Hacim – Sıcaklık İlişkisi
Sabit basınçta, belirli bir miktar gazın hacmi ile mutlak sıcaklığı doğru orantılıdır. Isınan gazın tanecikleri hızlanır ve kabı genişletmeye çalışır.
Formül: V1 / T1 = V2 / T2
Kritik Not: Hesaplamalarda Celsius (°C) kullanılmaz. Kelvin’e geçiş için: K = °C + 273
3. Gay-Lussac Yasası: Basınç – Sıcaklık İlişkisi
Sabit hacimli kapalı bir kapta, gazın mutlak sıcaklığı arttıkça basıncı da doğru orantılı olarak artar. Düdüklü tencerelerin çalışma prensibi bu yasaya dayanır.
Formül: P1 / T1 = P2 / T2
4. Avogadro Yasası: Mol Sayısı – Hacim İlişkisi
Aynı sıcaklık ve basınç altında, gazların hacimleri ile mol sayıları doğru orantılıdır. Kaba gaz eklemek, sabit basınçlı bir kapta (pistonlu kap) hacmi artırır.
Formül: V1 / n1 = V2 / n2
Önemli Bilgi: Standart Koşullarda (0°C, 1 atm) 1 mol gaz 22,4 L; Oda Koşullarında (25°C, 1 atm) ise 24,5 L hacim kaplar.
5. Dalton’un Kısmi Basınçlar Yasası
Bir gaz karışımının toplam basıncı, karışımı oluşturan gazların tek başlarına uyguladıkları kısmi basınçların toplamına eşittir. Her gaz, sanki kapta tek başınaymış gibi davranır.
Formül: Ptoplam = PA + PB + PC …
Bir gazın kısmi basıncı, mol kesri ile toplam basıncın çarpımına eşittir: PA = Ptoplam . (nA / ntoplam)
İdeal Gaz Denklemi ve Gazlarda Yoğunluk
Tüm yasaların birleşimi olan P.V = n.R.T formülü, gaz problemlerinin çözüm anahtarıdır. Ayrıca gazların yoğunluğunu hesaplamak için şu türetilmiş formül kullanılır:
P . MA = d . R . T (Akılda kalması için: “Pijama Daha Rahat”)
- d: Yoğunluk (g/L)
- MA: Mol kütlesi
- R: İdeal gaz sabiti (0,082 veya 22,4/273)
Gaz Yasaları Özet Tablosu
| Yasa Adı | İlişki | Sabitler | Orantı |
|---|---|---|---|
| Boyle | P – V | n, T | Ters |
| Charles | V – T | n, P | Doğru |
| Gay-Lussac | P – T | n, V | Doğru |
| Avogadro | V – n | P, T | Doğru |
Sıkça Sorulan Sorular (SSS)
Gaz yasalarında neden hep Kelvin kullanılır?
Celsius ölçeğinde 0 ve eksi değerler bulunur. Ancak gaz hacmi veya basıncı matematiksel olarak negatif olamaz. Mutlak sıfır noktasını (0 K) temel alan Kelvin ölçeği, oran-orantı kurmayı mümkün kılar.
İdeal gaz ve gerçek gaz farkı nedir?
İdeal gazlar, tanecikleri arasında etkileşim olmadığı ve tanecik hacminin ihmal edildiği varsayılan gazlardır. Gerçek gazlar ise yüksek sıcaklık ve düşük basınçta idealliğe yaklaşır.
R sabiti ne zaman 0,082 alınır?
Eğer sıcaklık (T) 300 K, 400 K gibi 273’ün katı olmayan değerlerse 0,082 kullanılır. Eğer 273, 546 gibi değerlerse sadeleştirme için 22,4/273 kullanılır.
Sonuç ve Çalışma İpuçları
Gaz yasalarını öğrenirken formül ezberlemek yerine PV = nRT denklemini merkezde tutun. Soruda hangi değişkenlerin sabit olduğunu belirlediğinizde, geri kalanlar arasındaki ilişki kendiliğinden ortaya çıkacaktır. Özellikle gazlarda kinetik teori ve kısmi basınç hesaplamaları konularıyla bu bilgileri birleştirmek, AYT Kimya netlerinizi artıracaktır.
Konuyu pekiştirmek için kimyasal hesaplamalar rehberimize göz atabilir ve bol bol grafik yorumlama sorusu çözebilirsiniz.
