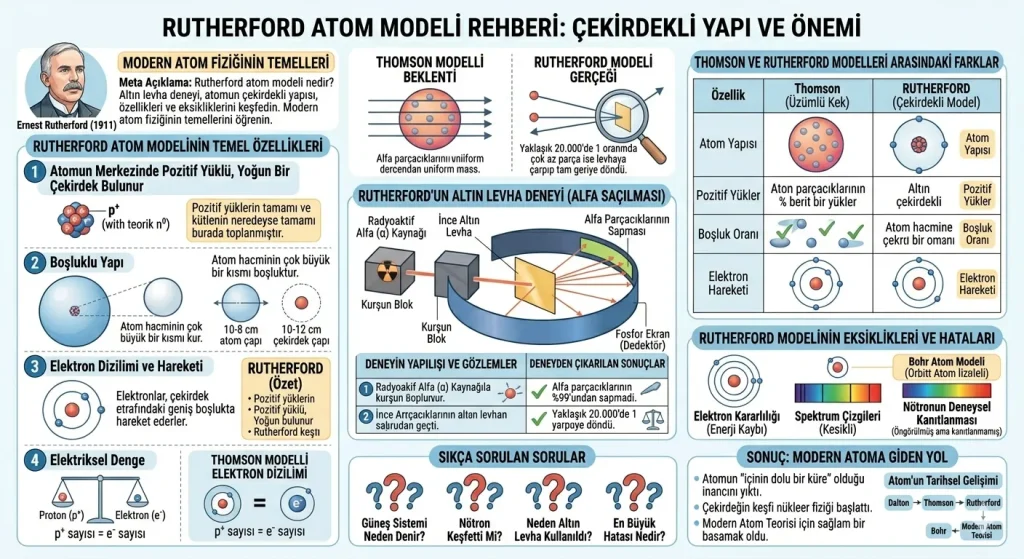
Rutherford atom modeli, modern atom fiziğinin en kritik dönüm noktalarından biridir. 1911 yılında Ernest Rutherford tarafından geliştirilen bu model, atomun merkezinde bir “çekirdek” olduğunu kanıtlayarak bilim dünyasında devrim yaratmıştır. Rutherford, ünlü altın levha deneyi ile atomun büyük kısmının boşluktan oluştuğunu ve pozitif yüklerin merkezde toplandığını ortaya koymuştur.
Rutherford Atom Modeli Nedir? (Özet)
Konuyu hızlıca kavramak isteyenler için Rutherford atom modelinin temel çıkarımları şunlardır:
- Çekirdek Keşfi: Atomun merkezinde pozitif yüklü, yoğun bir çekirdek bulunur.
- Boşluklu Yapı: Atom hacminin çok büyük bir kısmı boşluktur.
- Elektron Dizilimi: Elektronlar, çekirdek etrafındaki geniş boşlukta hareket ederler.
- Kütle Merkezi: Atomun kütlesinin neredeyse tamamı çekirdekte toplanmıştır.
- Elektriksel Denge: Atomdaki pozitif yük (proton) sayısı, negatif yük (elektron) sayısına eşittir.
Daha önceki model olan Thomson Atom Modeli hakkında bilgi alarak aradaki farkı daha iyi anlayabilirsiniz.
Rutherford’un Altın Levha Deneyi (Alfa Saçılması)
Ernest Rutherford, atomun yapısını test etmek için radyoaktif bir kaynaktan çıkan pozitif yüklü alfa (α) parçacıklarını ince bir altın levha üzerine göndermiştir. Bu deney, o dönem kabul gören “üzümlü kek” modelinin doğruluğunu sorgulamak amacıyla yapılmıştır.
Deneyin Yapılışı ve Gözlemler
Rutherford, deney sırasında şu kritik gözlemleri yapmıştır:
- Alfa parçacıklarının %99’undan fazlası levhadan sapmadan doğrudan geçmiştir.
- Bazı parçacıklar levhaya çarptıktan sonra küçük açılarla yön değiştirmiştir.
- Yaklaşık 20.000’de 1 oranında çok az parça ise levhaya çarpıp tam geriye dönmüştür.
Deneyden Çıkarılan Sonuçlar
Bu gözlemler atom hakkında iki devrimsel gerçeği kanıtlamıştır: Parçacıkların çoğunun doğrudan geçmesi atomun büyük kısmının boşluk olduğunu; çok azının geri dönmesi ise merkezde pozitif yüklü, yoğun bir kütlenin (çekirdek) varlığını gösterir.
Rutherford Atom Modelinin Temel Özellikleri
Rutherford, deney sonuçlarına dayanarak atomun yapısını şu maddelerle tanımlamıştır:
- Atomun merkezinde pozitif yüklü ve kütlesi yoğun “çekirdek” yer alır.
- Çekirdeğin çapı (10-12 cm), atomun çapına (10-8 cm) oranla çok küçüktür.
- Elektronlar, çekirdek dışındaki geniş boşluklarda sürekli hareket halindedir.
- Protonların toplam kütlesi, atom kütlesinin yaklaşık yarısıdır; bu da çekirdekte yüksüz parçacıkların (nötron) varlığına işaret eder.
Rutherford’dan sonra geliştirilen Bohr Atom Modeli ile elektronların yörüngeleri daha net açıklanmıştır.
Rutherford Atom Modelinin Eksiklikleri
Rutherford modeli büyük bir ilerleme olsa da klasik fizik kuralları nedeniyle bazı noktaları açıklayamamıştır:
- Elektron Kararlılığı: Çekirdek etrafında dönen elektronların neden enerji kaybedip çekirdeğe düşmediğini açıklayamamıştır.
- Spektrum Çizgileri: Atomların yaydığı ışık spektrumlarının neden kesikli (çizgisel) yapıda olduğunu izah edememiştir.
- Nötronun Kanıtlanması: Yüksüz bir parçacığın varlığını öngörmüş ancak nötronu deneysel olarak kanıtlayamamıştır (Nötron, 1932’de James Chadwick tarafından keşfedilmiştir).
Thomson ve Rutherford Modelleri Arasındaki Farklar
Bilimsel gelişimi anlamak için iki model arasındaki temel farkları aşağıdaki tabloda inceleyebilirsiniz:
| Özellik | Thomson (Üzümlü Kek) | Rutherford (Çekirdekli Model) |
|---|---|---|
| Atom Yapısı | Pozitif yüklü küre içinde dağılmış elektronlar. | Merkezde çekirdek, etrafında büyük boşluklar. |
| Pozitif Yükler | Atomun her yerine homojen dağılmıştır. | Küçük bir merkezde (çekirdekte) toplanmıştır. |
| Boşluk Oranı | Atom dolu bir küredir, boşluk yoktur. | Atomun hacminin %99’undan fazlası boşluktur. |
| Elektron Hareketi | Hareketsiz ve gömülü haldedir. | Çekirdek etrafında hareket halindedir. |
Sıkça Sorulan Sorular (SSS)
Rutherford atom modeline neden “Güneş Sistemi Modeli” denir?
Merkezdeki çekirdeği Güneş’e, çevresinde dönen elektronları ise gezegenlere benzettiği için bu isimle anılır.
Rutherford nötronu keşfetti mi?
Hayır, Rutherford çekirdekte yüksüz bir parçacık olması gerektiğini teorik olarak öngörmüştür ancak nötronu 1932’de James Chadwick keşfetmiştir.
Altın levha deneyinde neden altın kullanıldı?
Altın, atomik düzeyde inceltilebilen (yüksek dövülebilirlik) nadir metallerdendir. Rutherford, alfa parçacıklarının geçebileceği kadar ince bir yüzey için altını tercih etmiştir.
Rutherford modelinin en büyük hatası nedir?
Elektronların ivmeli hareket yaparken neden enerji kaybedip çekirdeğe düşmediğini klasik fizik yasalarıyla açıklayamamasıdır.
Sonuç: Modern Atoma Giden Yol
Rutherford atom modeli, atomun “içinin dolu bir küre” olduğu inancını yıkarak nükleer fiziğin kapılarını açmıştır. Çekirdeğin keşfi, kimya ve fizik disiplinlerinde yeni bir çağ başlatmıştır. Elektronların hareketi konusundaki eksiklikleri, kendisinden sonra gelen Modern Atom Teorisi için sağlam bir basamak oluşturmuştur.
Atomun tarihsel gelişimi hakkında daha fazla bilgi için Dalton Atom Modeli yazımıza da göz atabilirsiniz.
