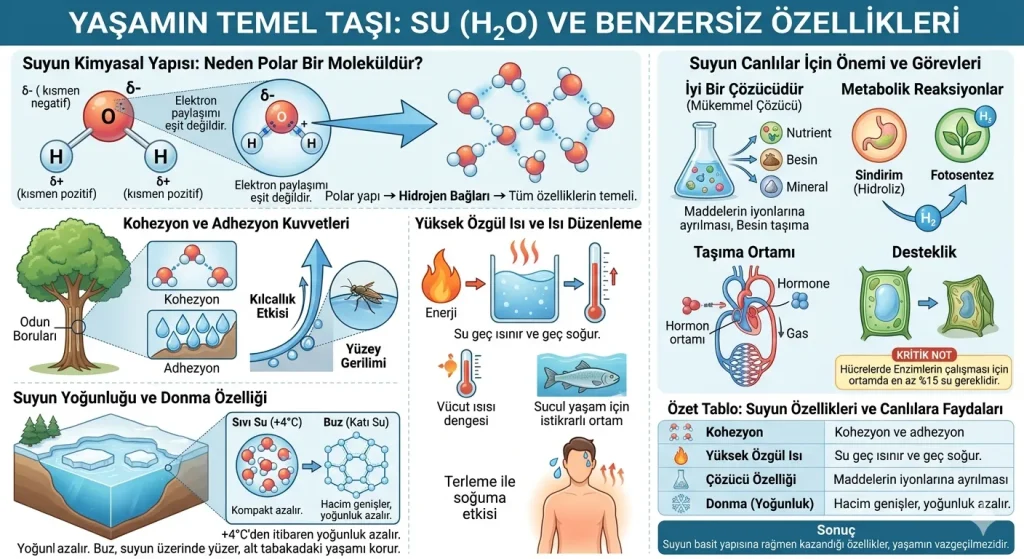
Kısa Özet: Su, iki hidrojen ve bir oksijen atomundan oluşan, yaşamın devamlılığı için zorunlu olan inorganik bir bileşiktir. Polar yapısı ve molekülleri arasındaki hidrojen bağları sayesinde kohezyon, yüksek özgül ısı ve mükemmel çözücü olma gibi benzersiz özelliklere sahiptir.
Su (H₂O), dünyadaki yaşamın temel taşıdır. Canlı organizmaların büyük bir kısmını oluşturan bu molekül, sadece bir içecek değil, biyolojik süreçlerin tamamının gerçekleştiği temel ortamdır. İnorganik bileşikler arasında yer alan su, kimyasal yapısı gereği diğer maddelerden ayrılan ve yaşamı mümkün kılan çok özel fiziksel özelliklere sahiptir.
Suyun Kimyasal Yapısı: Neden Polar Bir Moleküldür?
Bir su molekülü, bir oksijen atomuna kovalent bağlarla bağlanmış iki hidrojen atomundan oluşur. Ancak bu bağlardaki elektron paylaşımı eşit değildir. Oksijen atomu, elektronları hidrojenlere göre daha kuvvetli çeker. Bu durum, molekülün oksijen tarafının kısmen negatif (δ-), hidrojen tarafının ise kısmen pozitif (δ+) yüklü olmasına neden olur.
Zıt kutuplara sahip olan bu yapıya polarite denir. Suyun polar olması, komşu su moleküllerinin birbirini çekmesini sağlar. Bu çekim kuvveti sonucunda moleküller arasında hidrojen bağları kurulur. Suyun sahip olduğu tüm “sıra dışı” özelliklerin temelinde bu zayıf ama sayıca çok olan hidrojen bağları yatar.
Suyun Temel Fiziksel ve Kimyasal Özellikleri
Suyun biyolojik sistemlerdeki başarısı, fiziksel prensiplerle doğrudan ilişkilidir. Bu özellikler, bitkilerin en üst yapraklarına su taşımasından, vücut ısımızın korunmasına kadar pek çok hayati noktada devreye çıkar.
Kohezyon ve Adhezyon Kuvvetleri
- Kohezyon: Aynı cins moleküllerin (su moleküllerinin) hidrojen bağları sayesinde birbirini tutmasıdır. Bu kuvvet, suyun bir bütün halinde kalmasını sağlar.
- Adhezyon: Su moleküllerinin farklı yüzeylere (örneğin bir bitkinin odun borularına) tutunma eğilimidir.
Kohezyon ve adhezyon kuvvetleri birlikte çalışarak suyun yerçekimine zıt yönde hareket etmesine (kılcallık) olanak tanır. Bu sayede devasa ağaçların en uç dallarına kadar su taşınabilir.
Yüzey Gerilimi ve Kılcallık Etkisi
Kohezyon kuvveti, suyun yüzeyinde sanki görünmez bir zar varmış gibi bir direnç oluşturur. Buna yüzey gerilimi denir. Bazı böceklerin suyun üzerinde batmadan yürüyebilmesi bu fiziksel olay sayesinde gerçekleşir. Kılcallık ise suyun dar borularda yükselme yeteneğidir ve adhezyon kuvvetiyle desteklenir.
Yüksek Özgül Isı ve Isı Düzenleme
Suyun özgül ısısı oldukça yüksektir. Bu, suyun sıcaklığını 1 derece artırmak için çok fazla enerji gerektiği anlamına gelir. Su, geç ısınır ve geç soğur. Bu özellik canlılar için şu avantajları sağlar:
- Canlıların vücut ısısı ani dış sıcaklık değişimlerinden korunur.
- Deniz ve okyanuslardaki sıcaklık değişimleri yavaş gerçekleşir, bu da sucul yaşam için istikrarlı bir ortam sunar.
- Terleme yoluyla vücuttan su atıldığında, su buharlaşırken vücuttan yüksek miktarda ısıyı da beraberinde götürür (soğutma etkisi).
Suyun Yoğunluğu ve Donma Özelliği
Maddelerin çoğu donduğunda büzülür ve yoğunluğu artar. Ancak su, +4°C’den itibaren soğumaya devam ettiğinde hacmi genişler ve yoğunluğu azalır. Bu yüzden buz, suyun üzerinde yüzer.
Bu durum göllerin ve denizlerin üstten donmasını sağlar. Suyun alt kısmı sıvı kaldığı için su altındaki canlılık kış aylarında da devam edebilir. Buz tabakası aynı zamanda bir yalıtım görevi görerek aşağıdaki suyun aşırı soğumasını engeller.
Suyun Canlılar İçin Önemi ve Görevleri
Su, canlıların temel bileşenleri arasında en yüksek orana sahip olan maddedir. Temel görevleri şunlardır:
- İyi Bir Çözücüdür: Polar yapısı sayesinde birçok maddeyi çözer. Besinlerin hücrelere taşınması ve atıkların vücuttan uzaklaştırılması su sayesinde olur.
- Metabolik Reaksiyonlar: Sindirim (hidroliz) reaksiyonlarında su harcanır. Ayrıca fotosentez denklemi içerisinde hidrojen kaynağı olarak kullanılır.
- Taşıma Ortamı: Kanın büyük bir kısmı sudur; hormonları, besinleri ve gazları taşır.
- Desteklik: Bitkilerde turgor basıncı oluşturarak dik durmalarını sağlar.
Kritik Not: Hücrelerdeki enzimlerin özellikleri gereği, çalışabilmeleri için ortamda belirli bir oranda su bulunması şarttır. Su oranı %15’in altına düştüğünde enzim faaliyeti durur ve hayat durma noktasına gelir.
Özet Tablo: Suyun Özellikleri ve Canlılara Faydaları
| Özellik | Açıklama | Canlılar İçin Önemi |
|---|---|---|
| Kohezyon | Su moleküllerinin birbirini tutması | Bitkilerde suyun yükseğe taşınmasını sağlar. |
| Yüksek Özgül Isı | Sıcaklık değişimine direnç | Vücut ısısının dengede kalmasını sağlar. |
| Çözücü Özelliği | Maddeleri iyonlarına ayırma | Madde taşınması ve metabolizma için ortam hazırlar. |
| Donma (Yoğunluk) | Buzun sudan hafif olması | Su kütlelerinin alttan donmasını önler, yaşamı korur. |
Sıkça Sorulan Sorular (SSS)
Kohezyon ve adhezyon arasındaki fark nedir?
Kohezyon, aynı cins moleküllerin (su-su) birbirini tutmasıdır; adhezyon ise farklı cins moleküllerin (su-yüzey) birbirine tutunmasıdır.
Suyun özgül ısısının yüksek olması canlılara ne sağlar?
Suyun geç ısınıp geç soğumasını sağlayarak canlıların vücut ısısının dengede kalmasına ve ekosistemlerdeki sıcaklık değişimlerinin yavaş olmasına yardımcı olur.
Buz neden suyun üzerinde yüzer?
Su donduğunda molekülleri arasındaki mesafe artar ve hacmi genişler. Bu durum yoğunluğun azalmasına neden olur, böylece buz suyun üzerinde kalarak alt tabakadaki yaşamı izole eder.
Enzimlerin çalışması için neden en az %15 su gereklidir?
Enzimler sulu bir ortamda üç boyutlu yapılarını korur ve substratları ile etkileşime girebilir. Su oranı %15’in altına düştüğünde moleküler hareketlilik kısıtlanır ve enzim faaliyeti durur.
Sonuç
Su, kimyasal yapısındaki basitliğe rağmen sunduğu fiziksel ve biyolojik avantajlarla yaşamın vazgeçilmezidir. Polar yapısı ve hidrojen bağları sayesinde kazandığı özellikler, küresel iklim dengesinden hücre içindeki en küçük biyokimyasal tepkimeye kadar her süreci doğrudan etkiler. Suyun bu özelliklerini kavramak, biyolojinin temelini ve yaşamın nasıl sürdürüldüğünü anlamak adına en kritik adımdır.
