
İyonik bağ, bir atomdan bir veya daha fazla elektronun tamamen koparak başka bir atoma geçmesi sonucu oluşan, zıt yüklü iyonlar arasındaki çekim kuvvetidir. Bu bağ türü en sık metal ve ametal atomları arasında görülür.
İyonik bağ oluştuğunda:
- Elektron veren atom pozitif iyon (katyon) olur.
- Elektron alan atom negatif iyon (anyon) olur.
- Katyon ve anyon arasındaki elektrostatik çekim iyonik bağı oluşturur.
Buna en güzel örnek sofra tuzudur. Sodyum klorür (Na+Cl-) oluşturmak üzere sodyum ve klor atomları bir araya geldiğinde, her sodyum atomunun bir değerlik elektronu bir klor atomunun değerlik elektron katmanına aktarılarak bağ kurulur.
İyonik Bağ Neden Oluşur?
Atomlar bağ oluştururken daha kararlı bir elektron dizilimine ulaşmak ister. İyonik bağda bu kararlılık genellikle şöyle sağlanır:
- Metal atomları elektron vererek dış katmanını daha kararlı hâle getirir.
- Ametal atomları elektron alarak dış katmanını tamamlamaya yaklaşır.
Bu süreçte atomlar çoğu zaman soygazlara benzer bir düzen elde eder.
İyonik Bağ Nasıl Oluşur? (Adım Adım)
İyonik bağın mantığı “elektron alışverişi”dir.
Örnek: NaCl (Sodyum Klorür)
- Sodyum (Na) dış katmanındaki 1 elektronu verir.
- Sodyum → Na⁺ (katyon) olur.
- Klor (Cl) bu elektronu alır.
- Klor → Cl⁻ (anyon) olur.
- Na⁺ ve Cl⁻ birbirini çeker → iyonik bağ oluşur.
Önemli not: İyonik bileşiklerde “molekül” yapısından çok, düzenli bir kristal örgü (iyonik kristal) yapısı vardır.
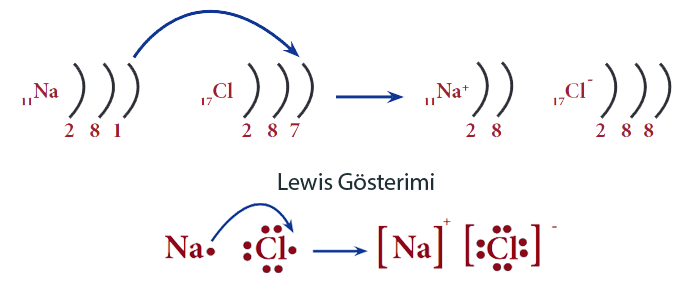
Oluşan iyonlar zıt yüklü olduklarından birbirlerini elektrostatik çekim kuvvetiyle çeker ve sodyum klorür kristali oluşur. Oluşan kristal ayılamayacak kadar çok sayıda sodyum ve klor iyonlarından oluşur.
İyonik Bağın Özellikleri
İyonik bağlı maddeler (iyonik bileşikler) genel olarak şu özellikleri gösterir:
1) Kristal Yapı Oluştururlar
İyonlar rastgele durmaz; artı ve eksi iyonlar düzenli bir şekilde dizilerek kristal örgü oluşturur.
2) Erime ve Kaynama Noktaları Genellikle Yüksektir
Zıt yüklü iyonlar arasındaki çekim kuvveti güçlü olduğu için bu yapıyı bozmak (eritmek) yüksek enerji gerektirir.
3) Katı Hâldeyken Elektrik İletmezler
Katı hâlde iyonlar sabittir, hareket edemez. Hareket olmayınca elektrik akımı da oluşmaz.
4) Erimiş Hâldeyken veya Suda Çözündüğünde Elektrik İletirler
Eridiğinde veya suda çözündüğünde iyonlar serbestçe hareket edebilir.
Bu yüzden elektrolit davranışı gösterirler.
5) Genellikle Sert ve Kırılgandırlar
Kristal yapı güçlüdür ama darbe alınca iyon katmanları kayabilir ve aynı yükler yan yana gelince itme olur. Bu da kırılganlığa yol açar.
6) Çözünürlük Davranışı Değişkendir
Birçok iyonik bileşik suda çözünür; fakat her iyonik bileşik suda çözünmek zorunda değildir. Çözünme, iyonların ve su moleküllerinin etkileşimine bağlıdır.
İyonik Bağ ile Kovalent Bağ Arasındaki Fark
| Özellik | İyonik Bağ | Kovalent Bağ |
| Elektron davranışı | Alışveriş | Paylaşım |
| Atom türleri | Metal + Ametal | Ametal + Ametal |
| Yapı | Kristal örgü | Molekül |
| Katı hâlde iletkenlik | İletmez | Genelde iletmez |
| Erimiş/suda iletkenlik | İletir | Genelde iletmez |
| Erime noktası | Genelde yüksek | Düşük–orta |
İyonik Bağa Örnekler
- NaCl (Sofra tuzu)
- MgO (Magnezyum oksit)
- CaCl₂ (Kalsiyum klorür)
- KBr (Potasyum bromür)
Günlük hayatta tuzlar, bazı gübreler ve birçok mineral iyonik bağlı bileşiklerdir.
Sık Sorulan Sorular
İyonik bileşikler molekül mü?
Genellikle “molekül” gibi düşünmek doğru değildir. İyonik bileşikler çoğunlukla düzenli kristal örgü oluşturur.
İyonik bağ her zaman metal–ametal arasında mı olur?
En yaygın şekli budur. Çünkü metal elektron vermeye, ametal elektron almaya yatkındır.
İyonik bağlı maddeler neden katı hâlde elektrik iletmez?
Çünkü iyonlar kristal yapıda sabittir; hareket eden yük taşıyıcısı yoktur.
Kısa Özet
- İyonik bağ, elektron alışverişi sonucu oluşur.
- Zıt yüklü katyon–anyon çekimi ile oluşur.
- Kristal yapı, yüksek erime noktası ve eriyik/suda iletkenlik tipiktir.
Ayrıca Bakın (İç link önerileri)
- Kimyasal Bağ Nedir?
- Kovalent Bağ Nedir?
- Metalik Bağ Nedir?
- Atom Nedir?
- Molekül Nedir?
- Elektrik Yükleri (Pozitif–Negatif)
- İletken ve Yalıtkan Nedir?
