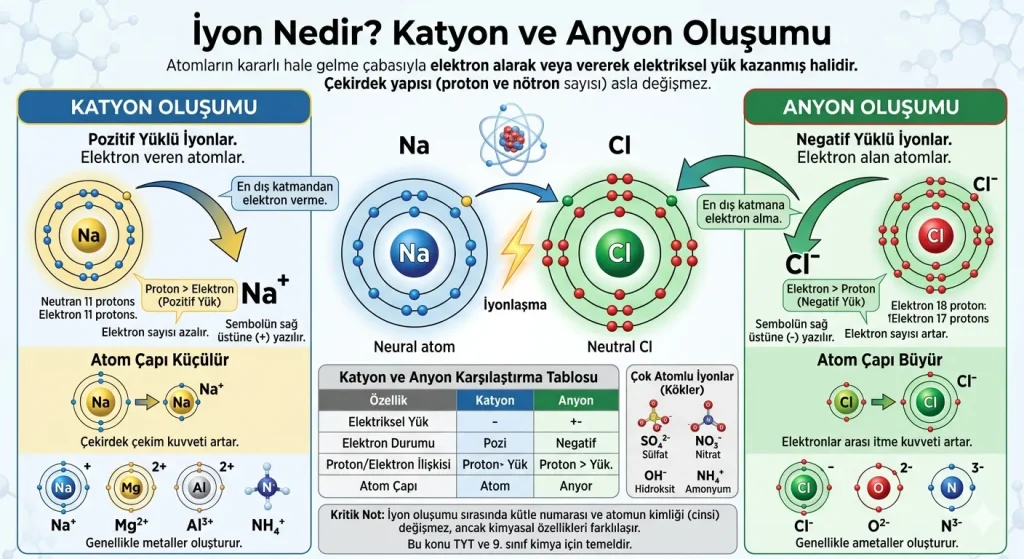
Kimya biliminin temel taşlarından biri olan iyon kavramı, atomların kararlı hale gelme çabasının bir sonucudur. En basit tanımıyla iyon; elektron alarak veya vererek elektriksel yük kazanmış atom ya da atom gruplarına denir. Doğada atomlar genellikle nötr haldedir, ancak kimyasal tepkimeler sırasında elektron alışverişi yaparak pozitif veya negatif yükle yüklenirler.
İyonların Temel Özellikleri
- Nötr bir atomda proton (pozitif) ve elektron (negatif) sayıları birbirine eşittir.
- Elektron alışverişi gerçekleştiğinde bu denge bozulur ve atom “iyon” haline gelir.
- Elektron kaybeden atomlar pozitif (+), elektron kazanan atomlar ise negatif (-) yükle yüklenir.
- İyonlar, kimyasal bağların oluşumunda ve maddelerin elektriksel iletkenliğinde kritik rol oynarlar.
İyon Nasıl Oluşur?
Atomlar, genellikle en dış katmanlarındaki elektron sayısını sekize (oktet) veya ikiye (dublet) tamamlayarak soygaz kararlılığına ulaşmak isterler. Bu süreçte gerçekleşen elektron alışverişi iyonlaşmayı sağlar. Daha kapsamlı bir temel için atomun yapısı ve özellikleri konusuna göz atabilirsiniz.
Kritik Not: İyon oluşumu sırasında atomun çekirdek yapısı (proton ve nötron sayısı) asla değişmez. Yalnızca elektron sayısı değiştiği için atomun kütle numarası sabit kalır ve atomun kimliği (cinsi) değişmez; ancak kimyasal özellikleri farklılaşır.
Katyon Nedir? (Pozitif Yüklü İyonlar)
Bir atomun dışarıya bir veya daha fazla elektron vermesi sonucunda oluşan pozitif yüklü iyonlara katyon denir. Elektron kaybeden bir atomda, çekirdekteki artı yüklü protonların sayısı, eksi yüklü elektronların sayısından fazla hale gelir.
Katyonların Özellikleri ve Örnekleri
- Genellikle metaller elektron vererek katyon oluşturma eğilimindedir.
- Katyon oluşurken atomun çapı küçülür; çünkü elektron başına düşen çekirdek çekim kuvveti artar.
- Sembolün sağ üst köşesine “+” işareti ve verilen elektron sayısı yazılır.
Sık Karşılaşılan Katyonlar:
- Sodyum (Na+): 1 elektron vermiştir.
- Magnezyum (Mg2+): 2 elektron vermiştir.
- Alüminyum (Al3+): 3 elektron vermiştir.
- Amonyum (NH4+): Çok atomlu bir katyon köküdür.
Anyon Nedir? (Negatif Yüklü İyonlar)
Bir atomun dışarıdan elektron alması sonucunda oluşan negatif yüklü iyonlara anyon denir. Elektron alan bir atomda, eksi yüklü elektronların sayısı artı yüklü protonların sayısını geçer. Bu dengesizlik sonucunda atom “-” yükle yüklenir.
Anyonların Özellikleri ve Örnekleri
- Genellikle ametaller elektron alarak anyon oluşturma eğilimindedir.
- Anyon oluşurken atomun çapı büyür; çünkü artan elektronlar arası itme kuvveti hacmi genişletir.
- Sembolün sağ üst köşesine “-” işareti ve alınan elektron sayısı yazılır.
Sık Karşılaşılan Anyonlar:
- Klorür (Cl–): 1 elektron almıştır.
- Oksit (O2-): 2 elektron almıştır.
- Nitrür (N3-): 3 elektron almıştır.
Elementlerin iyonlaşma eğilimlerini daha iyi anlamak için periyodik sistem ve elementler içeriğimizi inceleyebilirsiniz.
Katyon ve Anyon Arasındaki Temel Farklar
| Özellik | Katyon | Anyon |
|---|---|---|
| Elektriksel Yük | Pozitif (+) | Negatif (-) |
| Elektron Durumu | Elektron vermiştir. | Elektron almıştır. |
| Proton/Elektron İlişkisi | Proton > Elektron | Elektron > Proton |
| Atom Çapı | Nötr haline göre küçülür. | Nötr haline göre büyür. |
| Genel Kaynak | Genellikle metaller. | Genellikle ametaller. |
Çok Atomlu İyonlar (Kökler) Nelerdir?
İyonlar her zaman tek bir atomdan oluşmaz. Birden fazla atomun birbirine bağlanarak oluşturduğu ve üzerinde net bir yük taşıyan gruplara kök veya çok atomlu iyon denir. Kimyasal tepkimelerde bu gruplar genellikle tek bir birim gibi hareket ederler.
- Sülfat (SO42-): Yaygın bir anyon köküdür.
- Nitrat (NO3–): Dinamik bir anyon köküdür.
- Hidroksit (OH–): Bazik özellik gösteren bir köktür.
- Amonyum (NH4+): Pozitif yüklü nadir köklerden biridir.
Sıkça Sorulan Sorular (SSS)
1. Bir atom nasıl katyon haline gelir?
Bir atom dışarıya elektron verdiğinde, proton sayısı elektron sayısından fazla olur ve atom pozitif (+) yüklü bir katyona dönüşür.
2. Nötr bir atom iyon olduğunda kütle numarası değişir mi?
Hayır. İyon oluşumu sadece elektron alışverişiyle ilgilidir. Proton ve nötron sayısı (çekirdek yapısı) değişmediği için kütle numarası sabit kalır.
3. Anyonlar elektron alır mı verir mi?
Anyonlar dışarıdan elektron alarak negatif (-) yükle yüklenen atom veya atom gruplarıdır.
4. İyonlaşma sırasında atomun kimliği değişir mi?
Hayır. Atomun kimliğini proton sayısı belirler. İyonlaşmada sadece elektron sayısı değiştiği için atomun cinsi aynı kalır, ancak fiziksel ve kimyasal özellikleri değişir.
Sonuç
İyon kavramı, kimyanın en temel konularından biridir ve maddelerin nasıl etkileşime girdiğini anlamamızı sağlar. Katyonlar elektron vererek “+” yüklenen atomlarken, anyonlar elektron alarak “-” yüklenen atomlardır. Bu elektron alışverişi, atomların daha kararlı bir yapıya ulaşmasını sağlar. Özellikle TYT ve 9. sınıf kimya sınavlarında kritik öneme sahip olan bu konuyu kavramak, kimyasal bağlar ve bileşik adlandırma gibi ileri seviye konular için sağlam bir temel oluşturur.
